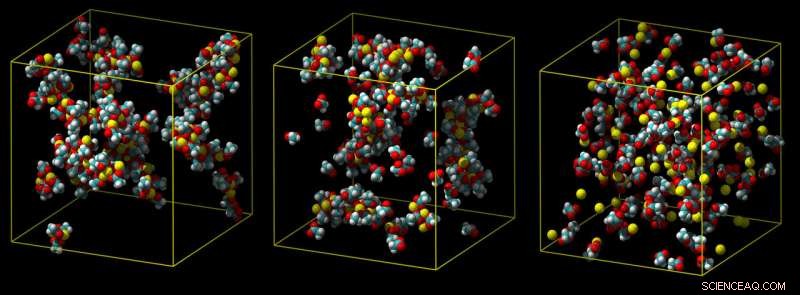
Un modello standard del calcio sopravvaluta la forza con cui il calcio si lega, portando a gruppi di coppie ioniche (a sinistra). Un modello intermedio mostra meno grumi (al centro), e un raffinato modello in scala di carica predice correttamente un'associazione debole con i gruppi carbossilici nell'acqua (non mostrato) (a destra). Credito:Philip Mason ed Elise Duboue-Dijon
Il calcio è essenziale per il funzionamento del nostro corpo. Gli ioni di calcio consentono alle cellule di comunicare tra loro, permettendo ai neuroni di interagire, muscoli a contrarsi, e le cellule muscolari del cuore per sincronizzarsi e battere. Per comprendere meglio questi processi, in cui gli ioni calcio interagiscono con molecole biologiche come proteine, i ricercatori usano spesso simulazioni al computer. Ma i modelli accurati sono impegnativi e computazionalmente costosi.
"Se hai il modello sbagliato di calcio, semplicemente non funzionerà, " ha affermato Pavel Jungwirth dell'Istituto di chimica organica e biochimica dell'Accademia delle scienze ceca a Praga. "La maggior parte dei modelli disponibili non sono sufficientemente precisi per catturare le importanti caratteristiche dello ione calcio".
Nel numero di questa settimana di Il Giornale di Fisica Chimica , però, Il gruppo di ricerca di Jungwirth dimostra come una semplice modifica in un modello al computer porti a simulazioni altamente accurate, che servono come potenti strumenti per studiare una serie di processi biologici. "Credo che in questo momento abbiamo il meglio dei semplici modelli di calcio al mondo, " disse Jungwirth.
Gli ioni di calcio viaggiano da cellula a cellula come messaggeri. Quando raggiungono una cella, si legano a una molecola, come una proteina, innescando una cascata di risposte chimiche. Ma a causa dell'ambiente acquoso dello ione, simulare esattamente come si lega il calcio è difficile.
Lo ione calcio, che è doppiamente caricato positivamente, interagisce fortemente con gli ossigeni delle molecole d'acqua circostanti. Questi ossigeni hanno una parziale carica negativa (come nella molecola dell'acqua) e l'atomo di ossigeno attrae più efficacemente gli elettroni dei legami. Le forze elettrostatiche tra calcio e acqua inducono le molecole d'acqua a riorganizzarsi attorno allo ione. Lo ione calcio costringe anche gli elettroni nella molecola d'acqua a spostarsi, un fenomeno chiamato polarizzazione elettronica.
La maggior parte delle simulazioni incorpora il riarrangiamento delle molecole d'acqua. Ma poiché calcolare esattamente come si muovono gli elettroni richiede troppa potenza di calcolo, non tengono conto della polarizzazione elettronica. Senza polarizzazione elettronica, Jungwirth ha detto, le simulazioni che coinvolgono il calcio sono imprecise.
Tipicamente, le interazioni con le molecole d'acqua funzionano per allontanare uno ione calcio dalla molecola con cui sta cercando di legarsi, come in un tiro alla fune molecolare. Se una simulazione non tiene pienamente conto di questi effetti, sopravvaluta la forza con cui il calcio si lega, producendo ioni che non possono separarsi, che non è realistico.
Alcuni anni fa, però, Alexei Stuchebrukhov e Igor Leontyev hanno proposto una soluzione:abbassare la carica elettrica degli ioni nelle simulazioni. Si scopre che ridimensionare la carica di un fattore di circa 0,75 imita l'effetto della polarizzazione elettronica. Inoltre, un ridimensionamento così semplice non aggiunge alcun onere computazionale aggiuntivo.
"È quasi un miracolo, " ha detto Jungwirth. "Sappiamo che non è una soluzione perfetta, ma forse risolve il 90% del problema".
In precedenza, Il team di Jungwirth ha testato la strategia modellando l'interazione relativamente semplice tra gli ioni calcio e cloruro. Per verificare se le simulazioni erano accurate e se il ridimensionamento funzionava, hanno fatto esplodere soluzioni di cloruro di calcio reali con neutroni. Misurando come quei neutroni si sono dispersi dal cloruro di calcio acquoso, i ricercatori ne hanno dedotto la struttura e hanno confrontato i dati con le simulazioni.
Nel nuovo studio, i ricercatori hanno testato il loro modello con gruppi carbossilici, gruppi molecolari presenti nelle proteine, e quindi più rilevante per la biologia. Dopo aver regolato anche la carica del gruppo carbossilico, hanno nuovamente dimostrato che le loro simulazioni combaciavano molto bene con i dati degli esperimenti di diffusione di neutroni.
Poiché i gruppi carbossilici sono semplici rispetto a, dire, una proteina intera, i ricercatori potrebbero anche descrivere le interazioni del calcio utilizzando calcoli di strutture elettroniche accurati ma computazionalmente costosi. Confrontando questi calcoli con le simulazioni, hanno nuovamente confermato l'accuratezza dei loro modelli.
Questi test mostrano che il nuovo modello può simulare le interazioni del calcio con quasi tutte le proteine, ha detto Jungwirth. I ricercatori hanno anche sviluppato un modello analogo che funziona per le interazioni del calcio con i fosfolipidi sulla membrana cellulare. Il prossimo passo, Egli ha detto, è fare lo stesso con le molecole di DNA e RNA. E più avanti, i ricercatori hanno in programma di sviluppare un modello simile per il magnesio, un altro importante ione di segnalazione con le sue sfide uniche.