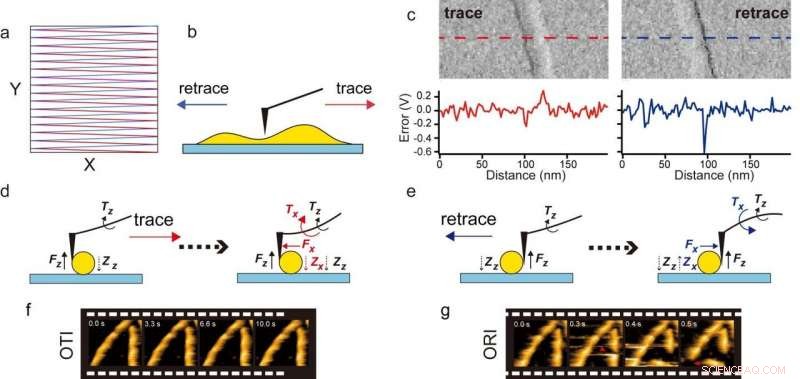
(a) Scansione raster:scansione di traccia (linea rossa) e scansione di ritraccia (linea blu) della fase del campione, (b) direzioni di scansione della punta rispetto al campione nei processi di scansione di traccia e ritraccia, (c) differenza nell'errore di controllo del feedback tra i processi di scansione traccia e ritraccia. Immagini di errore del filamento di actina orientato quasi lungo l'asse Y (in alto) e il profilo di errore (in basso), (D, e) differenza nelle direzioni delle coppie prodotte dalle forze laterali e verticali esercitate sul cantilever dal campione durante i processi di scansione di traccia (d) e ritraccia (e), (F, g) Immagini HS-AFM di filamenti di actina catturati a 10 fps nelle modalità OTI (f) e ORI (g). In modalità ORI, filamenti di actina sono stati rapidamente rotti. Credito:Università di Kanazawa
La microscopia a forza atomica ad alta velocità (HS-AFM) è una tecnica di imaging che può essere utilizzata per visualizzare processi biologici, per esempio l'attività delle proteine. Oggi, i frame rate tipici di HS-AFM raggiungono i 12 frame al secondo. Al fine di migliorare le capacità del metodo, in modo che possa essere applicato a una gamma sempre più ampia di campioni biologici, sono necessarie velocità video migliori, anche se. Inoltre, tempi di registrazione più rapidi implicano una minore interazione tra il campione e la sonda, una punta che scansiona la superficie del campione, rendendo la procedura di imaging meno invasiva. Ora, Shingo Fukuda e Toshio Ando del Nano Life Science Institute (WPI-NanoLSI), L'Università di Kanazawa ha sviluppato un approccio HS-AFM alternativo per aumentare la frequenza dei fotogrammi fino a 30 fotogrammi al secondo.
Un'immagine AFM viene generata spostando lateralmente una punta appena sopra la superficie di un campione. Durante questo movimento di scansione xy, la posizione della punta nella direzione perpendicolare al piano xy (la coordinata z) seguirà il profilo di altezza del campione. La variazione della coordinata z della punta produce quindi una mappa dell'altezza, l'immagine del campione.
Fukuda e Ando hanno lavorato su HS-AFM nella cosiddetta modalità di modulazione di ampiezza. La punta viene quindi fatta oscillare con un'ampiezza impostata. Durante la scansione di una superficie, l'ampiezza dell'oscillazione cambierà a causa delle variazioni di altezza nella struttura del campione. Per tornare all'ampiezza originale, è necessario apportare una correzione alla distanza punta-campione. Quanto deve essere grande la correzione è correlato alla topologia della superficie del campione, ed è dettato dal cosiddetto errore di controllo in retroazione del setup. Gli scienziati hanno notato che l'errore di controllo del feedback è diverso quando la punta si muove in direzioni opposte, chiamato tracciare e ripercorrere. Questa differenza è in definitiva dovuta alle diverse forze fisiche in gioco quando la punta viene "tirata" (traccia) e quando viene "spinta" (ritraccia).
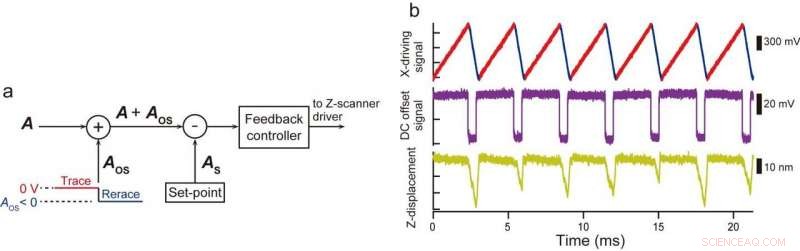
(a) Durante la scansione di ritraccia, un segnale di offset CC ( UN os <0) viene aggiunto al segnale di ampiezza ( UN ). Il controllo di feedback funziona come se la sonda fosse in forte contatto con il campione, e quindi lo stadio di campionamento viene allontanato dalla punta. (b) Segnale di guida per X-scanner in modalità OTI (in alto), Segnale di offset CC aggiunto al segnale di ampiezza reale (al centro), e spostamento dello scanner Z (in basso). Credito:Università di Kanazawa
Sulla base delle loro intuizioni sulla fisica dei processi di tracciamento e ritracciamento, Fukuda e Ando hanno sviluppato un regime di imaging che aggira il ritracciamento. Questo deve quindi essere adeguatamente considerato nell'algoritmo di controllo. I ricercatori hanno testato la loro modalità di imaging a sola traccia su campioni di filamenti di actina. (L'actina è una proteina molto comune nelle cellule.) L'imaging non era solo più veloce, ma anche meno invasivo:i filamenti si rompevano molto meno frequentemente. Hanno anche registrato processi di polimerizzazione (attraverso interazioni proteina-proteina); ancora, il metodo è risultato essere più veloce e meno fastidioso rispetto all'operazione di tracciamento-ritracciamento AFM standard.
Gli scienziati sono fiduciosi che il loro "metodo semplice e altamente efficace sarà presto installato nei sistemi HS-AFM esistenti e futuri, e migliorerà una vasta gamma di studi di imaging HS-AFM in biofisica e in altri campi".