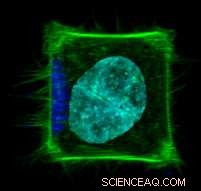
Cella contenente nanoparticelle magnetiche. Una cellula modellata per aderire alla forma di un quadrato con nanoparticelle localizzate (blu scuro) che causano la generazione locale di filopodi ricchi di actina (verde). Viene mostrato anche il nucleo (ciano). La dimensione della cella è di ~ 30 micrometri.
(Phys.org)—Utilizzando grappoli di minuscole particelle magnetiche di circa 1, 000 volte più piccolo della larghezza di un capello umano, ricercatori della UCLA Henry Samueli School of Engineering and Applied Science hanno dimostrato di poter manipolare il modo in cui migliaia di cellule si dividono, trasformarsi e sviluppare estensioni simili a dita.
Questo nuovo strumento potrebbe essere utilizzato nella biologia dello sviluppo per capire come si sviluppano i tessuti, o nella ricerca sul cancro per scoprire come le cellule tumorali si muovono e invadono i tessuti circostanti, hanno detto i ricercatori.
I risultati del team dell'UCLA sono stati pubblicati online il 14 ottobre sulla rivista Metodi della natura .
Una cellula può essere considerata una complessa macchina biologica che riceve un assortimento di "input" e produce specifici "output, "come la crescita, movimento, divisione o la produzione di molecole. Al di là del tipo di input, le celle sono estremamente sensibili alla posizione di un input, in parte perché le cellule eseguono "multiplexing spaziale, " riutilizzare gli stessi segnali biochimici di base per funzioni diverse in luoghi diversi all'interno della cellula.
Comprendere questa localizzazione dei segnali è particolarmente difficile perché gli scienziati non dispongono di strumenti con una risoluzione e un controllo sufficienti per funzionare all'interno dell'ambiente in miniatura di una cellula. E qualsiasi strumento utilizzabile dovrebbe essere in grado di perturbare molte cellule con caratteristiche simili contemporaneamente per ottenere un'accurata distribuzione delle risposte, poiché le risposte delle singole cellule possono variare.
Per affrontare questo problema, un team interdisciplinare UCLA che includeva il professore associato di bioingegneria Dino Di Carlo, lo studioso postdottorato Peter Tseng e il professore di ingegneria elettrica Jack Judy hanno sviluppato una piattaforma per manipolare con precisione le nanoparticelle magnetiche all'interno di cellule di forma uniforme. Queste nanoparticelle hanno prodotto un segnale meccanico locale e hanno prodotto risposte distinte dalle cellule.
Determinando le risposte di migliaia di singole cellule con la stessa forma a stimoli locali indotti da nanoparticelle, i ricercatori sono stati in grado di eseguire una media automatizzata della risposta delle cellule.
Per realizzare questa piattaforma, il team ha dovuto prima superare la sfida di spostare particelle così piccole (ognuna misura 100 nanometri) attraverso l'interno viscoso di una cellula una volta che le cellule le hanno inghiottite. Utilizzando tecnologie ferromagnetiche, che consentono ai materiali magnetici di accendersi e spegnersi, " il team ha sviluppato un approccio per incorporare una griglia di piccoli blocchi ferromagnetici all'interno di un vetrino microfabbricato e per posizionare con precisione le singole cellule in prossimità di questi blocchi con uno schema di proteine che aderiscono alle cellule.
Quando un campo magnetico esterno viene applicato a questo sistema, i blocchi ferromagnetici sono "accesi" e possono quindi trascinare le nanoparticelle all'interno delle cellule in direzioni specifiche e allinearle uniformemente. I ricercatori potrebbero quindi modellare e controllare le forze in migliaia di cellule contemporaneamente.
Utilizzando questa piattaforma, il team ha mostrato che le cellule hanno risposto a questa forza locale in diversi modi, anche nel modo in cui si sono divisi. Quando le cellule passano attraverso il processo di replicazione per creare due cellule, l'asse di divisione dipende dalla forma della cellula e dai punti di ancoraggio con cui la cellula si aggrappa alla superficie. I ricercatori hanno scoperto che la forza indotta dalle nanoparticelle potrebbe cambiare l'asse di divisione cellulare in modo tale che le cellule si dividano invece lungo la direzione della forza.
I ricercatori hanno affermato che questa sensibilità alla forza potrebbe far luce sull'intricata formazione e stiramento dei tessuti durante lo sviluppo embrionale. Oltre a dirigere l'asse di divisione, hanno scoperto che la forza locale indotta dalle nanoparticelle ha portato anche all'attivazione di un programma biologico in cui le cellule generano filopodi, che sono simili a dita, estensioni ricche di actina che le cellule usano spesso per trovare siti a cui aderire e che aiutano nel movimento.
Di Carlo, il ricercatore principale della ricerca, prevede che la tecnica possa essere applicata oltre il controllo degli stimoli meccanici nelle cellule.
"Le nanoparticelle possono essere rivestite con una varietà di molecole importanti nella segnalazione cellulare, " ha detto. "Ora dovremmo avere uno strumento per indagare quantitativamente come la posizione precisa delle molecole in una cellula produce un comportamento specifico. Questo è un pezzo chiave mancante nel nostro set di strumenti per comprendere i programmi cellulari e per consentire alle cellule di eseguire funzioni utili".