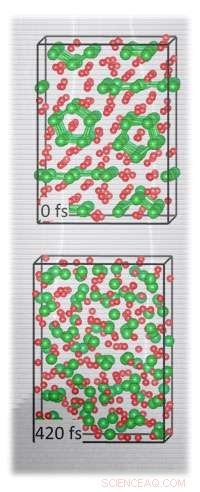
Simulazioni ed esperimenti molecolari mostrano la struttura iniziale della lega litio-silicio e l'amorfizzazione che avviene dopo 420 femtosecondi. Gli ioni di litio sono le sfere rosse e gli atomi di silicio sono le sfere verdi.
(Phys.org) — Onnipresente ma frustrante, le batterie agli ioni di litio si sbiadiscono perché i materiali perdono la loro struttura in risposta alla carica e alla scarica. Questo cambiamento strutturale è strettamente correlato alla formazione di regioni ricche di elettroni all'interno dell'elettrodo, secondo gli scienziati del Pacific Northwest National Laboratory (PNNL), l'Università di Scienze e Tecnologie Elettroniche della Cina, Università nordoccidentale, e Rensselaer Polytechnic Institute. Il team ha utilizzato esperimenti e simulazioni molecolari per dimostrare che la regione ricca di elettroni provoca la rottura dei legami di silicio. La rottura del legame trasforma il silicio cristallino in una lega amorfa di litio e silicio.
"Non era assolutamente chiaro cosa stesse succedendo, sebbene molti articoli descrivano come l'inserimento di ioni di litio nei materiali porti all'amorfizzazione, " ha detto il dottor Fei Gao, un fisico chimico e un corrispondente autore dello studio. "Proponiamo che le condizioni locali ricche di elettroni inducano l'amorfizzazione".
Come ogni proprietario di un telefono cellulare sa, le batterie agli ioni di litio si sbiadiscono, immagazzinando meno energia ogni volta che vengono caricati. Col tempo, una batteria si deteriora al punto da dover essere sostituita, a un costo ambientale e finanziario. Questo studio spiega ciò che è stato visto più volte negli esperimenti:far funzionare le batterie con il silicio, ossido di zinco, germanio, o certi altri materiali isolanti portano ad elettrodi amorfizzati, ma l'alluminio o altri metalli rimangono una lega cristallina. I risultati di questo studio potrebbero aiutare nella progettazione di materiali più durevoli non solo per i telefoni cellulari, ma anche per auto elettriche.
"La domanda energetica sempre crescente di informazioni e trasporti si basa sul progresso delle tecniche di stoccaggio dell'energia, come le batterie agli ioni di litio a causa della loro densità di energia relativamente elevata e flessibilità di progettazione. Lo sviluppo tempestivo di una batteria migliore è la forza trainante per la creazione di nuovi materiali per lo stoccaggio di energia, " ha detto il dottor Chongmin Wang, esperto di imaging chimico al PNNL e investigatore di questo studio.
Quando si carica una batteria agli ioni di litio, gli ioni di litio sono inseriti nell'anodo, un processo noto come litiazione. Gli ioni dell'anodo iniziano per essere disposti in un reticolo ben definito, ma in certi casi si trasformano in un guazzabuglio amorfo. In questo studio, gli scienziati hanno utilizzato anodi di nanofili di silicio drogato con fosforo. I nanofili sono stati coltivati presso il Centro per le nanotecnologie integrate del DOE, al Los Alamos National Laboratory e alla Northwestern University, utilizzando la deposizione chimica da vapore.
Il team ha portato i nanofili all'EMSL del DOE, situato al PNNL, e li ha assemblati in una minuscola batteria all'interno di un microscopio elettronico a trasmissione corretto per l'aberrazione e litiazione osservata, a risoluzione reticolare. Hanno inoltre osservato il comportamento di queste regioni con immagini di microscopia elettronica a trasmissione a scansione e mappe di spettroscopia a perdita di energia degli elettroni. Per completare le osservazioni sperimentali, hanno studiato gli elettrodi a base di metallo utilizzando un metodo di dinamica molecolare della teoria del funzionale della densità su larga scala e hanno visto la forma dei cristalli. Il team ha anche esaminato le reazioni che producono siliciuro di litio cristallino in condizioni ricche di elettroni.
Hanno scoperto che l'amorfizzazione inizia sempre alle interfacce tra il silicio e una lega litio-silicio dove si verifica un'elevata concentrazione localizzata di elettroni. Per adattarsi agli elettroni extra e ad un alto livello di ioni di litio che entrano nel reticolo, i legami tra gli atomi di silicio nel reticolo cristallino si rompono. I legami spezzati creano atomi di silicio isolati e portano alle fasi disordinate.
"L'esperienza sia sulle batterie agli ioni di litio che sull'imaging chimico ci ha dato il vantaggio, " ha detto il dottor Luigi Terminello, che guida la Chemical Imaging Initiative al PNNL, lo sponsor principale di questo studio.
Gli scienziati stanno conducendo simulazioni computazionali per supportare esperimenti volti a comprendere appieno le batterie. Per esempio, continuano ad esplorare il comportamento del grafene, un materiale di grande interesse per l'accumulo di energia. Anche, stanno facendo un lavoro computazionale con gli sperimentatori per chiarire il comportamento degli ioni nei materiali per la batteria ricaricabile agli ioni di litio, in particolare il catodo di ossido di litio nichel manganese.