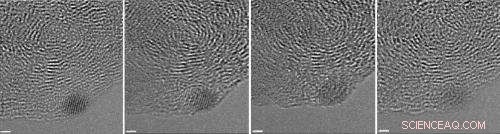
Una serie di immagini mostra un piccolo nanodiamante (la macchia scura nell'angolo in basso a destra) che torna all'antracite. Gli scienziati della Rice University hanno visto la formazione di nanodiamanti nel carbone idrogenato quando colpiti dal fascio di elettroni utilizzato nei microscopi elettronici a trasmissione ad alta risoluzione. Ma diamanti più piccoli come questo si sono degradati con le immagini successive. La barra della scala è di 1 nanometro. Credito:Billups Lab/Rice University
(Phys.org) —Le immagini scattate dagli scienziati della Rice University mostrano che alcuni diamanti non sono per sempre. I ricercatori della Rice dietro un nuovo studio che spiega la creazione di nanodiamanti nel carbone trattato mostrano anche che alcuni diamanti microscopici durano solo pochi secondi prima di svanire di nuovo in forme meno strutturate di carbonio sotto l'impatto di un fascio di elettroni.
La ricerca del chimico della Rice Ed Billups e dei suoi colleghi appare nell'American Chemical Society's Journal of Physical Chemistry Letters .
Billups e Yanqiu Sun, un ex ricercatore post-dottorato nel suo laboratorio, assistito all'effetto interessante mentre lavorava su modi per ridurre chimicamente il carbonio dal carbone antracite e renderlo solubile. Per prima cosa hanno notato la formazione di nanodiamanti in mezzo all'amorfo, strati di grafite infusi di idrogeno.
È successo, Hanno scoperto, quando hanno preso i primi piani del carbone con un microscopio elettronico, che emette un fascio di elettroni nel punto di interesse. inaspettatamente, l'energia immessa ha congelato i cluster di atomi di carbonio idrogenati, alcuni dei quali hanno assunto la struttura reticolare dei nanodiamanti.
"Il raggio è molto potente, "Ha detto Billups. "Per far cadere gli atomi di idrogeno da qualcosa ci vuole un'enorme quantità di energia".

Le macchie scure in queste immagini sono nanodiamanti formati nel carbone antracite idrogenato quando vengono colpiti dai raggi di un microscopio elettronico, secondo i ricercatori della Rice University. Credito:Billups Lab/Rice University
Anche senza il tipo di pressione necessaria per produrre diamanti su macroscala, l'energia ha fatto cadere gli atomi di idrogeno per provocare una reazione a catena tra gli strati di grafite nel carbone che ha prodotto diamanti larghi tra 2 e 10 nanometri.
Ma il più "nano" dei nanodiamanti è stato visto svanire sotto la potenza del fascio di elettroni in una successione di immagini riprese nell'arco di 30 secondi.
"I piccoli diamanti non sono stabili e ritornano al materiale di partenza, l'antracite, "Ha detto Billups.
Billups si è rivolto al fisico teorico della Rice Boris Yakobson e ai suoi colleghi dell'Istituto tecnologico per i materiali superhard e nuovi in carbonio di Mosca per spiegare cosa hanno visto i chimici. Yakobson, Pavel Sorokin e Alexander Kvashnin avevano già elaborato un grafico, chiamato diagramma di fase, che dimostrava come si potevano realizzare sottili film di diamante senza una pressione massiccia.
Hanno usato calcoli simili per mostrare come i nanodiamanti potrebbero formarsi nell'antracite trattata e nel carbone subbituminoso. In questo caso, il raggio del microscopio elettronico fa cadere gli atomi di idrogeno dagli strati di carbonio. Quindi i legami penzolanti compensano collegandosi a uno strato di carbonio adiacente, che viene richiesto di connettersi al livello successivo. La reazione comprime gli atomi in una matrice caratteristica del diamante fino a quando la pressione costringe il processo a fermarsi.
Naturale, i diamanti su macroscala richiedono pressioni e temperature estreme per formarsi, ma il diagramma di fase dovrebbe essere riconsiderato per i nanodiamanti, hanno detto i ricercatori.
"Esiste una finestra di stabilità per i diamanti nell'intervallo 19-52 angstrom (decimi di nanometro), oltre la quale la grafite è più stabile, "Ha detto Billups. Nell'antracite idrogenata si possono formare nanodiamanti stabili di dimensioni fino a 20 nanometri, hanno trovato, sebbene i nanodiamanti più piccoli fossero instabili sotto la continua radiazione del fascio di elettroni.
Billups ha notato che successivi esperimenti con fasci di elettroni con antracite incontaminata non formavano diamanti, mentre i test con infusioni di idrogeno meno robuste hanno portato a regioni con "frange simili a cipolla" di carbonio grafitico, ma nessun diamante completamente formato. Entrambi gli esperimenti hanno sostenuto la necessità di una quantità sufficiente di idrogeno per formare nanodiamanti.
Kvashnin è un ex studente in visita alla Rice e uno studente laureato presso l'Istituto di fisica e tecnologia di Mosca (MIPT). Sorokin ricopre incarichi al MIPT e alla National University of Science and Technology, Mosca. Yakobson è Karl F. Hasselmann Professore di Rice di ingegneria meccanica e scienza dei materiali, un professore di chimica e membro del Richard E. Smalley Institute for Nanoscale Science and Technology. Billups è professore di chimica alla Rice.