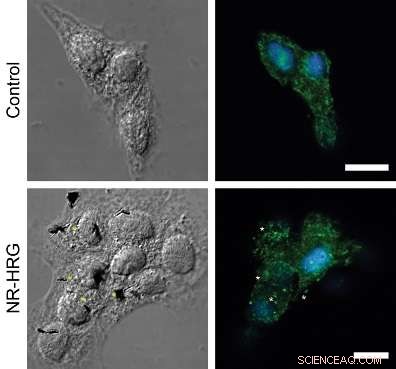
Figura:cluster del recettore ErbB2 dopo il legame di HRG-nanorod alle cellule MCF7. Micrografie confocali che mostrano una sezione dorsale di cellule MCF7 mirate (pannello inferiore) e non mirate (pannello superiore). I recettori ErbB2 (verde) sono stati immunocolorati senza permeabilizzare la membrana plasmatica. I nuclei sono stati colorati con Hoechst 33342 (blu). Le stelle indicano esempi di cluster di recettori ErbB2 che si trovano in prossimità di nanorod.
I ricercatori dell'UCD hanno manipolato con successo le nanoparticelle per colpire due linee cellulari di cancro al seno umano come strumento nella diagnosi e nel trattamento del cancro.
Il rivestimento di nanoparticelle con diverse sostanze consente di regolare in modo particolare la loro interazione con le cellule. Per esempio, l'utilizzo di una particella otticamente attiva come l'oro (Au) fornirà un eccellente contrasto nell'imaging nel vicino infrarosso (NIR) e, se riscaldato, può effettivamente distruggere il tessuto circostante. Questa è chiamata terapia di ablazione fototermica. Le particelle magneticamente attive come il ferro (Fe) possono consentire terapie fisiche generando calore quando esposte a campi magnetici alternati che causano la morte cellulare (ipertermia magnetica).
Il team dell'UCD guidato da Conway Fellows, Il professor Gil Lee alla School of Chemistry and Chemical Biology e il professor Walter Kolch alla Systems Biology Ireland, nanotubi sintetizzati con un lungo segmento di ferro rivestito con glicole polietilenico e una punta corta in oro rivestita con un singolo strato della proteina, eregulina (HRG).
HRG è un fattore di crescita che si lega e attiva la famiglia di recettori proteici ErbB. ErbB2 è sovraespresso in alcuni tumori al seno ed è collegato a una prognosi infausta. Però, La sovraespressione di ErbB2 porta a una maggiore sensibilità a determinati farmaci. Il team ritiene che nanobarre funzionalizzate Fe-Au utilizzate in combinazione con questi farmaci potrebbero essere utili nel trattamento del cancro.
Dopo aver caratterizzato e messo a punto l'interazione dei nanotubi con le cellule, il team di ricerca ha valutato come le cellule rispondono alla stimolazione meccanica. Per fare questo, hanno integrato una pinzetta elettromagnetica con un microscopio ottico e hanno utilizzato un nuovo chip microfluidico per monitorare l'interazione di singole nanobarre con due linee cellulari di cancro al seno umano che esprimono la famiglia di recettori ErbB a velocità diverse. Quando i nanorodi HRG si legano alle cellule tumorali che esprimono ErbB, danno il via a una cascata di eventi di segnalazione che portano alla morte cellulare.
"Usando pinzette magnetiche per allungare le cellule, siamo stati in grado di attivare ulteriormente le vie di segnalazione cellulare per innescare la morte cellulare. Questo è stato ancora più efficace nel causare la morte delle cellule tumorali rispetto all'ipertermia magnetica, l'altro approccio terapeutico che abbiamo valutato", ha spiegato il dottor Devrim Kilinc, primo autore e ricercatore nel gruppo Lee.
"I risultati sono un'indicazione positiva per il targeting su nanoscala e la manipolazione localizzata delle cellule tumorali con un profilo recettore specifico".