Credito:Wiley
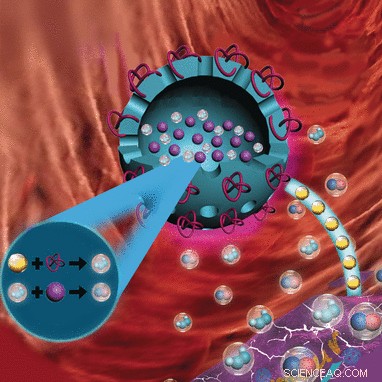
Nanocapsule biocompatibili, caricato con un amminoacido e dotato di un enzima, ora combina due strategie antitumorali in un concetto di trattamento sinergico. I ricercatori sperano che questo aumenti l'efficacia e riduca gli effetti collaterali. Nel diario Angewandte Chemie , gli scienziati spiegano il concetto:le cellule tumorali vengono private del loro nutriente glucosio poiché questo viene convertito in monossido di azoto tossico (NO) e perossido di idrogeno (H2O2).
NO è un gas tossico che provoca smog. Però, a basse concentrazioni nel corpo è un'importante molecola messaggera che regola cose come la circolazione e la libido. È anche un'importante arma di difesa fisiologica contro funghi e batteri. A concentrazioni più elevate, L'NO è in grado di uccidere le cellule tumorali e aumentare l'efficacia dei trattamenti fotodinamici e radiologici. Per uso clinico, NO deve essere rilasciato nell'area bersaglio da un precursore biocompatibile.
L'amminoacido naturale L-arginina (L-Arg) può essere utile in un tale sistema, perché l'enzima nativo NO sintasi inducibile (iNOS) produce NO da L-Arg. NO si forma anche quando L-Arg viene ossidato da H2O2. Questo è interessante perché il microambiente intorno ai tumori è ricco di H2O2. Questo approccio alla terapia con gas NO è perseguito dai ricercatori dell'Università di Shenzhen (Cina), gli Istituti Nazionali di Sanità (Bethesda, STATI UNITI D'AMERICA), e l'Università del Maryland (College Park, STATI UNITI D'AMERICA). La loro svolta speciale è quella di combinare questa terapia del gas con un metodo per far morire di fame le cellule tumorali in un trattamento sinergico.
Invece di far morire di fame un tumore bloccando i vasi sanguigni che lo alimentano, i ricercatori intendono rimuovere il glucosio di cui il tumore ha bisogno per nutrirsi consumandolo in una reazione metabolica:l'enzima glucosio ossidasi (GOx) converte il glucosio in acido gluconico e H2O2. L'aumento della concentrazione di H2O2 è un utile effetto collaterale, perché H2O2 è sia citotossico che accelera il rilascio di NO da L-Arg. Un altro effetto collaterale utile è che H2O2 e NO reagiscono per formare perossinitriti altamente tossici che danneggiano le cellule tumorali.
Il gruppo di ricerca guidato da Peng Huang, Tianfu Wang, e Xiaoyuan Chen ha ora raggiunto un'importante pietra miliare nello sviluppo di questo concetto. Hanno sviluppato biocompatibilità, biodegradabile, nanocapsule porose costituite da organosilicati che trasportano simultaneamente GOx e L-Arg nelle cellule tumorali. GOx è legato alla superficie; L-Arg è immagazzinato all'interno della capsula. Mentre il GOx è attivo subito dopo l'iniezione delle nanocapsule nel tumore, L-Arg viene rilasciato a poco a poco, prima attraverso i pori della capsula, poi come la capsula si disintegra. La loro ampia cavità consente inoltre alle capsule di fungere da materiale di contrasto ad ultrasuoni per una migliore localizzazione del tumore.
Esperimenti sia con colture cellulari che con topi hanno dimostrato il significativo effetto sinergico di questa terapia combinata, che inibisce con successo la crescita cellulare, avvia la morte cellulare, e riduce i tumori nei topi.