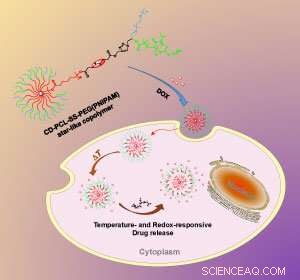
Il cambiamento di temperatura e ambiente chimico all'interno della cellula fa sì che la nanoparticella rilasci il suo carico utile di farmaco. Credito:The Royal Society of Chemistry
I ricercatori di A*STAR hanno sviluppato particelle di somministrazione di farmaci su scala nanometrica in grado di rilevare l'ambiente circostante, e rilasciano il loro carico utile solo dopo essere entrati in una cella, una scoperta che potrebbe rendere più efficaci molti farmaci esistenti.
Le nuove nanoparticelle, sviluppato da Zibiao Li dell'A*STAR Institute of Materials Research and Engineering e dai suoi collaboratori, rappresentano un aggiornamento significativo rispetto alle generazioni precedenti di nanoparticelle per la somministrazione di farmaci a base di polimeri. I primi esempi consistevano tipicamente in semplici catene polimeriche con un polo polare, testa idrofila e una non polare, coda idrofoba. In acqua, queste catene si aggregano naturalmente in sfere, con le loro code idrofobe tutte rivolte verso l'interno per formare un nucleo non polare. Il nucleo ha formato un buon sito per l'annidamento delle molecole di farmaci. Nel flusso sanguigno, però, questi aggregati tendono a essere lacerati.
Li e i suoi colleghi hanno utilizzato le più recenti tecniche di sintesi dei polimeri per creare nanoparticelle a singola molecola. Piuttosto che un aggregato autoassemblato di polimeri separati, il team ha sintetizzato una struttura più robusta in cui le catene polimeriche erano fortemente legate in modo covalente a un nucleo centrale. La sintesi è iniziata con la beta-ciclodestrina, una molecola di zucchero circolare con 21 gruppi ossidrilici sulla sua superficie. I gruppi idrossilici hanno formato gli ancoraggi chimici da cui il team ha costruito il multiplo lungo, a forma di Y, bracci multifunzionali in polimero.
"La sfida più grande nel realizzare la [nanoparticella] è stata quella di integrare diverse metodologie sintetiche in un unico progetto macromolecolare, " dice Li. Ad una delle estremità di ogni ramo a forma di Y, il team ha attaccato un polimero sensibile alla temperatura chiamato PNIPAM. A temperatura ambiente il polimero PNIPAM si estende verso l'esterno, ma crolla una volta che la temperatura corporea, 37 gradi Celsius, è raggiunto, permettendo al carico di molecole di farmaco della nanoparticella di fuoriuscire.
A metà di ogni braccio in polimero, il team ha installato un legame zolfo-zolfo. Quando le particelle entrano in una cellula, soddisfano alti livelli di glutatione, una molecola che scinde i legami zolfo-zolfo. Così il rivestimento polimerico esterno della nanoparticella viene tagliato via, e il farmaco viene rilasciato ancora più velocemente.
Quando il team ha testato questo effetto con un farmaco antitumorale chiamato doxorubicina, l'effetto a doppia azione era chiaro. "Il passaggio dalla temperatura ambiente alla temperatura corporea, e l'effetto del glutatione, ha mostrato un rilascio sinergico e rapido del farmaco, " dice Li. A temperature più basse, o in assenza di glutatione, il rilascio del farmaco è stato significativamente più lento, lui dice.
"Il prossimo piano è quello di integrare nuove funzionalità, per il rilascio di precisione del farmaco per la terapia mirata del cancro, " dice Li. Un'estremità di ogni ramo a forma di Y potrebbe essere funzionalizzata con una molecola che si attacca selettivamente alle cellule tumorali, consegnare il farmaco esattamente dove è necessario.