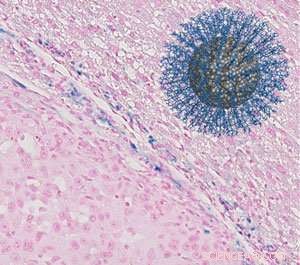
Le nanoparticelle magneticamente attive rivestite di peptidi sviluppate per la risonanza magnetica con mezzo di contrasto rilevano un tumore al fegato. Credito:American Chemical Society.
Il cancro diventerà più facile da rilevare e diagnosticare precocemente utilizzando la risonanza magnetica (MRI) grazie ai ricercatori A*STAR che hanno progettato agenti di contrasto di nanoparticelle di ossido di ferro biocompatibili¹.
Mentre i composti a base di gadolinio si sono dimostrati efficaci come agenti di contrasto per migliorare il rapporto segnale-rumore durante la risonanza magnetica, possono causare effetti collaterali come la fibrosi sistemica nefrogenica che può colpire pazienti con ridotta funzionalità renale. Le nanoparticelle di ossido di ferro sono emerse come alternative a basso rischio. In ambienti biologici complessi, però, queste nanoparticelle tendono a degradarsi, aggregato, e aderiscono ad altre sostanze, che riduce la loro attività magnetica.
Per mitigare questo problema, un team guidato da David Paramelle, dall'A*STAR Institute of Materials Research and Engineering, ha sviluppato rivestimenti peptidici che prevengono la decomposizione e l'aggregazione delle nanoparticelle, facilitando nel contempo la biocompatibilità. Questi rivestimenti sono cruciali per la transizione degli agenti di contrasto a base di ossido di ferro all'uso clinico.
Basandosi sulla loro vasta esperienza di nanoparticelle d'argento e d'oro rivestite di peptidi, i ricercatori hanno creato una libreria di brevi peptidi e hanno depositato questi composti sulle nanoparticelle di ossido di ferro per produrre vari film a strato singolo. Hanno anche sintetizzato ligandi analoghi per colmare qualsiasi spazio tra i peptidi sulla superficie delle nanoparticelle e generare rivestimenti misti.
Ogni peptide comprendeva uno stelo collegato a un "piede" e una "testa" a ciascuna estremità. Mentre il piede ancorava il peptide alle nanoparticelle, la testina alcol-funzionalizzata ha stabilizzato le nanoparticelle e bloccato le interazioni indesiderate con l'ambiente.
"La parte difficile era trovare un piede con un'elevata forza di legame, "Paramelle ha spiegato, perché, le nanoparticelle di ossido di ferro hanno presentato una chimica diversa nonostante la loro geometria e dimensione sferica simili alle nanoparticelle d'oro e d'argento."
"Per progettare i peptidi, dovevamo tornare al tavolo da disegno, "dice Paramelle, rilevando che passando dai metalli nobili, che si legano preferenzialmente alle molecole contenenti zolfo, all'ossido di ferro ha ampliato la gamma di gruppi funzionali che fungono da piede per includere fosfati e acidi carbossilici.
Attraverso test sempre più rigorosi, i ricercatori hanno valutato la capacità di ciascun film di stabilizzare le nanoparticelle in condizioni biologiche mantenendo le loro proprietà magnetiche. Hanno scoperto che i peptidi e i ligandi che portano due gruppi fosfato al piede si comportano meglio in presenza di cellule tumorali del fegato. Le nanoparticelle rivestite di peptidi hanno superato gli agenti di contrasto disponibili in commercio senza distruggere le cellule in vitro, e ha fortemente migliorato il contrasto tra tessuto tumorale e sano durante la risonanza magnetica in vivo quando iniettato in topi con cancro al fegato.
Il team di Paramelle sta studiando modi per ampliare l'applicazione del loro sistema ad altri tumori, soprattutto il cancro al seno. "Abbiamo in programma di funzionalizzare le nanoparticelle con anticorpi e controllare il numero di questi anticorpi sulla superficie delle nanoparticelle, " lui dice.