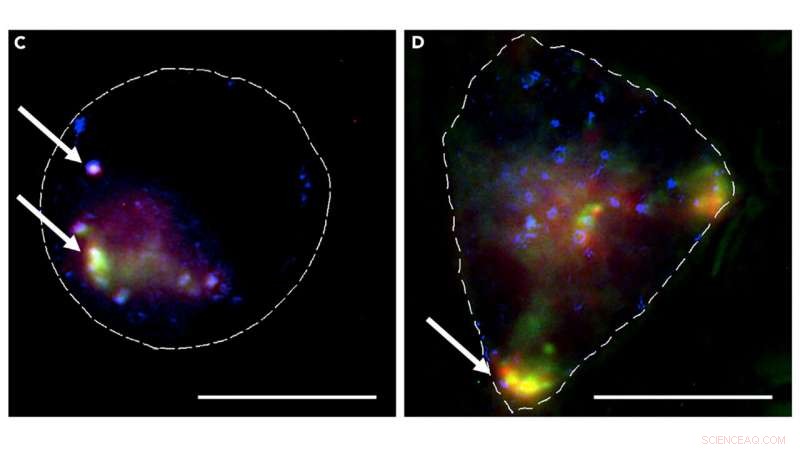
Cellule con MOF che trasportano siRNA. Credito:Università di Cambridge
Scienziati dell'Università di Cambridge hanno sviluppato una piattaforma che utilizza nanoparticelle note come strutture metallo-organiche per fornire un promettente agente antitumorale alle cellule.
Ricerca guidata dal Dr. David Fairen-Jimenez, dal Dipartimento di Ingegneria Chimica e Biotecnologia di Cambridge, indica che le strutture metallo-organiche (MOF) potrebbero rappresentare una piattaforma praticabile per fornire un potente agente antitumorale, noto come siRNA, alle cellule.
Piccolo acido ribonucleico interferente (siRNA), ha il potenziale per inibire i geni che causano il cancro sovraespressi, ed è diventato un obiettivo crescente per gli scienziati alla ricerca di nuovi trattamenti contro il cancro.
Il gruppo di Fairen-Jimenez ha utilizzato simulazioni computazionali per trovare un MOF con la dimensione dei pori perfetta per trasportare una molecola di siRNA, e che si romperebbe una volta dentro una cella, rilasciando il siRNA al suo bersaglio. I loro risultati sono stati pubblicati oggi sulla rivista Cell Press, chimica .
Alcuni tumori possono verificarsi quando geni specifici all'interno delle cellule causano una produzione eccessiva di particolari proteine. Un modo per affrontare questo problema è bloccare il percorso di espressione genica, limitando la produzione di queste proteine.
Le molecole di siRNA possono fare proprio questo:legarsi a specifiche molecole messaggere di geni e distruggerle prima che possano dire alla cellula di produrre una particolare proteina. Questo processo è noto come "atterramento genetico". Gli scienziati hanno iniziato a concentrarsi maggiormente sugli siRNA come potenziali terapie contro il cancro nell'ultimo decennio, poiché offrono una soluzione versatile per il trattamento delle malattie:tutto ciò che devi sapere è la sequenza del gene che vuoi inibire e puoi creare il siRNA corrispondente che lo scompone. Invece di progettare, sintetizzando e testando nuovi farmaci, un processo incredibilmente lungo e costoso, è possibile apportare alcune semplici modifiche alla molecola di siRNA e trattare una malattia completamente diversa.
Uno dei problemi con l'utilizzo di siRNA per curare le malattie è che le molecole sono molto instabili e spesso vengono scomposte dai meccanismi di difesa naturali della cellula prima che possano raggiungere i loro obiettivi. Le molecole di siRNA possono essere modificate per renderle più stabili, ma questo compromette la loro capacità di abbattere i geni bersaglio. È anche difficile portare le molecole nelle cellule:devono essere trasportate da un altro veicolo che funge da agente di consegna.

Struttura cristallina metallo-organica. Credito:David Fairen-Jimenez
I ricercatori di Cambridge hanno utilizzato una speciale nanoparticella per proteggere e fornire siRNA alle cellule, dove mostrano la sua capacità di inibire uno specifico gene bersaglio.
Fairen-Jimenez guida la ricerca sui materiali avanzati, con un focus particolare sui MOF:composti 3-D autoassemblanti costituiti da blocchi metallici e organici collegati tra loro.
Esistono migliaia di diversi tipi di MOF che i ricercatori possono realizzare:attualmente ce ne sono più di 84, 000 strutture MOF nel database strutturale di Cambridge con 1000 nuove strutture pubblicate ogni mese e le loro proprietà possono essere regolate per scopi specifici. Modificando diversi componenti della struttura MOF, i ricercatori possono creare MOF con diverse dimensioni dei pori, stabilità e tossicità, consentendo loro di progettare strutture in grado di trasportare molecole come i siRNA nelle cellule senza effetti collaterali dannosi.
"Con la terapia anticancro tradizionale se stai progettando nuovi farmaci per curare il sistema, questi possono avere comportamenti diversi, geometrie, dimensioni, e quindi avresti bisogno di un MOF ottimale per ciascuno di questi singoli farmaci, " dice Fairen-Jimenez. "Ma per siRNA, una volta sviluppato un MOF utile, in linea di principio puoi usarlo per una gamma di diverse sequenze di siRNA, curare diverse malattie».
"Le persone che l'hanno fatto prima hanno usato MOF che non hanno una porosità abbastanza grande da incapsulare il siRNA, quindi molto probabilmente è solo bloccato all'esterno, "dice Michelle Teplensky, ex dottorato di ricerca studente nel gruppo di Fairen-Jimenez, che ha svolto la ricerca. "Abbiamo usato un MOF in grado di incapsulare il siRNA e quando è incapsulato offri una protezione maggiore. Il MOF che abbiamo scelto è costituito da un nodo metallico a base di zirconio e abbiamo fatto molti studi che mostrano che lo zirconio è abbastanza inerte e non funziona. t causare problemi di tossicità."
L'utilizzo di un MOF biodegradabile per la consegna di siRNA è importante per evitare l'accumulo indesiderato delle strutture una volta che hanno svolto il loro lavoro. Il MOF selezionato da Teplensky e dal team si scompone in componenti innocui che possono essere facilmente riciclati dalla cellula senza effetti collaterali dannosi. La grande dimensione dei pori significa anche che il team può caricare una quantità significativa di siRNA in una singola molecola MOF, mantenendo molto basso il dosaggio necessario per abbattere i geni.
"Uno dei vantaggi dell'utilizzo di un MOF con pori così grandi è che possiamo ottenere un risultato molto più localizzato, dose maggiore di quella richiesta da altri sistemi, " dice Teplensky. "SiRNA è molto potente, non è necessaria una quantità enorme per ottenere una buona funzionalità. La dose necessaria è inferiore al 5% della porosità del MOF."
Un problema con l'utilizzo di MOF o altri veicoli per trasportare piccole molecole nelle cellule è che spesso vengono fermate dalle cellule sulla strada per il loro obiettivo. Questo processo è noto come intrappolamento endosomiale ed è essenzialmente un meccanismo di difesa contro componenti indesiderati che entrano nella cellula. Il team di Fairen-Jimenez ha aggiunto componenti extra al proprio MOF per evitare che rimangano intrappolati mentre entrano nella cella, e con questo, potrebbe garantire che il siRNA raggiunga il suo obiettivo.
Il team ha usato il loro sistema per abbattere un gene che produce proteine fluorescenti nella cellula, quindi sono stati in grado di utilizzare metodi di imaging al microscopio per misurare come la fluorescenza emessa dalle proteine rispetto tra le cellule non trattate con il MOF e quelle che lo erano. Il gruppo si è avvalso delle competenze interne, collaborando con i professori Clemens Kaminski e Gabi Kaminski-Schierle, specialisti di microscopia a super risoluzione, che guidano anche la ricerca nel Dipartimento di Ingegneria Chimica e Biotecnologie.
Utilizzando la piattaforma MOF, il team è stato costantemente in grado di prevenire l'espressione genica del 27%, un livello che mostra la promessa per l'utilizzo della tecnica per abbattere i geni del cancro.
Fairen-Jimenez crede che saranno in grado di aumentare l'efficacia del sistema e il prossimo passo sarà applicare la piattaforma ai geni coinvolti nella causa dei cosiddetti tumori difficili da trattare.
"Una delle domande che ci vengono poste spesso è 'perché vuoi utilizzare una struttura metallo-organica per l'assistenza sanitaria?', perché sono coinvolti metalli che potrebbero suonare dannosi per il corpo, " dice Fairen-Jimenez. "Ma ci concentriamo su malattie difficili come i tumori difficili da trattare per i quali non c'è stato alcun miglioramento nel trattamento negli ultimi 20 anni. Abbiamo bisogno di qualcosa che possa offrire una soluzione; solo anni di vita in più saranno i benvenuti".
La versatilità del sistema consentirà al team di utilizzare lo stesso MOF adattato per fornire diverse sequenze di siRNA e mirare a geni diversi. A causa della sua grande dimensione dei pori, il MOF ha anche il potenziale per fornire più farmaci contemporaneamente, aprendo l'opzione della terapia di combinazione.