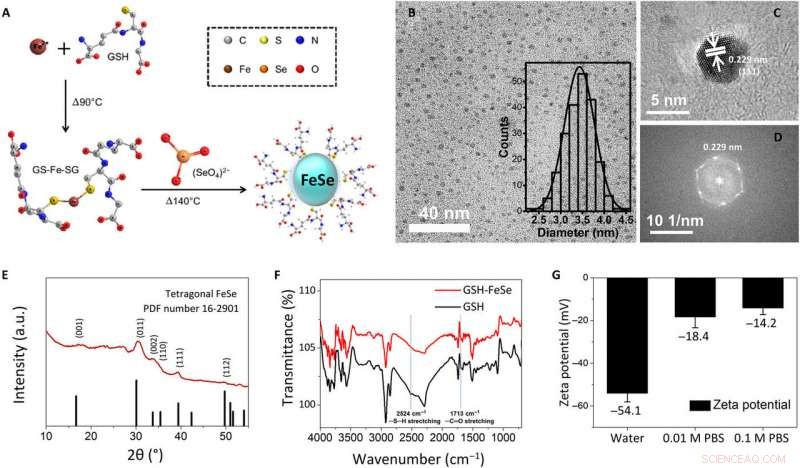
Caratterizzazione fisico-chimica di QD FeSe solubili in acqua sintetizzati in un vaso. (A) Illustrazione schematica della procedura di sintesi one-pot per FeSe QDs GSH-capped, (B) immagine TEM in campo chiaro (riquadro:istogramma della distribuzione delle dimensioni), (C) immagine TEM ad alta risoluzione, (D) trasformata di Fourier veloce dell'immagine TEM ad alta risoluzione, (E) modelli GIXRD, (F) spettri FTIR, e (G) potenziale zeta di FeSe QD. a.u., unità arbitrarie. Credito:progressi scientifici, doi:10.1126/sciadv.aay0044
Sonde fotoluminescenti ad alta biocompatibilità, la resa quantica e le prestazioni di assorbimento multifotone sono di notevole interesse nell'imaging biomedico, dovrebbe ottenere una migliore profondità di penetrazione e risoluzione spaziale. I punti quantici (QD) di seleniuro di ferro (FeSe) soddisfano questi criteri in base a un nuovo rapporto pubblicato in Progressi scientifici da J. Kwon e da un team di ricercatori dei dipartimenti interdisciplinari di Chimica, Scienza dei biomateriali e ingegneria cogno-meccatronica in Corea e Cina. I punti quantici sono cristalli semiconduttori luminescenti su scala nanometrica con proprietà chimiche e fisiche uniche relative alla loro struttura e composizione.
I QD sintetici nel presente studio possono esibire proprietà di eccitazione a due e tre fotoni a lunghezze d'onda di 800 e 1800 nm con un'elevata resa quantica (40%) per l'imaging di seconda finestra. I materiali erano anche biocompatibili e verificati da Kwon et al. quando hanno collegato QD poli(etilenglicole)-coniugato con anticorpi del recettore 2 del fattore di crescita epidermico umano (HER2) per l'imaging a due fotoni in vitro e in vivo. Gli scienziati hanno ripreso con successo le superfici a una profondità fino a 500 µm dalla superficie della pelle utilizzando un laser a femtosecondi non lineare a una lunghezza d'onda di eccitazione di 800 nm. I risultati possono aprire un nuovo percorso per utilizzare QD FeSe biocompatibili per l'imaging di tessuti multifotoni durante la diagnosi della malattia.
I calcogenuri dei metalli di transizione sono attraenti in una vasta gamma di aree di ricerca in nanoscienza con applicazioni come semiconduttori magnetici, superconduttori, fotovoltaico, elettrocatalizzatori, sensori e punti quantici. I materiali stratificati a base di ferro sono promettenti candidati superconduttori con bassa tossicità e costo, con una temperatura di transizione superconduttiva inaspettatamente alta. I materiali di calcogenuro di ferro possono diventare nanosemiconduttori fluorescenti quando le loro dimensioni si riducono a zero. Questi hanno proprietà optoelettroniche uniche rilevanti nell'imaging biologico e nella conversione dell'energia solare. L'imaging biomedico fluorescente con nanocristalli semiconduttori è una tecnica di rilevamento promettente grazie all'elevata fotostabilità e sintonizzabilità dei nanocristalli durante gli spettri di assorbimento ed emissione rispetto ai coloranti organici convenzionali. I QD possono anche esibire fotoluminescenza eccitata da più fotoni (PL) in cui un luminoforo può assorbire contemporaneamente più di due fotoni tramite uno stato virtuale per emettere luce visibile.
Il fenomeno può consentire una maggiore profondità di penetrazione per una ridotta autofluorescenza e dispersione dei tessuti con vantaggi per l'imaging a fluorescenza biomedica in situ durante la chirurgia del cancro. Gli scienziati considerano quindi la microscopia multifotonica (MPM) come un metodo non invasivo, in vivo, strumento di imaging dei tessuti profondi. In questo studio, Kwon et al. sono stati motivati dal lavoro precedente per sintetizzare QD biocompatibili con proprietà luminescenti a due e tre fotoni utilizzando elementi di ferro (Fe) e selenio (Se). Generalmente, i due (precursori di Fe e Se) si trovano naturalmente nel corpo umano e presentano una bassa tossicità in forma di nanoparticelle. Il team di ricerca ha testato la specificità delle cellule tumorali in vitro mirando alla specificità con l'anticorpo monoclonale umanizzato HER2 (recettore del fattore di crescita epidermico umano 2):punti quantici di seleniuro di ferro coniugato (FeSe) (anti-HER2-QD). Per gli esperimenti in vitro, hanno utilizzato un modello di xenotrapianto MCF-7 (Michigan Cancer Foundation) sovraespresso da HER2 (innesti di una diversa specie di donatore) di una linea cellulare di cancro al seno. Hanno quindi condotto l'imaging MPM (microscopia multifotonica) in vivo all'interno di un modello di xenotrapianto dal vivo di tumore al seno umano.
Per sviluppare i QD FeSe solubili in acqua, gli scienziati hanno utilizzato una strategia sintetica a un solo piatto. Hanno formato QD di dimensioni approssimative a 3,4 ± 0,3 nm e li hanno osservati utilizzando la microscopia elettronica a trasmissione in campo chiaro (TEM). Utilizzando TEM ad alta risoluzione e modelli di diffrazione elettronica dei QD, hanno osservato il piano di FeSe tetragonale. Gli scienziati hanno utilizzato l'analisi strutturale con uno spettrometro a diffrazione di raggi X a incidenza radente (GIXRD) e la spettroscopia fotoelettronica a raggi X per dimostrare meticolosamente la morfologia dei FeSe QD. I test del potenziale Zeta hanno mostrato che i QD di FeSe si dissolvono in acqua deionizzata e in soluzione salina 0,01 M e tampone fosfato (PBS) 0,1 M. Quando Kwon et al. li ha monitorati utilizzando una fotocamera digitale e una microscopia a fluorescenza dopo cinque giorni, i QD non si aggregavano o differivano in fluorescenza. Il bandgap dei QD FeSe si è avvicinato a 2,44 eV dallo spettro dall'ultravioletto al visibile (UV-Vis).
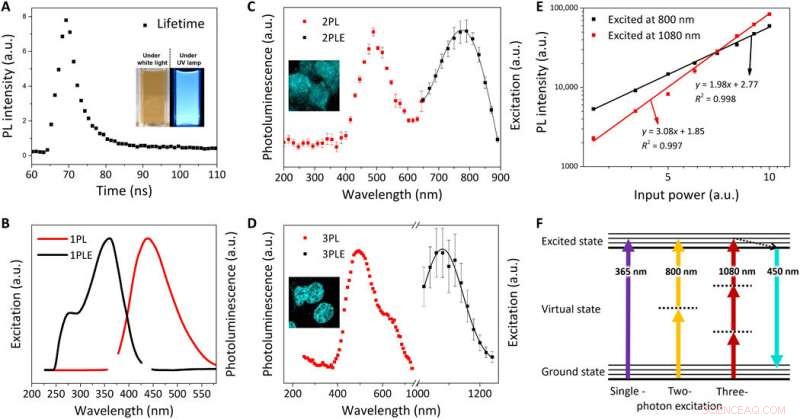
Caratterizzazione ottica di FeSe QD. (A) durata PL (τ) di FeSe QD a una lunghezza d'onda di eccitazione di 380 nm; riquadro:immagini digitali della dispersione di FeSe sotto luce bianca e lampada UV (λex =365 nm). Spettro di eccitazione PL (PLE) normalizzato (linea nera) e spettro PL (linea rossa) a λem di 440 nm e λex di (B) 365 nm per 1PL, (C) 800 nm per 2PL, e (D) 1080 nm per 3PL. (E) Dipendenza dalla potenza dell'intensità PL per 2PL (quadrato nero) e 3PL (quadrato rosso). La pendenza della funzione di dipendenza dalla potenza è 1,98 e 3,08 per 2PL e 3PL, rispettivamente. (F) diagramma di Jablonski di singolo, Due-, e luminescenza a tre fotoni. Credito:progressi scientifici, doi:10.1126/sciadv.aay0044
Kwon et al. ha esplorato le proprietà della fotoluminescenza (PL) dei QD FeSe a 25 gradi C per osservare una durata di 3,23 nanosecondi (ns). Hanno notato un PL eccitato a due fotoni (2PL) e tre fotoni (3PL), seguita da immagini microscopiche rappresentative di fluorescenza di cellule MCF27 colorate con FeSe QD da 2PL e 3PL. Questa proprietà di eccitazione multifotone è notevole per il bioimaging con una lunghezza d'onda più lunga che può penetrare una profondità massima del tessuto con fototossicità ridotta, osservato all'interno della "finestra d'oro" durante l'imaging del tessuto cerebrale.
Il team di ricerca ha prima testato l'influenza del QD sulla vitalità cellulare prima di applicare i QD FeSe agli esperimenti di bioimaging. Hanno usato diverse linee cellulari coltivate con diverse concentrazioni di FeSe QD a varie durate di coltura e hanno osservato un'eccellente vitalità entro sette giorni, con> 75 percento di vitalità cellulare. Utilizzando immagini microscopiche a fluorescenza delle colture cellulari, Kwon et al. ha registrato la biocompatibilità superiore dei QD FeSe, dove i punti quantici non hanno interferito con la crescita cellulare. Per ridurre ulteriormente il legame non specifico durante l'assemblaggio, gli scienziati hanno incapsulato FeSe QD con poli(etilenglicole) (PEG) prima della coniugazione con anticorpi HER2 per sviluppare anti-HER2-PEG-QD.
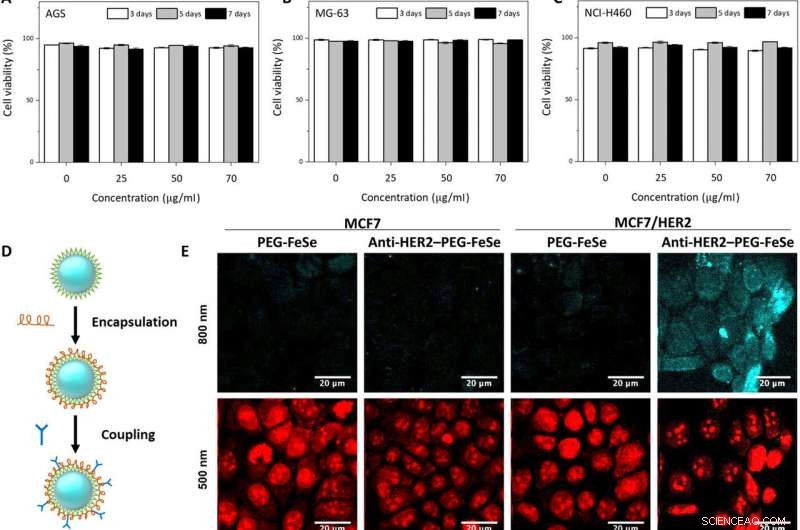
Imaging microscopico a due fotoni in vitro e in vivo di FeSe QD mirati al tumore al seno. valutazione in citometria a flusso della vitalità di (A) AGS, (B) MG-63, e (C) cellule NCI-H460 esposte a QD a varie concentrazioni (0, 25, 50, e 70 μg ml-1) per 3, 5, e 7 giorni. (D) Procedura di coniugazione per preparare anti-HER2–PEG-QD. (E) Imaging microscopico a due fotoni in vitro di cellule MCF7 MCF7 e HER2 sovraespresse (MCF7/HER2) colorate con FeSe QD rivestite con PEG o PEG-QD anti-HER2 coniugato (anti-HER2-PEG-QD, 2 μg ml−1), dove i nuclei sono stati tinti con ioduro di propidio, e la membrana cellulare e i nuclei sono stati ripresi a ex di 800 e 500 nm. Potenza laser =40 mW sul piano focale. (F) Confronto della fotostabilità di QD e rodamina 6G (Rh6G) in acqua deionizzata sotto eccitazione a due fotoni (λex =800 nm, potenza laser =50 mW), dove l'intensità relativa del PL è stata monitorata per 30 min. (G) Fotografia digitale di xenotrapianto di tumore per l'imaging in vivo. (H) Sistema MPM. CH PMT, tubo fotomoltiplicatore a canale; OPO, oscillatore parametrico ottico. (I) Immagini MPM in vivo prima e dopo l'iniezione di anti-HER2-QD e (J) immagini MPM in vivo a diverse profondità focali (da 450 a 500 μm). Barre della scala, 20 micron. Credito:progressi scientifici, doi:10.1126/sciadv.aay0044
Il team ha testato l'assorbimento non specifico e la selettività dei coniugati durante il targeting delle cellule del cancro al seno umano tramite colorazione con ioduro di propidio. Gli anti-HER2-PEG-QD miravano specificamente ai recettori HER2, indicando la possibilità di utilizzare QD PEGilati come agenti di imaging in vivo. Le molecole fisiologicamente stabili hanno mantenuto le loro proprietà ottiche per sette giorni nel siero e in una varietà di soluzioni tampone. I QD FeSe erano altamente fotostabili durante l'eccitazione a due fotoni con proprietà aggiuntive adatte per l'imaging biologico e il monitoraggio a lungo termine delle cellule mirate.
Lo studio ha offerto una nuova prospettiva per la diagnosi del cancro al seno. Il cancro al seno è la seconda causa di morte per cancro per le donne, con tassi di recidiva significativi, dove la chirurgia minimamente invasiva aiutata con tecniche di rilevamento e imaging sono cruciali per identificare la malattia. Il team di ricerca ha stabilito un metodo di imaging MPM (microscopia multifotonica) in vivo con iniezione endovenosa di anti-HER2-PEG-QD in un modello animale di xenotrapianto MCF. Hanno quindi stabilito un modello murino di xenotrapianto sottocutaneo di cancro al seno iniettando cellule MCF7 e cellule MCF/HER2 nel fianco dei topi. Dopo quattro settimane, quando il volume del tumore ha raggiunto i 200 mm 3 , gli scienziati hanno iniettato 100 µl di anti-HER2-PEG-QD e hanno osservato i QD di FeSe come segnale magenta. Hanno quindi ottenuto segnali 2PL a diverse profondità nell'area del tumore a intervalli regolari. Il segnale di seconda generazione armonica (SHG) sembrava blu per rappresentare il collagene nell'area superficiale e gli scienziati hanno distinto il segnale PL dai QD vicino alle cellule del cancro al seno.
In questo modo, J. Kwon e colleghi hanno sintetizzato QD FeSe biocompatibili con una forte vitalità cellulare a concentrazioni QD aumentate. Il team ha utilizzato QD durante l'imaging a fluorescenza a due e tre fotoni e con l'imaging multifotone a una profondità fino a 500 µm per monitorare le cellule tumorali con un laser a femtosecondi non lineare all'interno di animali vivi in vivo. I QD FeSe biocompatibili combinati e l'imaging multifotonico possono aprire un nuovo metodo per realizzare bioimaging in situ non invasivo all'interno di soggetti vivi.
© 2019 Scienza X Rete