
I ricercatori hanno assemblato tre distinte nanostrutture di DNA, tra cui una struttura a forma di C e due a botte, e hanno mostrato al microscopio elettronico a trasmissione che erano protetti dalla loro strategia combinata di rivestimento e reticolazione. Credito:Wyss Institute presso l'Università di Harvard
Vincere il cancro e una miriade di altre malattie non dipende solo dall'ottenere i farmaci giusti, ma anche dal portarli nei punti giusti del corpo, mantenendo al minimo i danni ai tessuti sani. Le nanostrutture di DNA come gli origami di DNA autoassemblanti che si piegano in forme definite sono veicoli promettenti per la somministrazione di farmaci e diagnostica, e diverse strategie di vaccinazione. Questo perché possono essere funzionalizzati in modo flessibile con farmaci a piccole molecole e proteine, e antigeni immunogeni, così come le caratteristiche che facilitano la loro consegna a cellule e tessuti bersaglio specifici. Inoltre, sono biocompatibili e biodegradabili.
Il grande potenziale delle nanostrutture di DNA per diverse applicazioni biomediche, però, è ancora ostacolato dalla loro limitata stabilità nei tessuti e nel sangue del corpo. William Shih, dottorato di ricerca e il suo team hanno ora ideato un facile, efficace, e un approccio scalabile di reticolazione chimica in grado di fornire alle nanostrutture di DNA la stabilità di cui hanno bisogno come veicoli di consegna per farmaci e diagnostica. Il loro studio è pubblicato su Giornale della Società Chimica Americana ( JACS ).
"Per contribuire a mantenere la straordinaria promessa delle nanostrutture di DNA, abbiamo sviluppato un approccio chimico ampiamente applicabile per aumentare la loro resistenza alla degradazione, " ha detto William Shih, un membro della Core Faculty presso il Wyss Institute che guida il progetto nell'Iniziativa di Robotica Molecolare dell'Istituto. "Modificando le nanostrutture del DNA in due semplici passaggi, possiamo migliorare notevolmente la loro sopravvivenza, che rimuove un collo di bottiglia centrale nella traduzione di quei nanodispositivi in soluzioni a una varietà di problemi medici".
Gli origami di DNA sono tipicamente assemblati da un lungo filamento di DNA che si piega in una forma tridimensionale definita su scala nanometrica con l'aiuto di più filamenti corti che collegano diverse parti della struttura nello spazio. La spina dorsale del DNA è fortemente caricata negativamente, il che significa che portare diverse parti dei fili pieghevoli l'una vicino all'altra può essere problematico perché si respingono naturalmente l'un l'altro, simile alle superfici negative di due magneti. Per vincere queste forze repulsive, i ricercatori aggiungono comunemente un eccesso di ioni caricati positivamente come gli ioni di magnesio (Mg 2 + ) alle loro reazioni di piegatura che coprono le cariche negative del DNA.
Spesso, però, il Mg aggiunto 2 + gli ioni non sono sufficientemente mantenuti nelle strutture origami di DNA 3D. Soprattutto quando introdotto nel corpo, dove normale Mg 2 + le concentrazioni sono molto più basse, Mg 2 + gli ioni fuoriescono dalle nanostrutture e le fanno disintegrare. Inoltre, Le nanostrutture del DNA sono sotto costante attacco da parte degli enzimi della DNA nucleasi che sono prodotti naturalmente nel corpo e degradano le molecole di DNA libere, riducendo drasticamente la loro stabilità, che comunemente viene misurata come la loro emivita. Ne consegue logicamente che interrompendo l'integrità strutturale delle nanostrutture di DNA, queste forze interne ed esterne riducono anche il rilascio di farmaci o la disponibilità di molecole reporter diagnostiche.
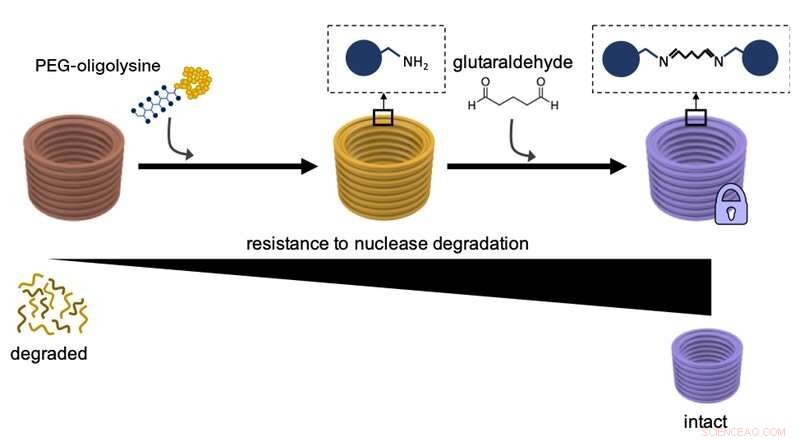
Questo diagramma spiega come rivestire le nanostrutture di DNA con PEG-oligolisine, e quindi la reticolazione chimica di distinte oligolisine PEG con glutaraldeide come agente di reticolazione aumenta la loro resistenza alla degradazione da parte degli enzimi della DNA nucleasi e la stabilità complessiva. Credito:Wyss Institute presso l'Università di Harvard
In uno studio precedente, Shih e il suo team hanno trovato un modo per superare la necessità di un'eccessiva Mg 2 + concentrazioni per stabilizzare le nanostrutture di DNA. Rivestendo essenzialmente le superfici dei grandi filamenti di DNA con un agente neutralizzante relativamente piccolo e discreto che trasporta più cariche positive ed è noto come PEG-oligolisina (o oligolisina PEGilata), avevano inventato un metodo che poteva essere facilmente applicato per stabilizzare le nanostrutture di DNA in tutte le forme e forme in modo scalabile. L'oligolisina PEGilata è costituita da corte catene dell'amminoacido lisina, uno degli elementi costitutivi delle proteine, che sono saldamente attaccati al polietilenglicole (PEG), una molecola polimerica in grado di legare più catene di oligolisina. I ricercatori pensano che il PEG funzioni come un "pennello molecolare" per prevenire l'aggregazione delle nanoparticelle neutralizzate.
A differenza del singolo Mg 2 + ioni che, in teoria, ciascuno può neutralizzare solo due delle tante cariche negative esposte dalla spina dorsale del DNA con le loro due cariche positive, L'oligolisina PEGilata può coprire più cariche negative di DNA contemporaneamente, e forma così una "rete elettrostatica" stabile che ricopre la superficie delle nanostrutture di DNA. La stabilità delle nanostrutture rivestite è stata mantenuta anche nelle cellule viventi e nei topi, dimostrando che la squadra era sulla strada giusta.
"Utilizzando questa semplice strategia, potremmo estendere la sopravvivenza delle nanostrutture di DNA di circa 400 volte con emivite fino a 36 ore in ambienti fisiologici che contenevano anche normali livelli di nucleasi, " ha detto la prima autrice Frances Anastassacos, dottorato di ricerca, che al momento dello studio era uno studente laureato che lavorava con Shih. "Però, questo non era ancora all'altezza di ciò che è necessario in alcune applicazioni terapeutiche reali. L'oligolisina PEGilata tendeva ancora a cadere dal DNA in una certa misura".
Nel JACS studio, il team ha ora risolto questa parte rimanente del "problema di stabilità". "Abbiamo essenzialmente legato nodi aggiuntivi alla rete elettrostatica utilizzando un reagente di reticolazione chimico noto come "glutaraldeide" che lega fortemente distinte oligolisine PEGilate sulla superficie delle nanostrutture di DNA, " ha detto Anastassacos. "In presenza di livelli di nucleasi di DNA che superano di gran lunga quelli del corpo umano, la loro sopravvivenza si estendeva oltre le 300 ore. L'aumento di stabilità di 400 volte che abbiamo osservato con la sola oligolisina PEGilata è stato aumentato di altre 250 volte, che colpisce nel segno per le applicazioni cliniche."
Altri tentativi che sono riusciti a stabilizzare le nanostrutture del DNA con modifiche chimiche si sono basati principalmente sulla riprogettazione delle strutture esistenti in modo che siti specifici all'interno delle loro strutture 3-D diventassero accessibili alla chimica dispiegata. In contrasto, "il nostro approccio può essere eseguito su qualsiasi nanostruttura di DNA, e la sua facilità ed economicità potrebbero rafforzare significativamente la traduzione di molte strutture terapeutiche e diagnostiche già esistenti e di nuova concezione, " disse Zhao Zhao, dottorato di ricerca, che è un co-primo autore dello studio ed ex borsista post-dottorato nel team di Shih.
Nel loro studio, Shih e il suo team miravano a massimizzare la stabilità delle nanostrutture di DNA. I ricercatori, però, pensare che variando ulteriormente la fase di reticolazione, l'emivita delle strutture potrebbe essere messa a punto per applicazioni specifiche che richiedono la disponibilità di molecole cargo in tempi e intervalli di tempo diversi. Hanno già scoperto che il loro metodo di protezione non interferiva con il legame delle molecole cargo alle strutture modificate e l'assorbimento delle strutture da parte delle cellule umane in coltura. Ora, può iniziare la traduzione clinica.