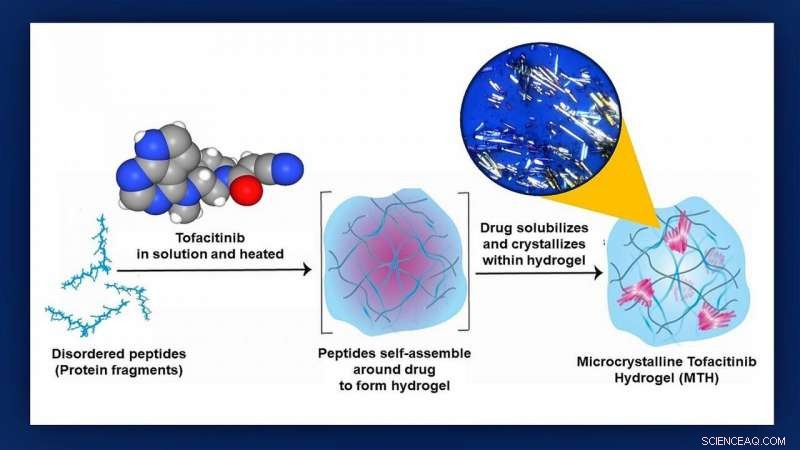
I ricercatori della Johns Hopkins Medicine e dell'NCI Frederick hanno dimostrato nei topi che possono facilmente fornire una promettente terapia anti-rigetto direttamente a un cuore trapiantato confezionandolo all'interno di un minuscolo bozzolo di gel proteico noto come idrogel. I passaggi nella costruzione dell'idrogel e nell'incapsulamento del farmaco, tofacitinib, sono illustrati in questo grafico. L'inserto in alto a destra è una microfotografia reale dei cristalli di tofacitinib in posizione Credito:grafico creato da M.E. Newman, Medicina Johns Hopkins, utilizzando un'illustrazione originale di Poulami Majumder e un modello molecolare di tofactinib per gentile concessione del National Center for Biotechnology Information
Per i pazienti che riceveranno un trapianto di cuore nel prossimo futuro, il vecchio adagio, "Le cose buone arrivano in piccoli pacchetti, " possono diventare parole con cui vivere. In uno studio recente, i ricercatori della Johns Hopkins Medicine e del National Cancer Institute (NCI) hanno dimostrato nei topi che possono facilmente somministrare un promettente farmaco anti-rigetto direttamente nell'area che circonda un cuore innestato confezionandolo all'interno di un minuscolo contenitore tridimensionale, bozzolo di gel proteico noto come idrogel. Meglio di tutto, i ricercatori affermano che il rilascio del farmaco è scaglionato nel tempo, rendendolo altamente regolabile ed eliminando la necessità di farmaci giornalieri per tenere sotto controllo il rigetto.
I risultati sono presentati nel 18 agosto, 2020, numero della rivista Piccolo .
Prevenire il rigetto di un cuore trapiantato è stata spesso una situazione di Catch-22. Se somministrate a un ricevente d'organo grandi quantità di farmaci immunosoppressori, ci possono essere gravi effetti collaterali, compreso il danno renale, ipertensione, squilibri di zucchero nel sangue e persino linfomi. Ridurre la dose può essere più sicuro per la salute generale, ma aumenta il rischio che il rigetto non venga adeguatamente controllato e il cuore trapiantato vada perduto.
"Ciò che serviva era un metodo di somministrazione del farmaco che ottenesse il farmaco anti-rigetto solo dove necessario; proteggesse il farmaco dalla degradazione prematura e mantenesse un'alta concentrazione per il periodo di tempo necessario per riqualificare il sistema immunitario, ", afferma il coautore dello studio Giorgio Raimondi, M.Sc., dottorato di ricerca, assistente professore di chirurgia plastica e ricostruttiva presso la Johns Hopkins University School of Medicine.
"Due studi precedenti hanno utilizzato il metodo dell'idrogel per somministrare con successo farmaci immunosoppressori convenzionali ad altri siti, e questo ci ha spinto a provarlo per i cuori trapiantati, " spiega Raimondi. "Inoltre, lavoro di un team presso l'NCI Frederick National Laboratory for Cancer Research sotto Joel Schneider [Ph.D., un coautore dello studio] ha dimostrato che i pacchetti di farmaci idrogel possono essere somministrati con una siringa".
Il farmaco che questi ricercatori volevano fornire ai cuori trapiantati è tofacitinib, un inibitore del processo mediante il quale le cellule allertano la loro ricettività al legame con proteine che inducono l'infiammazione chiamate citochine. Nelle normali risposte immunitarie agli invasori estranei all'interno del corpo, le citochine svolgono un ruolo fondamentale nell'avvisare i globuli bianchi specializzati, i linfociti T, per attaccare e rimuovere i batteri o i virus minacciosi. Però, le citochine in presenza di un cuore trapiantato possono indirizzare il sistema immunitario a distruggere l'innesto.
Per vedere se un corriere idrogel potrebbe essere utilizzato per consegnare tofacitinib, i ricercatori hanno prima innestato cuori di topo nel collo dei topi riceventi per creare un modello animale di un trapianto umano. Prossimo, hanno mescolato tofacitinib con una soluzione di piccoli frammenti proteici che si sono assemblati attorno al farmaco durante un processo di incubazione di 24 ore che Raimondi paragona ai kit "crea il tuo cristallo" popolari tra i bambini.
"Abbiamo scoperto che trasformare il tofacitinib in un cristallo controllava al meglio il modo in cui il farmaco si diffonde dall'idrogel, ", afferma l'autore principale dello studio Poulami Majumder, dottorato di ricerca, ex NCI presso Frederick borsista post-dottorato. "Il risultante 'tofacitinib idrogel microcristallino, ' o MTH, era estremamente stabile, ha preservato il farmaco incapsulato in ottime condizioni e potrebbe essere iniettato nel sito del trapianto semplicemente usando una siringa".
I ricercatori hanno testato il sistema di somministrazione di MTH nel loro modello murino in tandem con un secondo farmaco immunosoppressore, CTLA4-Ig, che è stato iniettato separatamente. Era la prima volta che veniva provata questa specifica terapia combinata.
Per determinare se la posizione della consegna MTH era importante, i ricercatori hanno iniettato localmente il medicinale confezionato, nel sito del trapianto, e lontano, vicino alla coda del topo. Come previsto, solo il gruppo di topi con iniezioni locali ha mostrato un aumento significativo del tempo di sopravvivenza dell'innesto.
"La sopravvivenza media dei cuori innestati nel gruppo iniettato localmente è stata di circa 125 giorni rispetto ai soli 35 giorni per i topi iniettati con MTH lontano dal trapianto, " Dice Raimondi. "Abbiamo anche testato il plasma del primo gruppo e abbiamo trovato solo tracce minime rilevabili di tofacitinib, il che significa che la somministrazione di MTH mantiene il farmaco vicino al sito del trapianto e gli consente di agire in sinergia con CTLA4-Ig per fornire una protezione potenziata e duratura dell'organo».
Senza il trattamento con tofactinib/CTLA4, Raimondi dice, i cuori dei topi trapiantati hanno smesso di battere entro 10 giorni.
Raimondi afferma che tra i vantaggi dell'utilizzo dell'MTH come sistema di somministrazione dei farmaci c'è il fatto che l'idrogel rilascia il suo contenuto lentamente, per un periodo da 5 a 20 giorni, e non provoca altre complicazioni perché è biocompatibile, non infiammatorio e biodegradabile. Lui e i suoi colleghi credono che l'uso dell'ingegneria dei cristalli per migliorare ulteriormente la capsula di idrogel, è possibile ottenere un maggiore controllo sulla velocità di rilascio, un obiettivo fondamentale da raggiungere prima di poter tentare la sperimentazione umana, oppure, la capsula può essere resa "sintonizzabile" per erogare farmaco solo quando il cuore trapiantato viene attaccato dal sistema immunitario.
I ricercatori ritengono inoltre che con ulteriori ricerche e test, il sistema di somministrazione MTH potrebbe essere applicato alla lotta contro il rigetto degli organi trapiantati diversi dal cuore e nel trattamento delle malattie autoimmuni.