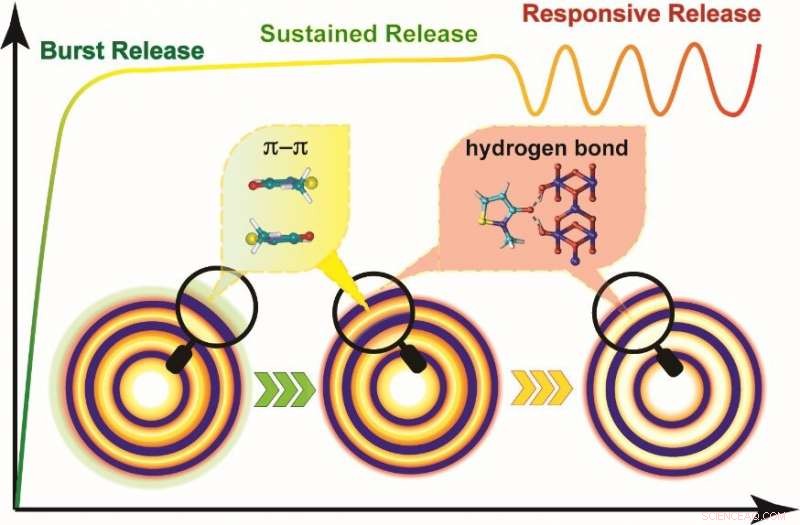
Illustrazione schematica del rilascio sequenziale del farmaco da parte della struttura multiguscio Hollow. Credito:Yang Nailiang
Strutture cave multishell (HoMS), con cavità relativamente isolate e pori gerarchici nei gusci, sono strutturalmente simili alle cellule. Possono essere utilizzati come veicolanti per agenti antibatterici.
Una recente ricerca condotta dal Prof. Wang Dan e dal Prof. Zhang Suojiang dell'Institute of Process Engineering (IPE) dell'Accademia Cinese delle Scienze ha studiato il meccanismo di diffusione e trasporto di molecole antimicrobiche attraverso HoMS, e ha scoperto che l'esclusiva proprietà dell'ordine spazio-temporale degli HoMS può realizzare per la prima volta il rilascio sequenziale del farmaco.
Questa ricerca è stata pubblicata in Comunicazioni sulla natura il 7 settembre.
"Abbiamo sintetizzato TiO 2 -HoMS attraverso l'approccio del modello sequenziale, e ha introdotto l'agente antibatterico Metilisotiazolinone (MIT) come molecole modello negli HoMS, " ha detto il prof. Wang.
Analizzando il comportamento degli HoMS durante il rilascio del farmaco, i ricercatori hanno scoperto che il rilascio delle molecole dagli HoMS passava attraverso fasi di rilascio sequenziali, vale a dire rilascio a raffica, rilascio prolungato, e rilascio reattivo allo stimolo.
In dettaglio, semplicemente regolando la quantità di MIT-HoMS introdotti nell'ambiente, la concentrazione desiderata può essere raggiunta rapidamente nella fase di burst release grazie alle molecole MIT assorbite sulla superficie esterna degli HoMS.
Il rilascio prolungato di molecole MIT nello stato impilato π-π nella cavità degli HoMS potrebbe mantenere la concentrazione richiesta per un lungo periodo e inibire la crescita dei batteri.
L'HoMS a triplo guscio potrebbe fornire un lungo periodo di sterilità in un ambiente ricco di batteri che è quasi otto volte più lungo di quello dell'agente antimicrobico puro nelle stesse condizioni.
"Quando gli agenti patogeni estranei sono stati aggiunti al nostro sistema HoMS, la forza motrice era abbastanza forte da rompere la barriera energetica, e le molecole di farmaco immagazzinate tra i gusci e assorbite in superficie sono state rilasciate, con conseguente rilascio reattivo. Ma ancora più importante, la concentrazione del farmaco può essere ripristinata automaticamente all'intervallo desiderato, " ha detto il prof. Wang.
A causa delle diverse caratteristiche di adsorbimento negli HoMS e delle barriere fisiche dei multishell, molecole di farmaco in diverse posizioni di HoMS hanno tempi di rilascio diversi.
Tutti questi vantaggi potrebbero essere attribuiti al rilascio sequenziale di farmaci guidato dalla diffusione chimica e dalla barriera fisica, fornendo un percorso per la progettazione di nanomateriali intelligenti.