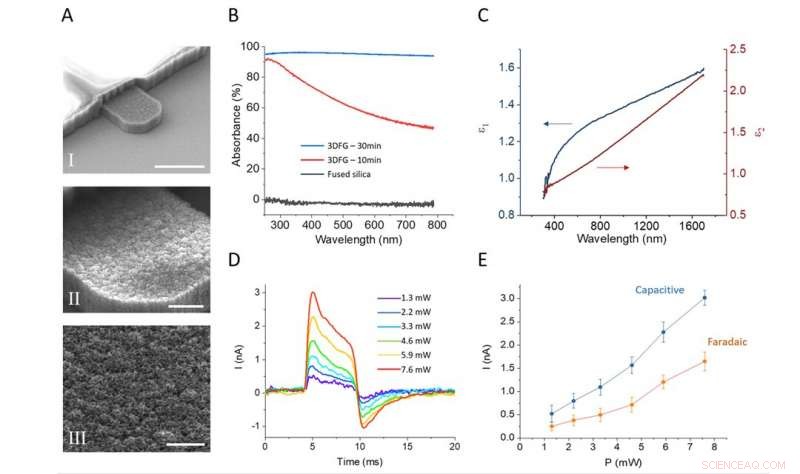
Le immagini SEM forniscono uno sguardo più da vicino agli elettrodi 3DFG. Credito:Carnegie Mellon University, Dipartimento di Ingegneria Biomedica
Dietro ogni battito cardiaco e segnale cerebrale c'è un'enorme orchestra di attività elettrica. Mentre le attuali tecniche di osservazione elettrofisiologica sono state per lo più limitate alle registrazioni extracellulari, un gruppo lungimirante di ricercatori della Carnegie Mellon University e dell'Istituto Italiano di Tecnologia ha identificato un flessibile, basso costo, e piattaforma biocompatibile per consentire registrazioni intracellulari più ricche.
L'esclusiva partnership "attraverso l'oceano" del gruppo è iniziata due anni fa alla Bioelectronics Winter School (BioEl) con libagioni e uno schizzo di tovaglioli da bar. Si è evoluto in una ricerca pubblicata in Progressi scientifici , dettagliare una nuova piattaforma di microelettrodi che sfrutta il grafene fuzzy tridimensionale (3DFG) per consentire registrazioni intracellulari più ricche di potenziali d'azione cardiaci con un elevato rapporto segnale/rumore. Questo progresso potrebbe rivoluzionare la ricerca in corso relativa alle malattie neurodegenerative e cardiache, così come lo sviluppo di nuove strategie terapeutiche.
Un leader chiave in questo lavoro, Tzahi Cohen Karni, professore associato di ingegneria biomedica e scienza e ingegneria dei materiali, ha studiato le proprietà, effetti, e potenziali applicazioni del grafene durante tutta la sua carriera. Ora, sta facendo un passo collaborativo in una direzione diversa, utilizzando un orientamento verticale dello straordinario materiale a base di carbonio (3DFG) per accedere al compartimento intracellulare della cellula e registrare l'attività elettrica intracellulare.
Grazie alle sue proprietà elettriche uniche, il grafene si distingue come un candidato promettente per i dispositivi di biorilevamento a base di carbonio. Recenti studi hanno dimostrato il successo dell'impiego di biosensori al grafene per il monitoraggio dell'attività elettrica dei cardiomiociti, o cellule del cuore, fuori dalle cellule, o in altre parole, registrazioni extracellulari dei potenziali d'azione. registrazioni intracellulari, d'altra parte, sono rimasti limitati a causa di strumenti inefficaci... fino ad ora.
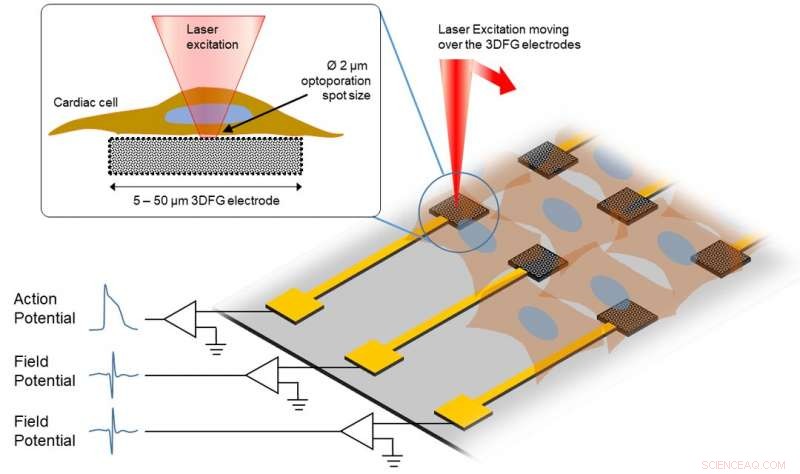
Questo schizzo mostra la procedura sperimentale del laser ultraveloce che si muove sugli elettrodi 3DFG. Credito:Facoltà di Ingegneria, Università Carnegie Mellon
"Il nostro obiettivo è registrare l'intera orchestra, vedere tutte le correnti ioniche che attraversano la membrana cellulare, non solo il sottoinsieme dell'orchestra mostrato dalle registrazioni extracellulari, " spiega Cohen-Karni. "L'aggiunta della dimensione dinamica delle registrazioni intracellulari è di fondamentale importanza per lo screening dei farmaci e il test di tossicità, ma questo è solo un aspetto importante del nostro lavoro".
"Il resto è il progresso tecnologico, " Cohen-Karni continua. "3DFG è economico, piattaforma flessibile e interamente in carbonio; nessun metallo coinvolto. Possiamo generare elettrodi di questo materiale delle dimensioni di un wafer per consentire registrazioni intracellulari multisito in pochi secondi, che è un miglioramento significativo rispetto a uno strumento esistente, come un morsetto patch, che richiede ore di tempo e competenza."
Così, Come funziona? Sfruttando una tecnica sviluppata da Michele Dipalo e Francesco De Angelis, ricercatori dell'Istituto Italiano di Tecnologia, un laser ultraveloce viene utilizzato per accedere alla membrana cellulare. Puntando brevi impulsi di laser sull'elettrodo 3DFG, un'area della membrana cellulare diventa porosa in un modo, consentendo di registrare l'attività elettrica all'interno della cellula. Quindi, i cardiomiociti vengono coltivati per studiare ulteriormente le interazioni tra le cellule.
interessante, 3DFG è nero e assorbe la maggior parte della luce, con conseguente proprietà ottiche uniche. In combinazione con la sua struttura simile alla schiuma e l'enorme superficie esposta, 3DFG ha molti tratti desiderabili che sono necessari per realizzare piccoli biosensori.
"Abbiamo sviluppato un elettrodo più intelligente; un elettrodo che ci consente un migliore accesso, " sottolinea Cohen-Karni. "Il più grande vantaggio dalla mia parte è che possiamo avere accesso a questa ricchezza di segnali, essere in grado di esaminare processi di importanza intracellulare. Avere uno strumento come questo rivoluzionerà il modo in cui possiamo studiare gli effetti delle terapie sugli organi terminali, come il cuore».
Mentre questo lavoro va avanti, il team prevede di applicare le sue conoscenze in interfacce cellula/tessuto su larga scala, per comprendere meglio lo sviluppo dei tessuti e la tossicità dei composti chimici (ad es. tossicità del farmaco).