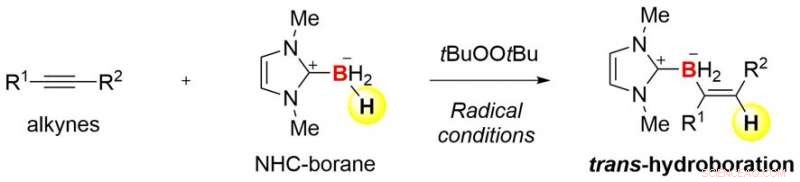
Panoramica della presente ricerca Credito:Kanazawa University
Una combinazione di organoboro e chimica dei radicali genera un'insolita trans-selettività nell'idroborazione degli alchini. L'uso di borani carbene N-eterociclici è la chiave del successo di questa trasformazione chimica. Questo studio dovrebbe aprire le porte allo sviluppo di nuovi materiali contenenti boro.
I composti organoboro sono stati ampiamente utilizzati per creare nuove molecole organiche da quando il Prof. Suzuki, vincitore del Premio Nobel 2010 per la chimica, sviluppato reazioni di accoppiamento incrociato catalizzate da palladio con composti di organoboro (accoppiamento Suzuki). Inoltre, molti composti contenenti boro stessi sono materiali promettenti. Possono essere usati come medicinali e materiali organici di elettroluminescenza a causa della natura elettronica unica del boro.
Il borano (BH3) e i suoi derivati stabilizzati da ligandi sono i composti di boro più semplici. Possono reagire con un triplo legame carbonio-carbonio (alchino, C-C) per ottenere un prodotto di inserzione (H-C=C-BH 2 ). Questa reazione, chiamato idroborazione, è un metodo potente per preparare composti organoboro. Però, la reazione fornisce tipicamente solo un prodotto cis, il che significa che H e BH 2 vengono introdotti dallo stesso lato del triplo legame. Questo è, è difficile sintetizzare un prodotto di trans-idroborazione con la configurazione geometrica opposta. In precedenza, ci sono stati esempi molto limitati di trans-idroborazione di alchini.
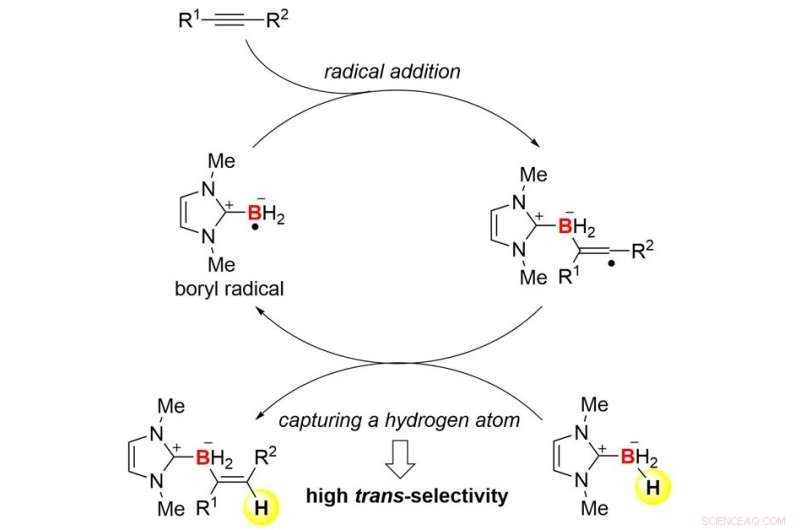
Cenni sul meccanismo di reazione. Credito:Università di Kanazawa
Il team di collaborazione tra l'Università di Kanazawa e l'Università di Pittsburgh è riuscito a sviluppare reazioni di trans-idroborazione degli alchini basate sulla chimica dei radicali (Figura 1). Il team ha impiegato carbene borani N-eterociclici (NHC-borani) per combinare l'idroborazione con la chimica dei radicali. I borani NHC possono essere maneggiati facilmente grazie alla loro stabilità, e sono buoni precursori dei radicali borile (radicali boro centrati). Infatti, un radicale NHC-borile può essere facilmente formato mediante semplice termolisi in presenza di perossido di di-terz-butil commerciale poco costoso. Il radicale può aggiungersi a un alchino per formare un legame carbonio-boro (C-B) e un nuovo radicale carbonio (Figura 2). La transselettività nell'idroborazione è indotta cineticamente quando il radicale carbonioso altamente reattivo cattura un atomo di idrogeno dall'NHC-borano di partenza. Di conseguenza, il processo complessivo stabilisce un ciclo a catena radicale. Questo meccanismo è molto diverso da quello delle reazioni di idroborazione note.
Dagli alchini facilmente reperibili, il presente protocollo fornisce vari composti di alchenil borano stabili al banco che non sono facilmente accessibili con metodi noti. Alcuni di essi possono essere convertiti in imitazioni retinoidi, che sono candidati alla droga, mediante giunto Suzuki modificato (Figura 3).
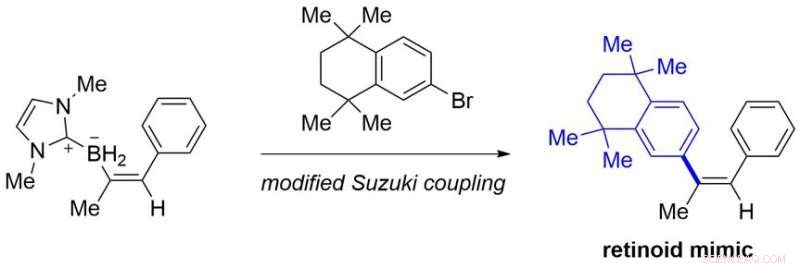
L'applicazione di un prodotto di sintesi. Credito:Università di Kanazawa
I composti organoboro sintetizzati con il presente metodo daranno accesso a nuovi sistemi contenenti boro mediante un'ulteriore trasformazione chimica. Perciò, questo tipo di reazione di trans-idroborazione faciliterà i progressi nella chimica farmaceutica e nella scienza dei materiali. Dal punto di vista della chimica pura, questo studio amplia il potenziale dei radicali nella chimica di sintesi. In breve, illustriamo che i radicali sono in grado di controllare le reazioni chimiche proprio nonostante la loro estrema reattività.
Dennis Curran (Università di Pittsburgh), un collaboratore di questo studio, dice, "È stato un piacere essere coinvolti in questa collaborazione, che è stato guidato dal team di Kanazawa. La nuova reazione che abbiamo scoperto è unica, e sono entusiasta delle sue prospettive di estensione nelle direzioni sia della ricerca di base che delle applicazioni pratiche."