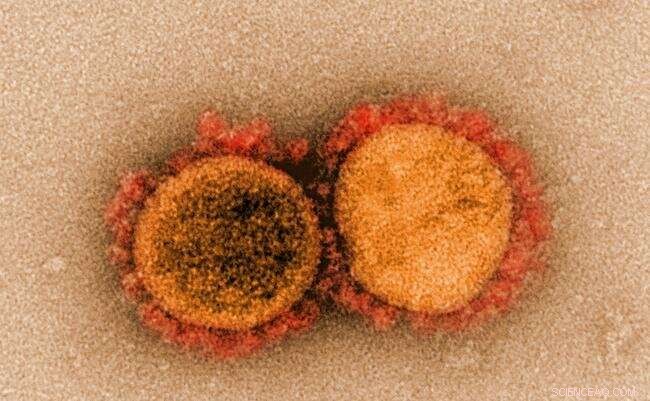
Micrografia elettronica a trasmissione di particelle di virus SARS-CoV-2, isolato da un paziente. Immagine acquisita e migliorata dal colore presso il NIAID Integrated Research Facility (IRF) a Fort Detrick, Maryland. Attestazione:NIAID
I nanodecoy realizzati da cellule sferoidi polmonari umane (LSC) possono legarsi e neutralizzare SARS-CoV-2, promuovere la clearance virale e ridurre il danno polmonare in un modello macaco di COVID-19. Imitando il recettore a cui si lega il virus invece di prendere di mira il virus stesso, la terapia con nanodecoy potrebbe rimanere efficace contro le varianti emergenti del virus.
SARS-CoV-2 entra in una cellula quando la sua proteina spike si lega al recettore dell'enzima di conversione dell'angiotensina 2 (ACE2) sulla superficie della cellula. Le LSC, una miscela naturale di cellule staminali epiteliali polmonari e cellule mesenchimali, esprimono anche ACE2, rendendoli un veicolo perfetto per ingannare il virus.
"Se si pensa alla proteina spike come a una chiave e al recettore ACE2 della cellula come a un lucchetto, allora quello che stiamo facendo con i nanodecoy è travolgere il virus con serrature finte in modo che non possa trovare quelle che lo lasciano entrare nelle cellule polmonari, "dice Ke Cheng, autore corrispondente della ricerca. "Le finte serrature legano e intrappolano il virus, impedendogli di infettare le cellule e replicarsi, e il sistema immunitario del corpo si prende cura del resto".
Cheng è Randall B. Terry Jr. Distinguished Professor in Medicina Rigenerativa presso la North Carolina State University e professore presso il Dipartimento congiunto di ingegneria biomedica NC State/UNC-Chapel Hill.
Cheng e colleghi di NC State e UNC-CH hanno convertito singole LSC in nanovescicole, o minuscole bolle di membrana cellulare con recettori ACE2 e altre proteine specifiche delle cellule polmonari sulla superficie.
Hanno confermato che la proteina spike si è legata ai recettori ACE2 sui richiami in vitro, ha quindi utilizzato un virus mimico SARS-Co-V-2 fabbricato per i test in vivo in un modello murino. I richiami sono stati consegnati tramite terapia inalatoria. Nei topi, le nanoesche sono rimaste nei polmoni per 72 ore dopo una dose e l'eliminazione accelerata del virus mimico.
Finalmente, un'organizzazione di ricerca a contratto ha condotto uno studio pilota su un modello di macaco e ha scoperto che la terapia inalatoria con le nanoesche accelerava la clearance virale, e ridotta infiammazione e fibrosi nei polmoni. Sebbene non sia stata osservata alcuna tossicità nello studio sui topi o sui macachi, saranno necessari ulteriori studi per tradurre questa terapia per i test sull'uomo e determinare esattamente come le nanoesche vengono eliminate dal corpo.
"Questi nanoechi sono essenzialmente fantasmi cellulari, ' e un LSC può generare circa 11, 000 di loro, " Dice Cheng. "La distribuzione di milioni di questi richiami aumenta esponenzialmente la superficie dei siti di legame falsi per intrappolare il virus, e le loro piccole dimensioni li trasformano sostanzialmente in piccoli snack per macrofagi, quindi vengono eliminati in modo molto efficiente."
I ricercatori sottolineano altri tre vantaggi dei nanodecoy LSC. Primo, possono essere somministrati in modo non invasivo ai polmoni tramite terapia inalatoria. Secondo, poiché le nanoesche sono acellulari - non c'è nulla che viva all'interno - possono essere facilmente conservate e rimanere stabili più a lungo, consentendo l'uso standard. Finalmente, Le LSC sono già in uso in altri studi clinici, quindi c'è una maggiore probabilità di poterli utilizzare nel prossimo futuro.
"Concentrandoci sulle difese del corpo piuttosto che su un virus che continuerà a mutare, abbiamo il potenziale per creare una terapia che sarà utile a lungo termine, " Dice Cheng. "Finché il virus ha bisogno di entrare nella cellula polmonare, possiamo continuare a ingannarlo."
La ricerca appare in Nanotecnologia della natura ed è stato sostenuto dal National Institutes of Health e dall'American Heart Association. Dottor Jason Lobo, pneumologo presso UNC-CH, è co-autore del documento.