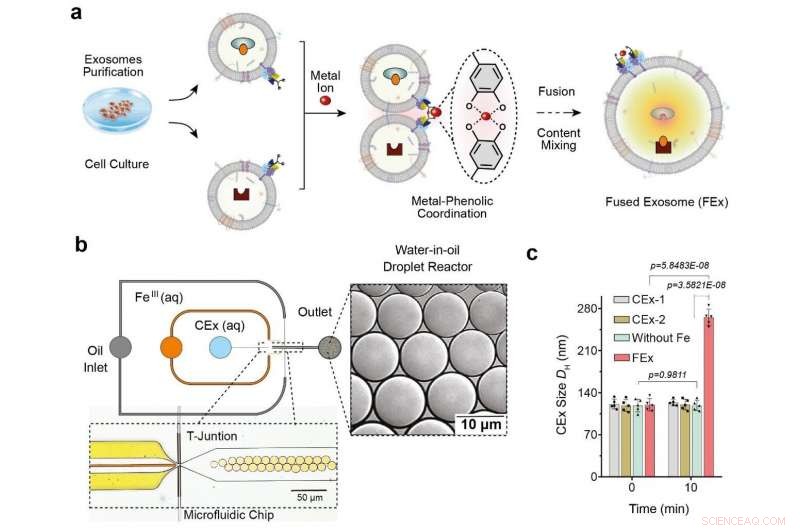
(a) Lo ione Fe3+ innesca la fusione della membrana negli esosomi adattati con catecolo (CEx). La formazione di un complesso metallo-catecolo avvicina gli esosomi e consente la fusione. Diversi reagenti in ciascun esosoma vengono quindi incapsulati insieme, promuovere la miscelazione e innescare reazioni all'interno degli esosomi fusi (FEx). (b) Il dispositivo microfluidico progettato per generare reattori a goccioline acqua-in-olio alla giunzione di focalizzazione del flusso. Le due fasi acquose (CEx e sale metallico) si incontrano e vengono immesse nel flusso di olio (1% tensioattivo PFPE-PEG in FC-40) per rompere il liquido in goccioline. (c) Dimensione media degli esosomi non fusi (CEx-1:121 ± 8 nm, CEx-2:123 ± 5 nm) e esosomi fusi (FEx:265 ± 14 nm). Credito:Istituto per le scienze di base
Le cellule hanno piccoli compartimenti noti come organelli che eseguono complesse reazioni biochimiche. Questi compartimenti hanno più enzimi che lavorano insieme per eseguire importanti funzioni cellulari. I ricercatori del Center for Soft and Living Matter all'interno dell'Institute for Basic Science (IBS, Corea del Sud) hanno imitato con successo questi compartimenti spaziali su nanoscala per creare "mitocondri artificiali". Lo studio è pubblicato su Catalisi della natura come articolo di copertina. I ricercatori affermano che la tecnologia può essere utilizzata per costruire organelli artificiali in grado di fornire ATP o altre molecole utili alle cellule nei tessuti danneggiati o malati.
Ciò è stato ottenuto attraverso la riprogrammazione degli esosomi, che sono piccole vescicole (diametro ~ 120 nm) che le cellule utilizzano per la segnalazione intercellulare. I ricercatori hanno effettuato gli esperimenti utilizzando reattori a goccioline microfluidici, che ha generato piccole goccioline di dimensioni simili a cellule tipiche. (diametro ~ 10 μm) I ricercatori hanno prima mirato a facilitare la fusione controllata di questi esosomi all'interno delle goccioline prevenendo fusioni indesiderate.
Hanno realizzato questo adattando le superfici dell'esosoma con molecole chiamate catecolo, che è un agente chelante che forma complessi con ioni metallici. Ciò è stato a sua volta fatto attaccando il catecolo su anticorpi che prendono di mira specifici marcatori cellulari, come CD9. La proprietà di formazione di complessi del catecolo consente loro di guidare fusioni tra esosomi quando vengono miscelati con ioni metallici come Fe 3+ . La fusione della membrana si verifica quando i catecoli sulle superfici si legano al ferro e avvicinano le vescicole l'una all'altra.
I ricercatori hanno prima testato l'efficacia di questo sistema caricando un tipo di esosomi con calceina-Co 2+ e un altro con EDTA. Quando le due vescicole si fondono e il contenuto si mescola, EDTA conquista il Co 2+ lontano da calcein, che poi permette a quest'ultimo di diventare fluorescente. Il team si è reso conto di aver avuto successo nel rilevamento del segnale di fluorescenza, e la fusione è stata ulteriormente confermata dal raddoppio del diametro dell'esosoma misurato.
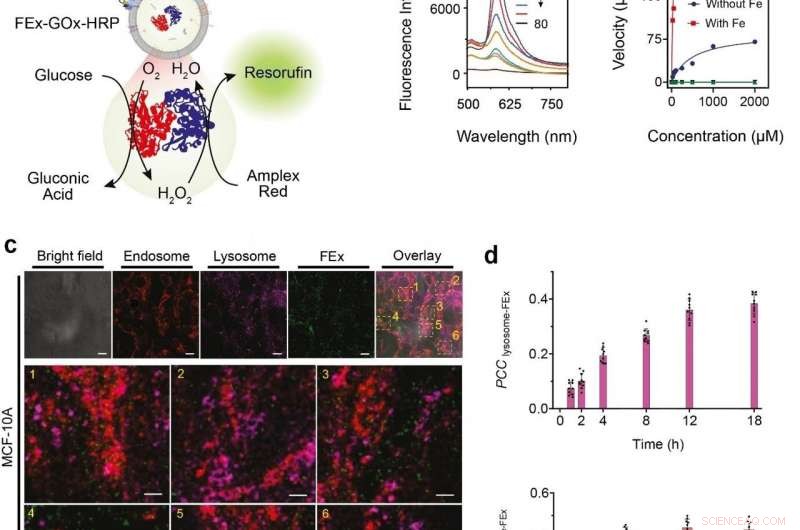
(a) Rappresentazione schematica di un doppio enzima GOx/HRP CEx che si fonde in FEx. La reazione catalitica è stata avviata aggiungendo glucosio, generazione di H2O2 per ossidazione aerobica, che è stato poi utilizzato per ossidare Amplex Red per generare resorufina. (b) Spettri di fluorescenza rappresentativi della resorufina generati dalla biocatalisi in esosomi fusi (FEx-GOx-HRP) in diversi momenti. Velocità di reazione per il nanoreattore rispetto alla concentrazione di glucosio per calcolare le costanti cinetiche adattando l'equazione di Michaelis-Menten. (c) Stabilità e integrità di FEx-GOx-HRP dopo l'integrazione cellulare dopo 48 ore. Endosomi (EEA1, rosso) lisosomi (LAMP1, magenta), e FEx (verde) sono mostrati. (d) Grafico dei valori del coefficiente di correlazione di Pearson (PCCLysosoma-FEx) nel tempo per la fluorescenza magenta (lisosoma) e verde (FEx), e per la fluorescenza rossa (Endosome) e verde (FEx). Credito:Istituto per le scienze di base
Questi esosomi personalizzati sono stati quindi precaricati con diversi reagenti ed enzimi, che li ha trasformati in nano fabbriche biomimetiche. Ciò consente loro di produrre biomolecole di alto valore eseguendo le trasformazioni biocatalitiche desiderate in un modo confinato nello spazio che non è possibile utilizzando provette di laboratorio convenzionali. Il team ha dimostrato questa funzione a cascata biocatalitica multienzimatica incapsulando glucosio ossidasi (GOx) e perossidasi di rafano (HRP) all'interno degli esosomi. Il GOx converte prima il glucosio in acido gluconico e perossido di idrogeno. L'HRP a sua volta utilizza il perossido di idrogeno generato nella prima reazione per ossidare Amplex Red in un prodotto fluorescente, resorufina. I ricercatori sono stati persino in grado di fare un ulteriore passo avanti aggiungendo un terzo enzima, galattosidasi che converte il lattosio in glucosio, nella miscela.
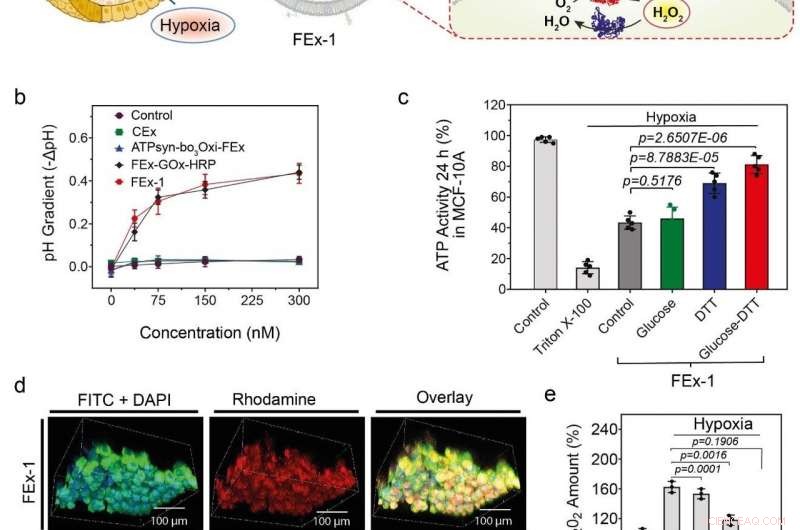
(a) Assemblaggio di organelli artificiali per la generazione di energia. L'ATP sintasi è stata ricostituita in CEx-GOx e la bo3 ossidasi è stata ricostituita in CEx-HRP. I due CEx sono stati fusi e sono stati in grado di penetrare in profondità negli sferoidi. (b) Diminuzione del pH (-ΔpH) rispetto alle concentrazioni di glucosio per diversi esosomi. Gli esosomi fusi mostrano un maggiore grado di diminuzione del pH. (c) Cambiamenti nella produzione di ATP dopo l'assorbimento di FEx-1 in condizioni diverse. (d) Gli organelli artificiali sono stati in grado di penetrare in profondità nello sferoide. La riga superiore mostra FEx-1 (etichettato in rosso con rodamina B), mentre la riga inferiore mostra l'enzima HRP libero all'interno degli sferoidi. (e) I livelli complessivi di ROS sono diminuiti sottoponendo FEx-1 sotto glucosio e DTT. Credito:Istituto per le scienze di base
Prossimo, i ricercatori volevano sapere esattamente quanto bene questi mini reattori possono essere captati e interiorizzati dalle cellule. Le cellule derivate dai tessuti del seno umano sono state alimentate con nanoreattori di esosomi fusi, e la loro interiorizzazione nelle successive 48 ore è stata osservata utilizzando vari marcatori e un microscopio confocale a scansione laser (CLSM). È stato scoperto che le cellule erano in grado di assorbire questi esosomi personalizzati principalmente attraverso l'endocitosi, insieme a molti altri meccanismi. Hanno ulteriormente testato il sistema a due enzimi GOx-HRP nelle cellule, e si è scoperto che gli esosomi fusi erano in grado di produrre con successo prodotti fluorescenti anche mentre si trovavano all'interno delle cellule.
Armato di questa conoscenza, il team ha cercato di creare mitocondri artificiali funzionali in grado di produrre energia all'interno delle cellule. Per realizzare questo, ATP sintasi e bo 3 ossidasi sono stati ricostituiti nei precedenti esosomi contenenti GOx e HRP, rispettivamente. Questi esosomi sono stati a loro volta fusi per creare nanoreattori in grado di produrre ATP utilizzando glucosio e ditiotreitolo (DTT). È stato scoperto che gli esosomi fusi erano in grado di penetrare in profondità nella parte centrale di un tessuto sferoide solido e produrre ATP nel suo ambiente ipossico. Le attività di questi semplici organelli sono state accompagnate da una marcata riduzione della generazione di specie reattive dell'ossigeno (ROS). In contrasto, gli enzimi liberi non sono stati in grado di penetrare all'interno di questi sferoidi di cellule strettamente imballati.
"Presi insieme, i nostri risultati evidenziano il potenziale di questi esosomi come nanoreattori nella regolazione dell'attività metabolica delle cellule all'interno degli sferoidi, e nell'attenuazione del danno cellulare dovuto all'ipossia, " nota CHO Yoon-Kyoung, il corrispondente autore dello studio. Si spera che ulteriori ricerche su tali organelli artificiali presenteranno un nuovo paradigma in vari campi come la diagnosi e il trattamento delle malattie, biotecnologia, medicinale, e l'ambiente.