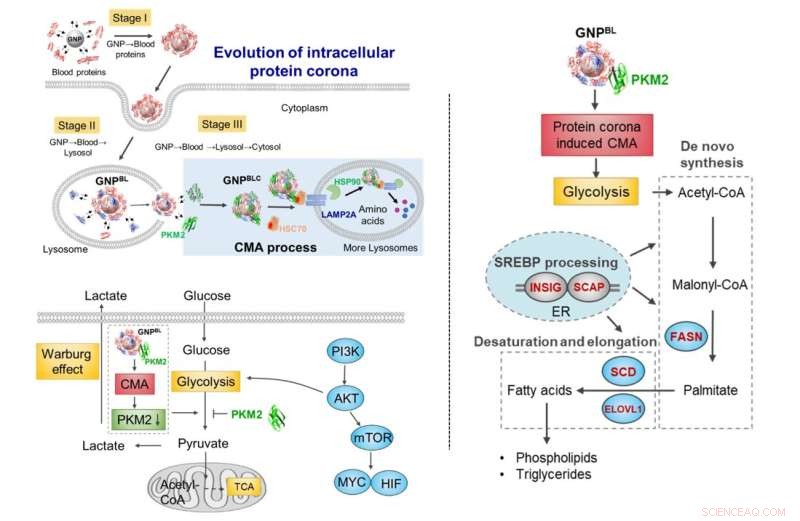
Evoluzione della corona nanoproteica durante il trasporto cellulare. Durante il trasporto dal citoplasma sangue-lisosomiale, lo scambio di componenti della corona proteica con proteine intracellulari (proteine chaperone, chinasi metaboliche) innesca un aumento dell'attività autofagica mediata da proteine chaperone e rimodella selettivamente il metabolismo cellulare. Credito:Chen Chunying et al.
Un gruppo di ricerca guidato dal Prof. Chen Chunying del National Center for Nanoscience and Technology (NCNST) dell'Accademia cinese delle scienze (CAS) ha recentemente studiato l'evoluzione della corona di nanoproteine durante l'endocitosi e il suo disturbo all'omeostasi proteica e alle cellule metabolismo. I loro risultati sono stati pubblicati in PNAS .
Quando le nanoparticelle entrano nei sistemi biologici, le biomolecole del fluido biologico si legano rapidamente alla superficie delle nanoparticelle. La corona di nanoproteine formata dall'interazione con le molecole proteiche nel sangue come fase iniziale ha un enorme impatto sul trasporto e sul destino delle nanoparticelle. Il modo in cui la formazione della corona di nanoproteine influenza il riconoscimento, il trasporto, la distribuzione, la funzione e gli effetti biologici delle nanoparticelle nei tessuti e nelle cellule di diversi sistemi di barriera è una "scatola nera" per l'applicazione medica dei nanomateriali, che non solo limita la consegna efficienza della nanomedicina, ma incide gravemente anche sull'efficacia e sulla sicurezza.
Una sfida importante in quest'area è la complessità della corona nanoproteica, che è influenzata dalla diversità delle biomolecole in diversi tessuti e organi, nonché da stati fisiologici e patologici. Al momento, è urgente capire come evolvono la composizione proteica e le caratteristiche strutturali della corona proteica all'interno dei microambienti biologici.
Per risolvere questo problema, i ricercatori hanno rivelato il modello di evoluzione dinamica della composizione proteica della corona nanoproteica nel processo di trasporto cellulare attraverso l'applicazione innovativa di multi-omica multidimensionale (proteomica, metabolomica, lipidomica), interazioni intermolecolari e imaging di spettrometria di massa in situ.
Prendendo come modello le nanoparticelle d'oro, è stato studiato il processo di evoluzione dinamica della corona proteica dal sistema sanguigno all'intracellulare (citoplasma sangue-lisosomiale). Quando le nanoparticelle sono state endocitate nel lisosoma dall'ambiente sanguigno, e poi sono fuggite dal lisosoma nel citoplasma, la composizione proteica sulla superficie delle nanoparticelle cambierebbe drasticamente. La maggior parte è stata sostituita da molecole proteiche intracellulari, conservando solo una parte dei componenti della corona proteica formati nell'ambiente sanguigno.
Successivamente, l'evoluzione intracellulare della corona nanoproteica non solo ha interrotto l'omeostasi proteica intracellulare (proteostasi), ma ha anche innescato l'arricchimento delle proteine chaperone (HSC70, HSP90) e della piruvato chinasi M2 (PKM2) sulla superficie della nanocorona intracellulare, e autofagia mediata da chaperone stimolata. Ha ulteriormente influenzato la glicolisi cellulare, causando cambiamenti nel metabolismo energetico cellulare e regolando il processo del metabolismo dei lipidi cellulari.
Questo studio chiarisce il modello evolutivo delle nanoparticelle dal sangue a un microambiente subcellulare e identifica la specificità del microambiente intracellulare della corona di nanoproteine, rimodellando così il metabolismo cellulare. Fornisce inoltre supporto teorico per una comprensione approfondita dei complessi effetti biologici dei nanomateriali e della regolazione dell'interfaccia nanobiotica. + Esplora ulteriormente