Credito:Università di Lehigh
Il cancro ovarico uccide 14.000 donne negli Stati Uniti ogni anno. È la quinta causa di morte per cancro tra le donne, ed è così mortale, in parte, perché la malattia è difficile da contrarre nelle sue fasi iniziali. I pazienti spesso non manifestano sintomi fino a quando il cancro non ha iniziato a diffondersi e non ci sono test di screening affidabili per la diagnosi precoce.
Un team di ricercatori sta lavorando per cambiarlo. Il gruppo comprende ricercatori del Memorial Sloan Kettering Cancer Center, Weill Cornell Medicine, University of Maryland, National Institutes of Standards and Technology e Lehigh University.
Due documenti recenti descrivono i loro progressi verso un nuovo metodo di rilevamento del cancro ovarico. L'approccio utilizza tecniche di apprendimento automatico per analizzare in modo efficiente le firme spettrali dei nanotubi di carbonio per rilevare i biomarcatori della malattia e riconoscere il cancro stesso.
Il primo articolo è apparso in Science Advances a novembre.
"Abbiamo dimostrato che una piattaforma di nanosensori basata sulla percezione potrebbe rilevare i biomarcatori del cancro ovarico utilizzando l'apprendimento automatico", afferma Yoona Yang, una ricercatrice associata post-dottorato presso il Dipartimento di ingegneria chimica e biomolecolare di Lehigh e co-primo autore del documento insieme a Zvi Yaari, post-dottorato ricercatore presso il Memorial Sloan Kettering Cancer Center di New York. Gli autori includevano anche Ming Zheng, un chimico ricercatore presso il National Institute of Standards and Technology, Anand Jagota, professore di bioingegneria e ingegneria chimica e biomolecolare presso la Lehigh University, e Daniel Heller, membro associato e capo del Cancer Nanotechnology Laboratory al Memorial Sloan Kettering Cancer Center.
Jagota, che è anche decano associato della ricerca per il College of Health di Lehigh, e Yang sono membri di Nano | Human Interfaces Presidential Initiative, un'iniziativa di ricerca multidisciplinare che mira a cambiare il modo in cui lavoriamo con i dati e i sofisticati strumenti della scoperta scientifica.
Tradizionalmente, il rilevamento dei biomarcatori per la malattia richiede che una molecola di riconoscimento molecolare come un anticorpo sia abbinata a ciascun marcatore. Ma per il cancro ovarico, non esiste un singolo biomarcatore, o analita, che indichi la presenza del cancro. Quando è necessario misurare più analiti in un dato campione, il che può aumentare l'accuratezza di un test, sono necessari più anticorpi, il che aumenta il costo del test e il tempo di risposta.
"Il rilevamento basato sulla percezione funziona come il cervello umano", afferma Yang. "Il sistema consiste in un array di rilevamento che cattura una determinata caratteristica degli analiti in un modo specifico, quindi la risposta dell'insieme dall'array viene analizzata dal modello percettivo computazionale. Può rilevare vari analiti contemporaneamente, il che lo rende molto più efficiente."
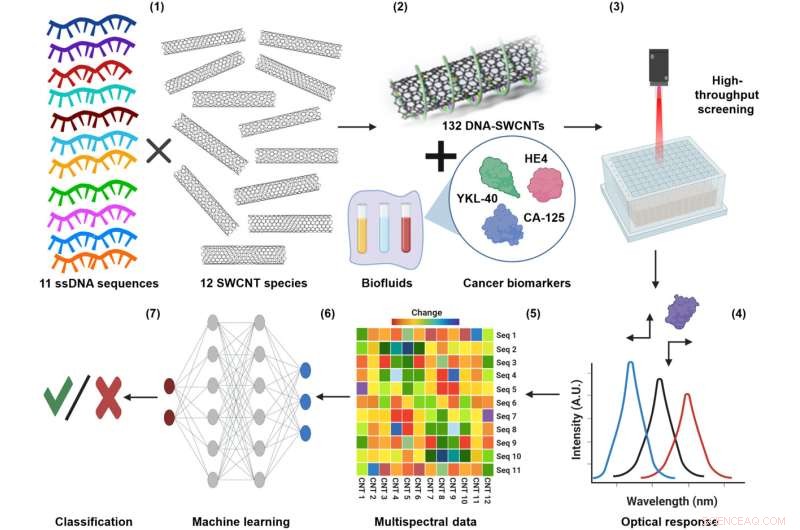
Per questo particolare studio, l'array era costituito da nanotubi di carbonio a parete singola avvolti in filamenti di DNA. Il modo in cui il DNA è stato avvolto e la varietà di sequenze di DNA utilizzate hanno creato una diversità di superfici sui nanotubi. Le diverse superfici, a loro volta, hanno attratto una serie di proteine all'interno di un campione di lavaggio uterino arricchito con livelli variabili di biomarcatori del cancro ovarico.
"I nanotubi di carbonio hanno proprietà elettroniche interessanti", afferma Heller. "Se spari contro di loro, emettono un colore di luce diverso e il colore e l'intensità della luce possono cambiare in base a ciò che si attacca al nanotubo. Siamo stati in grado di sfruttare la complessità di così tante potenziali interazioni di legame utilizzando una gamma di nanotubi con vari involucri. E questo ci ha fornito una gamma di sensori diversi che potevano rilevare cose leggermente diverse e si è scoperto che rispondevano in modo diverso a proteine diverse".
L'algoritmo di apprendimento automatico è stato addestrato utilizzando i dati dell'emissione di nanotubi, le firme spettrali, per riconoscere il modello di emissione che segnalava la presenza e la concentrazione di ciascun biomarcatore.
"La svolta mentale qui è che questi nanotubi sono sensori non specifici", afferma Jagota. "Non sanno nulla di biomarcatori, il che significa che non sono programmati per legarsi a nulla di specifico. Tutto quello che sapevamo è che possono essere esposti a un mezzo acquoso e qualunque cosa a cui siano esposti all'interno di quel mezzo produrrà spostamenti spettrali e variazioni di grandezza. E utilizzando una combinazione di questi sensori, siamo stati in grado di addestrare l'algoritmo a trasformare matematicamente questi input in output con un'elevata precisione. È come avere 20 serie di occhi che vedono tutti cose sovrapposte. Nessun occhio singolo è così buono , ma come collezione, possono essere addestrati a funzionare meglio dei metodi di rilevamento esistenti per il cancro ovarico".
Il secondo articolo è apparso a marzo su Nature Biomedical Engineering e comprendeva il lavoro di molti degli stessi ricercatori. Inoltre, gli autori includevano YuHuang Wang, professore nel dipartimento di chimica e biochimica dell'Università del Maryland, e Mijin Kim, ricercatrice post-dottorato presso il Memorial Sloan Kettering Cancer Center, che era l'autore principale dello studio.
"In questo articolo, non stavamo più guardando i biomarcatori, stavamo guardando la malattia stessa", afferma Heller. "Volevamo sapere, questa tecnologia potrebbe differenziare un campione di sangue da una paziente con cancro ovarico da una paziente senza cancro ovarico?"
Quei pazienti senza cancro ovarico includevano sia persone sane che persone con altre malattie.
In questo studio, i nanotubi sono stati funzionalizzati con difetti quantistici, che hanno sostanzialmente aumentato la diversità delle risposte che i nanotubi avrebbero fornito.
"I nanotubi avevano una certa molecola legata ad esso che gli dava un segnale extra in termini di dati", afferma Jagota. "Dati così più ricchi provenivano da ogni combinazione di nanotubi e DNA. E il modello è stato addestrato non sul biomarcatore, ma sullo stato della malattia".
Il modello ha sviluppato una "impronta digitale della malattia" dalle emissioni spettrali dei nanotubi. I risultati sono stati statisticamente significativi in termini di specificità del modello nel rilevare il cancro ovarico e di sensibilità nel rilevare biomarcatori sia noti che sconosciuti della malattia.
Heller afferma che un'analogia per il modo in cui funziona il modello di apprendimento automatico, in entrambi i documenti, è il naso umano. Ad esempio, non esiste un solo recettore degli odori per ogni odore.
"Invece, c'è un mucchio di diversi recettori degli odori che si legano a determinate molecole e creano uno schema o una sorta di impronta digitale", dice. "E quello schema viene elaborato dal tuo cervello, che a sua volta, ti dice cosa stai annusando. Quindi qui non c'è un sensore particolare che risponda a una cosa in particolare. Ma, in base al modello di sensori diversi che rispondono con vari cambiamenti in termini di colore e intensità della lunghezza d'onda, l'algoritmo è in grado di interpretare cosa è un biomarcatore e cosa no, o cosa è malattia e cosa non lo è".
Il team ha dimostrato che la loro tecnica può rilevare il cancro ovarico meglio dei metodi attuali, ma non è ancora in grado di identificare le prime fasi della malattia. In parte, afferma Heller, il problema è trovare campioni sufficienti per addestrare l'algoritmo perché in quei momenti vengono diagnosticate così poche persone.
"Stiamo lavorando per determinare come possiamo effettivamente rilevare questa malattia nelle prime fasi possibili", afferma.
I prossimi passi potrebbero anche includere lo sviluppo della tecnica per una serie di malattie e la determinazione se può essere ottimizzata per funzionare in condizioni cliniche, afferma Jagota.
"E questa è una tecnica che può essere applicata in una vasta gamma di aree", afferma. "Siamo concentrati sulla salute, ma potrebbe essere usata per identificare le sostanze inquinanti nell'aria, ad esempio. C'è il potenziale per andare dietro a molte malattie e condizioni diverse, e lo trovo affascinante". + Esplora ulteriormente