Dalla scoperta degli inibitori della poli(ADP-ribosio) polimerasi (PARP) e dei loro notevoli risultati nel trattamento dei tumori mutanti BRCA1/2, la letalità sintetica (SL) nella terapia antitumorale ha attirato crescente attenzione. La SL è un fenomeno in cui un singolo evento genetico non è sufficiente per indurre la morte cellulare, ma più eventi genetici portano alla morte cellulare.
La caratterizzazione delle interazioni genetiche SL con mutazioni specifiche del tumore può essere utilizzata per sviluppare un quadro concettuale per affrontare bersagli "non resistenti" come il gene soppressore del tumore p53. Il cancro della cistifellea (GBC) è il tumore maligno più diffuso del sistema biliare ed è generalmente fatale a causa della limitata efficacia dei trattamenti esistenti.
È stato riportato che p53 è uno dei geni mutati più frequentemente e un indicatore prognostico sfavorevole nel GBC. Pertanto, una strategia basata su SL per prendere di mira il GBC con mutazione p53 è un approccio promettente.
Un nuovo studio su questo argomento condotto dal Prof. Mingyu Chen, dal Prof. Xiujun Cai, dal Dr. Shjie Li, dal Dr. Sarun Juengpanich e dal Dr. Win Topatana, da tutti gli ospedali Sir Run-Run Shaw, Università di Zhejiang e dal Prof. Jicheng Yu del College of Pharmaceutical Sciences, Zhejiang University appare nel Science Bulletin .
Studi precedenti hanno dimostrato che la riparazione del danno al DNA ottenuta da WEE1 attraverso la regolazione del checkpoint G2 del ciclo cellulare è essenziale per la sopravvivenza delle cellule mutate con p53. Pertanto, adavosertib (ADA), un inibitore WEE1, ha un significativo effetto letale sintetico sui tumori con mutazione di p53. Tuttavia, la resistenza ai farmaci dovuta ai percorsi di compensazione della risposta al danno del DNA (DDR) e l'elevata tossicità limitano ulteriori applicazioni.
Studi recenti hanno indicato che l’uso di fattori fisici come la terapia fotodinamica (PDT), la terapia sonodinamica (SDT) e la gasterapia nel trattamento dei tumori ha effetti superiori e una gamma di applicazioni più ampia rispetto ai farmaci chimici convenzionali. I fattori fisici che forniscono condizioni irreversibili per potenziare l'effetto letale sintetico dell'uccisione del tumore si riveleranno una strategia efficace.
Pertanto, sulla base della capacità della struttura MOF di realizzare varie condizioni aggiuntive durante la somministrazione di farmaci, questo nuovo studio ha selezionato MOF come strumento in combinazione con SDT per migliorare l'effetto letale sintetico tra WEE1 e p53 in GBC e ha ottenuto un risultato promettente.
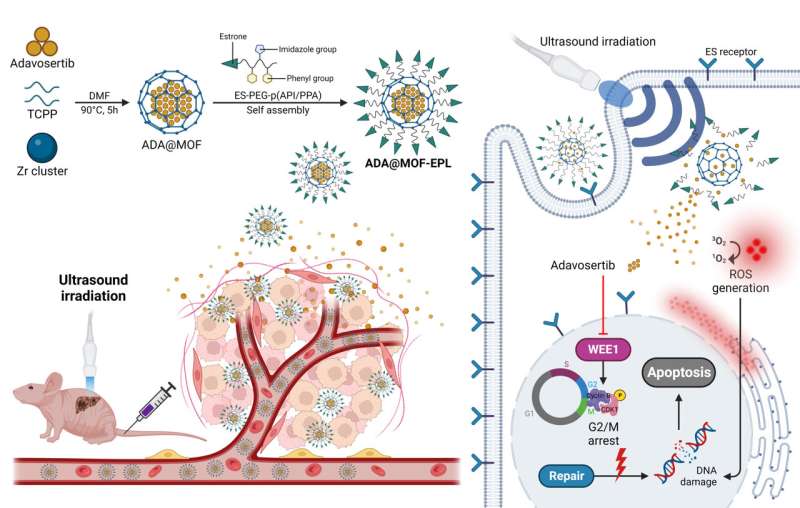
Nello specifico, una porfirina sonosensibile (tetrakis (4-carbossifenil) porfirina, TCPP) contenente Zr-MOF è stata utilizzata come struttura portante organica per la terapia sonodinamica (SDT), seguita dall'incapsulamento di ADA durante la sintesi MOF one-pot per aumentare il carico di ADA dei MOF (ADA@MOF). Inoltre, la superficie di ADA@MOF è stata rivestita con ligandi polimerici mirati all'estrone (EPL) sensibili al pH per fornire alle nanoparticelle una capacità di colpire il tumore (ADA@MOF-EPL).
A causa dell'elevata espressione del recettore degli estrogeni (ER) nel GBC, l'estrone funziona come un ligando che mira al tumore, consentendo alle nanoparticelle di entrare e accumularsi rapidamente e accuratamente vicino al nucleo cellulare. Entrando nel microambiente tumorale acido (TME), le interazioni ioniche indebolite tra ADA@MOF ed EPL allenteranno la sua struttura, portando al rilascio iniziale di ADA.
Successivamente, l'irradiazione con ultrasuoni (US) per stimolare il MOF contenente porfirina sonosensibile comporterà il rilascio accelerato di ADA e genererà ROS per danneggiare il DNA. Ciò causerà una maggiore sensibilità delle cellule tumorali con mutazione p53 all'ADA ed eviterà la resistenza ai farmaci a causa dei percorsi di compensazione DDR alla fonte.
Pertanto, l’effetto letale sintetico potenziato tra ADA e p53 attraverso una condizione aggiuntiva di SDT avrebbe una robusta capacità di uccidere il tumore. Inoltre, le nanoparticelle riducono notevolmente anche la reazione tossica del farmaco. Ancora più importante, questo nuovo studio offre una nuova prospettiva sull'uso di sistemi di somministrazione di farmaci basati su MOF nel trattamento di vari tumori refrattari tramite SL potenziato.
Ulteriori informazioni: Shijie Li et al, Strutture metallo-organiche incapsulate con Adavosertib per il trattamento del cancro della cistifellea con mutazione p53 tramite letalità sintetica, Science Bulletin (2024). DOI:10.1016/j.scib.2024.02.039
Fornito da Science China Press