I polimeri autoripieganti contenenti gadolinio che formano complessi di dimensioni nanometriche potrebbero essere la chiave per una migliore risonanza magnetica e la somministrazione di farmaci di prossima generazione, come dimostrato dagli scienziati della Tokyo Tech. Grazie alle loro piccole dimensioni, alla bassa tossicità e al buon accumulo e penetrazione del tumore, questi complessi rappresentano un passo avanti negli agenti di contrasto per la diagnosi del cancro, nonché nella radioterapia a cattura di neutroni.
La risonanza magnetica (MRI) è uno strumento diagnostico cruciale per il cancro, poiché consente di acquisire immagini dettagliate dei tessuti molli. Per visualizzare i tumori più chiaramente nelle scansioni MRI, i medici solitamente iniettano ai pazienti agenti di contrasto. Questi composti influenzano il modo in cui gli ioni idrogeno vicini rispondono agli impulsi a radiofrequenza utilizzati nella risonanza magnetica. Idealmente, gli agenti di contrasto dovrebbero accumularsi selettivamente nei tumori e aumentare il loro contrasto nella risonanza magnetica.
Tuttavia, nonostante i numerosi sforzi di ricerca, i tradizionali agenti di contrasto chelati di gadolinio (Gd) stanno raggiungendo i loro limiti di prestazione. In poche parole, ottenere una dose ottimale nella distribuzione dei chelati di Gd all'interno dei tumori, dei tessuti sani e del sangue si è rivelato difficile senza ricorrere a dosi eccessive di Gd.
In questo contesto, uno studio collaborativo condotto da un gruppo di ricerca del Tokyo Institute of Technology (Tokyo Tech), del National Institutes for Quantum Science and Technology (QST) e dell’Innovation Center of Nanomedicine (iCONM), guidato dal professore associato Yutaka Miura di Tokyo Tech, ha sviluppato con successo un nuovo agente di nanocontrasto (NCA) con prestazioni eccezionali grazie a un design molecolare innovativo. I loro risultati sono stati pubblicati su Advanced Science il 29 novembre.
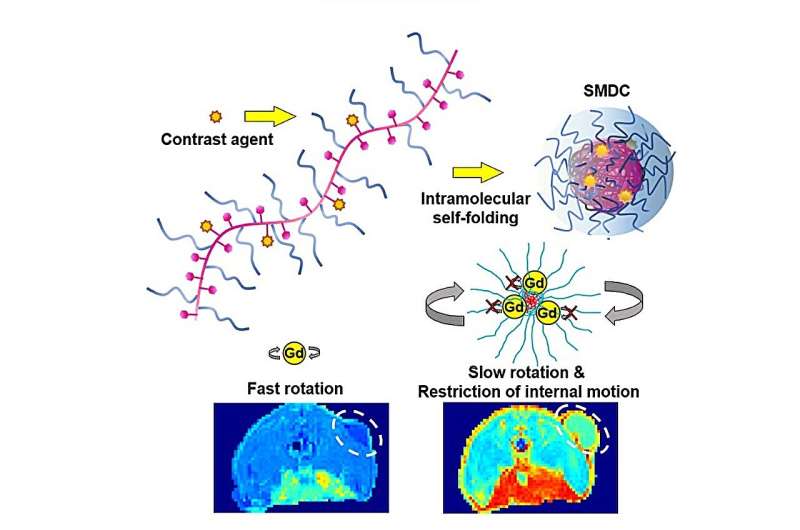
La proposta NCA si basa sull'uso di Gd come agente di contrasto in quello che i ricercatori hanno chiamato "trasporto di farmaci macromolecolari auto-pieganti (SMDC)". Hanno incorporato chelati contenenti Gd clinicamente approvati in una catena polimerica composta da poli(etilenglicole) metil etere acrilato (PEGA) e benzilacrilato (BZA). Poiché il polimero conteneva sia segmenti idrofili che idrofobi, si ripiegava rapidamente in una piccola forma a capsula quando veniva immerso in acqua, con i segmenti idrofobi al centro e i segmenti idrofili al guscio esterno.
Utilizzando questo approccio, i ricercatori potrebbero produrre molecole SMDC-Gds di diametro inferiore a 10 nanometri. Attraverso esperimenti su topi affetti da cancro al colon, hanno verificato che queste NCA non solo si accumulavano meglio nei tumori, ma venivano anche prontamente eliminate dal flusso sanguigno, portando a prestazioni di risonanza magnetica migliorate senza effetti tossici.
"L'elevato accumulo nel tumore e il rapido profilo di clearance ematica dell'SMDC-Gds consentono di aumentare i rapporti di accumulo del tumore rispetto agli organi principali e di ridurre al minimo la deposizione non necessaria di Gds", spiega il Prof. Miura.
Il team ha anche dimostrato un nuovo effetto che pone gli SMDC-Gd al di sopra dei chelati di Gd esistenti. Idealmente, il movimento degli ioni Gd dovrebbe essere minimo in modo che la loro influenza sugli ioni idrogeno vicini sia costante e prolungata. Nel disegno molecolare proposto, la struttura nucleo/guscio crea un ambiente molecolare "affollato" che sopprime non solo la rotazione, ma anche i movimenti segmentali e interni degli ioni Gd.
L'effetto risultante è un contrasto più forte nelle immagini MRI, che consentirà in futuro l'uso di elementi alternativi con profili più sicuri non solo nei pazienti ma anche nell'ambiente.
Vale la pena sottolineare che le applicazioni degli SMDC-Gds vanno oltre la risonanza magnetica. Questi composti possono essere utilizzati nella terapia con cattura di neutroni (NCT), una promettente tecnica di radioterapia mirata in cui i Gd catturano i neutroni e rilasciano radiazioni ad alta energia, uccidendo le cellule tumorali vicine.
Esperimenti sui topi hanno rivelato che l'NCT dopo ripetute iniezioni di SMDC-Gd ha portato a una notevole soppressione della crescita del tumore. Il team ritiene che la ragione di ciò sia l'accumulo selettivo e la profonda penetrazione di SMDC-Gd nei tessuti tumorali.
Nel complesso, gli sforzi collaborativi dei ricercatori per raggiungere questi risultati sottolineano il potenziale degli SMDC non solo per una migliore diagnostica MRI, ma anche come strumenti efficaci per il trattamento del cancro e di altre malattie.
"Questo studio presenta ulteriori possibilità per sfruttare la somministrazione di farmaci utilizzando vari carichi terapeutici e stiamo attualmente studiando lo sviluppo di tali sistemi SMDC", conclude il Prof. Miura.
Ulteriori informazioni: Shan Gao et al, Veicolo di farmaci macromolecolari ripiegabili per l'imaging e la terapia del cancro, Scienza avanzata (2023). DOI:10.1002/advs.202304171
Informazioni sul giornale: Scienza avanzata
Fornito dal Tokyo Institute of Technology