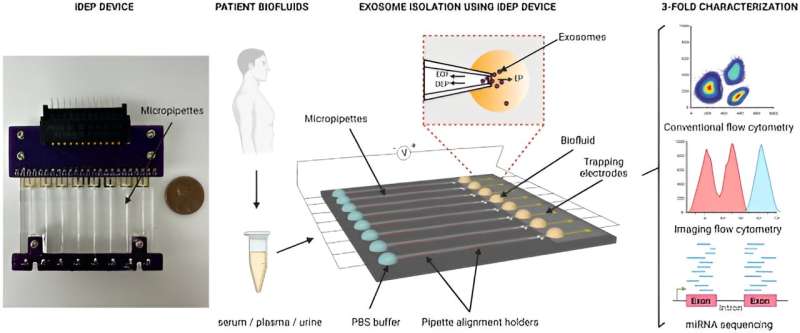
Tutte le cellule secernono vescicole extracellulari su scala nanometrica naturalmente come particelle delimitate da un doppio strato lipidico. Pertanto sono validi biomarcatori per identificare una varietà di malattie.
È importante isolare in modo efficiente le piccole vescicole extracellulari mantenendo la resa e la purezza per esplorarne il potenziale in applicazioni diagnostiche, prognostiche e terapeutiche.
I metodi convenzionali di isolamento presentano dei limiti, tra cui bassa purezza e resa, lunghe procedure di estrazione, attrezzature specializzate e costi elevati.
In uno studio pubblicato su Scientific Reports , Manju Sharma e un team di scienziati di ingegneria biomedica presso l'Università di Cincinnati, Ohio, Stati Uniti, hanno sviluppato un nuovo dispositivo dielettroforetico basato su isolanti per isolare rapidamente piccole vescicole extracellulari da biofluidi e terreni di coltura cellulare, in base alle loro proprietà dielettriche.
Gli scienziati hanno caratterizzato le piccole vescicole extracellulari isolate dai biofluidi dei pazienti affetti da cancro utilizzando lo strumento e hanno condotto una triplice caratterizzazione con citometria a flusso convenzionale, citometria a flusso con imaging avanzato e sequenziamento di microRNA per ottenere un'elevata resa di vescicole extracellulari pure. La piattaforma è efficiente nell'isolare rapidamente i biomarcatori e nel mantenere l'integrità biomolecolare delle vescicole.
Biologicamente, le piccole vescicole extracellulari sono vasi biologici incapsulati in membrana presenti nei biofluidi come sangue, urina, saliva, sperma, latte materno e liquido cerebrospinale; rilasciato dalle cellule nello spazio extracellulare.
Tali vescicole su scala nanometrica possono trasferire orizzontalmente il loro carico biomolecolare per funzionare come vettori di segnalazione intercellulare. Tali vescicole extracellulari forniscono un elevato grado di sensibilità e specificità grazie alla loro eccellente stabilità. La loro rilevazione precoce nelle biopsie liquide può migliorare l'individuazione di tumori, infezioni e malattie neurodegenerative e metaboliche.
L'isolamento delle vescicole è, tuttavia, impegnativo a causa delle loro dimensioni su scala nanometrica e delle proprietà fisico-chimiche. I metodi di isolamento dipendono tipicamente dalle proprietà delle vescicole extracellulari e, sebbene tali dispositivi abbiano caratteristiche promettenti, i costi di fabbricazione, la diluizione del campione e la suscettibilità all'intasamento rappresentano sfide intrinseche.
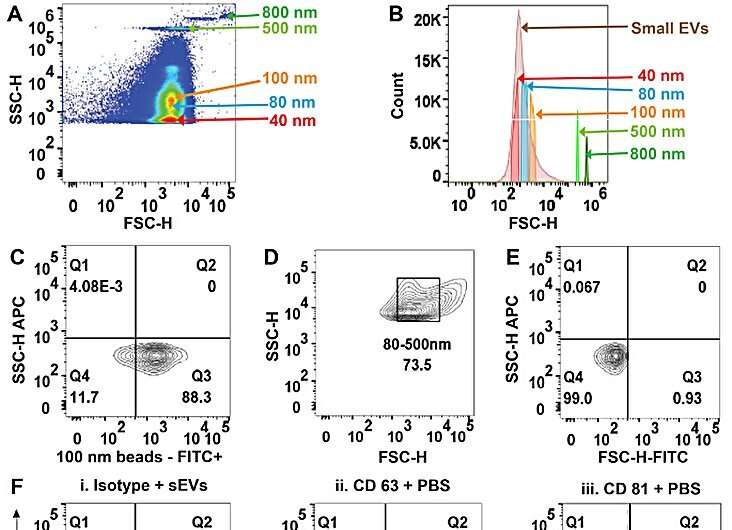
In risposta, Sharma e colleghi hanno sviluppato una classe di nuovi approcci dielettroforetici basati su isolanti con micropilastri in canali microfluidici per inghiottire rapidamente le nanoparticelle in base alle loro dimensioni e alle proprietà dielettriche uniche.
Il dispositivo mantiene una serie di micropipette in grado di isolare le nanoparticelle da piccoli volumi di campione applicando un campo elettrico significativamente basso su tutta la lunghezza delle pipette. L'architettura della geometria dei pori ha consentito l'isolamento di vescicole extracellulari da piccoli volumi di campioni di terreni di coltura cellulare condizionati e biofluidi da donatori sani.
In questo lavoro, Sharma e il team hanno isolato i biofluidi dei pazienti affetti da cancro, che includevano siero, plasma e urina, seguiti da caratterizzazione multiparametrica tramite citometria a flusso e sequenziamento di miRNA di nuova generazione.
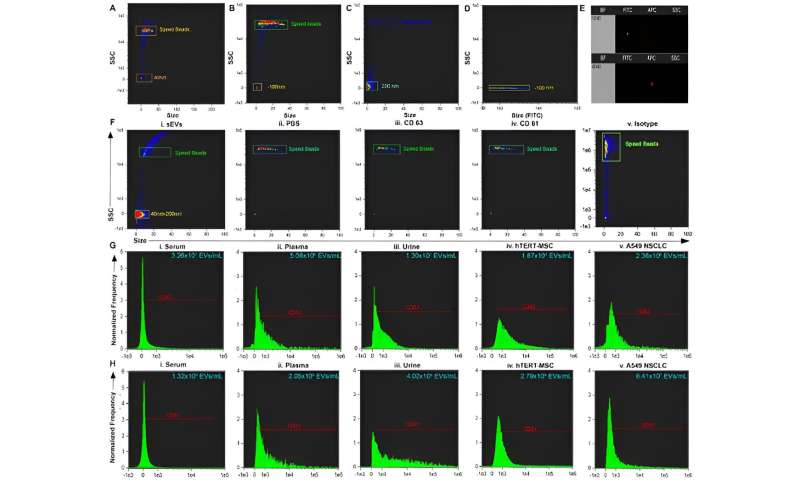
Il team ha purificato piccole vescicole extracellulari da siero, plasma e urina in soluzione salina tamponata con fosfato utilizzando l’approccio dielettroforetico basato su isolante. Sharma e colleghi hanno utilizzato la microscopia elettronica a trasmissione per confermare la presenza delle vescicole e hanno esplorato l'analisi multiparametrica di piccole vescicole extracellulari circolanti purificate tramite citometria a flusso.
Il team ha isolato le vescicole e le ha analizzate, seguite da studi di citometria a flusso convenzionali. I ricercatori hanno inoltre dimostrato la capacità e l'utilizzo del dispositivo caratterizzando gli isolati tramite il software ImageStream.
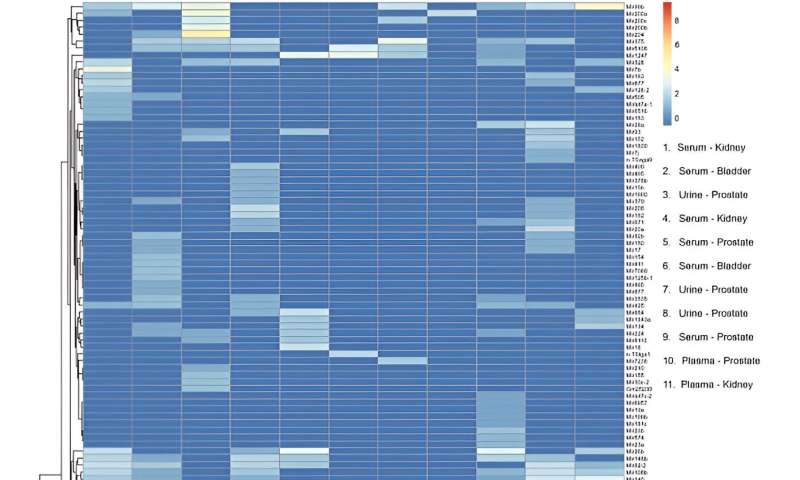
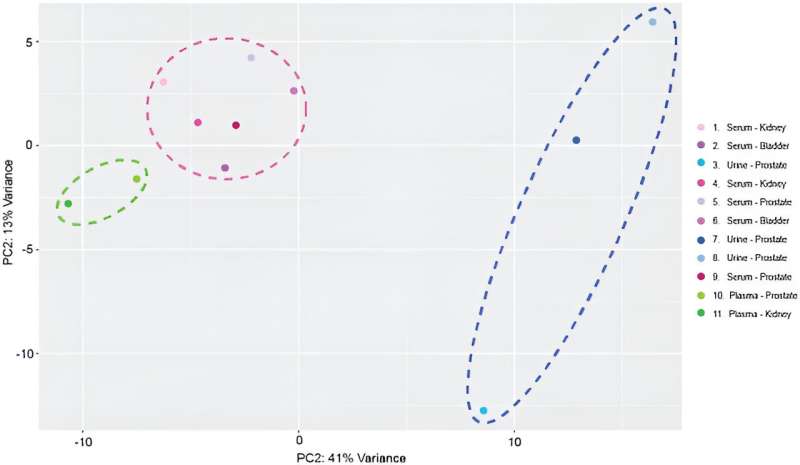
Dopo il sequenziamento dei miRNA, il team ha mappato 137 trascrizioni di miRNA distinte e mature nel genoma umano attraverso i campioni per includere il dispositivo nei flussi di lavoro di analisi dei biomarcatori di miRNA. Hanno condotto profili trascrittomici ed eseguito l'analisi delle componenti principali.
Prospettive
In questo modo, Manju Sharma e colleghi hanno dimostrato la capacità e l'efficienza di un dispositivo dielettroforetico basato su isolante privo di etichetta a bassa tensione per isolare piccole vescicole extracellulari da siero, plasma e urina di pazienti affetti da cancro attraverso il rilevamento di particelle submicroniche e caratterizzazione multiparametrica utilizzando la citometria a flusso convenzionale e metodi avanzati di citometria a flusso.
Le concentrazioni di RNA del lavoro erano paragonabili a lavori precedenti e hanno affermato che il metodo di isolamento è una valida alternativa a quelli già stabiliti in laboratorio. I metodi analitici possono essere utili come piattaforme di biopsia liquida per isolare piccole vescicole extracellulari e sviluppare piattaforme diagnostiche e di monitoraggio basate su vescicole extracellulari.
Ulteriori informazioni: Manju Sharma et al, Purificazione rapida e caratterizzazione multiparametrica di piccole vescicole extracellulari circolanti utilizzando un dispositivo lab-on-a-chip senza etichetta, Rapporti scientifici (2023). DOI:10.1038/s41598-023-45409-4
Informazioni sul giornale: Rapporti scientifici
© 2023 Rete Scienza X