Quando i Cavalieri Jedi devono sconfiggere un nemico, tirano fuori le loro fidate spade laser. In futuro, grazie ai ricercatori della Johns Hopkins, i medici che cercano di sconfiggere il cancro potrebbero brandire minuscole nanoSABRE molecolari che consentiranno loro di osservare i tumori in modi mai possibili prima.
Ispirato dal processo utilizzato dalle cellule per assemblare le proteine, un team guidato da due ricercatori:Ishan Barman della Whiting School of Engineering dell'università e Jeff W. Bulte, professore di radiologia e scienze radiologiche presso la School of Medicine, anch'egli affiliato alla JHU Institute for NanoBioTechnology – ha creato sonde infinitesimali che si illuminano quando incontrano alcuni enzimi presenti nelle cellule tumorali. La capacità di visualizzare i tumori nella loro interezza, e in fase iniziale, potrebbe migliorare significativamente l'imaging del cancro, informare le opzioni di trattamento e migliorare i risultati per i pazienti.
"Questo potrebbe essere un punto di svolta per il trattamento del cancro", ha detto Barman, professore associato di ingegneria meccanica presso la Whiting School, delle sonde autoassemblanti per il riconoscimento degli enzimi biortogonali (nanoSABER). I risultati del team vengono visualizzati in Advanced Science .
Attualmente, le biopsie tissutali rappresentano il gold standard per individuare la maggior parte dei tumori, anche se possono essere inesatte e addirittura trascurare parti del tumore in agguato ai margini. L'approccio del team della Johns Hopkins potrebbe risolvere questo problema, consentendo ai medici di visualizzare l'attività cancerosa su interi tumori, fornendo informazioni sulla loro possibile aggressività.
Gli enzimi, in particolare le legumi, svolgono un ruolo di primo piano nello sviluppo e nella progressione del cancro.
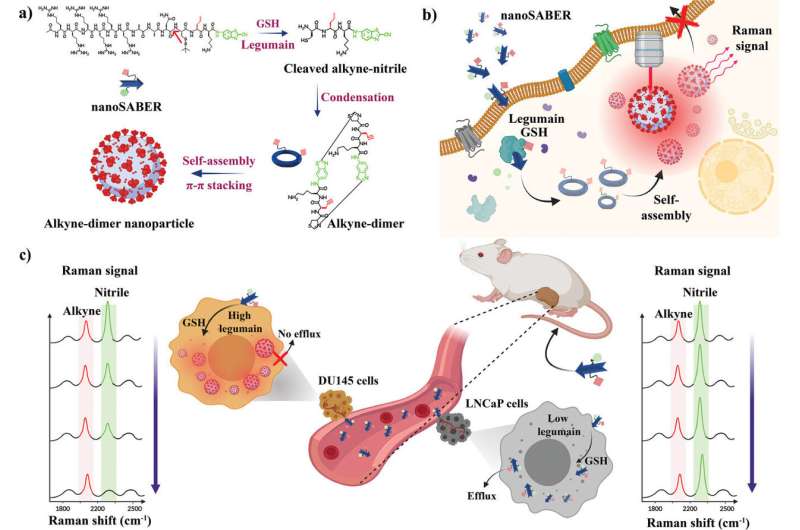
Il nuovo strumento del team si assembla in presenza di questi enzimi correlati al cancro ed emette un segnale che può poi essere captato dalla spettroscopia Raman, una tecnica di visualizzazione che analizza le vibrazioni molecolari per identificare e caratterizzare le sostanze. Ciò consente alle sonde di individuare con precisione le cellule tumorali.
Il team della Johns Hopkins afferma che il suo metodo potrebbe anche consentire ai medici di monitorare in modo più accurato l'accumulo di farmaci antitumorali nei tumori durante il trattamento, fornendo un'indicazione dell'efficacia di tali trattamenti.
"La capacità delle sonde di offrire uno sguardo chiaro ai livelli molecolari, cellulari e tissutali fornisce una prospettiva completa", ha affermato l'autore principale Swati Tanwar, un ricercatore post-dottorato in ingegneria meccanica. "È fondamentale capire cosa sta realmente accadendo ai margini del tumore per garantire la completa rimozione del cancro e ridurre al minimo le possibilità di recidiva."
I coautori dello studio della Johns Hopkins includono Behnaz Ghaemi, Piyush Raj, Aruna Singh, Lintong Wu, Dian R. Arifin e Michael T. McMahon. Del team faceva parte anche Yue Yuan dell'Università della Scienza e della Tecnologia della Cina.
Ulteriori informazioni: Swati Tanwar et al, Una nanosonda attiva Raman bioortogonale intracellulare autoassemblante intelligente per l'imaging tumorale mirato, Scienza avanzata (2023). DOI:10.1002/advs.202304164
Informazioni sul giornale: Scienza avanzata
Fornito dalla Johns Hopkins University