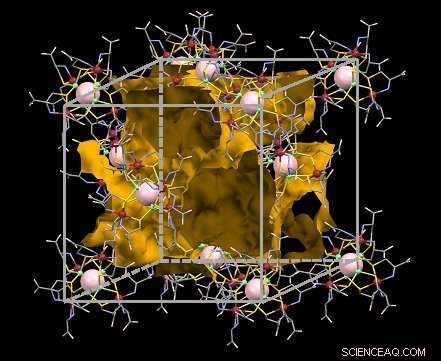
Figura 1:Struttura del cristallo ionico di nuova concezione. Il percorso in cui possono viaggiare gli ioni è evidenziato in giallo. Credito:Università di Osaka
Un gruppo di ricerca dell'Università di Osaka ha segnalato un nuovo progresso nella progettazione di materiali da utilizzare nelle batterie ricaricabili, in condizioni di elevata umidità. Usando l'ispirazione dalle cellule viventi che possono bloccare le particelle più piccole ma lasciano passare le particelle più grandi, i ricercatori sono stati in grado di creare un materiale con ioni potassio altamente mobili che possono migrare facilmente in risposta ai campi elettrici. Questo lavoro può aiutare a rendere le batterie ricaricabili abbastanza sicure ed economiche da ridurre drasticamente il costo delle auto elettriche e dell'elettronica di consumo portatile.
Le batterie ricaricabili agli ioni di litio sono ampiamente utilizzate nei laptop, telefono cellulare, e persino auto elettriche e ibride. Sfortunatamente, queste batterie sono costose, e sono anche noti per prendere fuoco occasionalmente. Nuovi materiali che non utilizzano il litio potrebbero ridurre i costi e migliorare la sicurezza di queste batterie, e hanno il potenziale per accelerare notevolmente l'adozione di auto elettriche ad alta efficienza energetica. Sia gli ioni sodio che potassio sono potenziali candidati che possono essere utilizzati per sostituire il litio, in quanto sono economici e in quantità elevata. Però, gli ioni sodio e potassio sono ioni molto più grandi del litio, quindi si muovono lentamente attraverso la maggior parte dei materiali. Questi ioni positivi sono ulteriormente rallentati dalle forti forze attrattive alle cariche negative nei materiali cristallini. "Gli ioni potassio possiedono una bassa mobilità allo stato solido a causa delle loro grandi dimensioni, che è uno svantaggio per la costruzione di batterie, " spiega l'autore corrispondente Takumi Konno.
Risolvere questo problema, i ricercatori hanno utilizzato lo stesso meccanismo impiegato dalle cellule per consentire ai grandi ioni di potassio di passare attraverso le loro membrane, tenendo contemporaneamente fuori le particelle più piccole. I sistemi viventi raggiungono questa impresa apparentemente impossibile considerando non solo gli ioni stessi, ma anche le molecole d'acqua circostanti, chiamato "strato di idratazione, " che sono attratti dalla carica positiva dello ione. Infatti, più piccolo è lo ione, più grande e più strettamente legato sarà il suo strato di idratazione associato. I canali specializzati del potassio nelle membrane cellulari hanno le dimensioni giuste per consentire il passaggio degli ioni di potassio idratati, ma bloccano i grandi strati di idratazione degli ioni più piccoli.

Figura 2:Conducibilità del litio (Li+, rosso), sodio (Na+, verde), e potassio (K+, blu) ioni all'interno del cristallo a diverse temperature. Le conducibilità aumentano anche all'aumentare delle dimensioni degli ioni. Credito:Università di Osaka
I ricercatori hanno sviluppato un cristallo ionico utilizzando rodio, zinco, e atomi di ossigeno. Proprio come con i canali biologici selettivi, la mobilità degli ioni nel cristallo è risultata maggiore per gli ioni potassio più grandi, rispetto agli ioni di litio più piccoli. Infatti, gli ioni di potassio si muovevano così facilmente, il cristallo è stato classificato come "conduttore superionico". I ricercatori hanno scoperto che il materiale attuale aveva la più grande mobilità di ioni potassio idrato mai vista fino ad oggi.
"Sorprendentemente, il cristallo ha mostrato una conduttività ionica particolarmente elevata a causa della rapida migrazione degli ioni potassio idrati nel reticolo cristallino", afferma l'autore principale Nobuto Yoshinari. "Tale conduttività superionica degli ioni potassio idrati allo stato solido non ha precedenti, e può portare a batterie ricaricabili più sicure ed economiche."