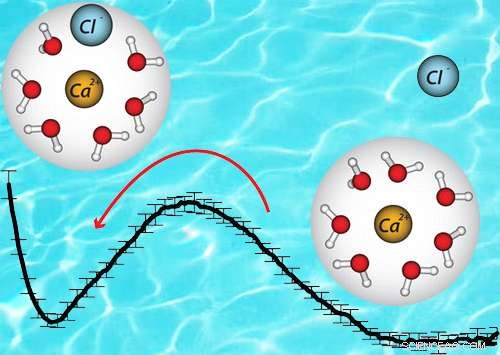
L'energia libera è diversa tra la coppia ionica (sinistra) e lo ione solo (destra). Non era possibile vedere questa differenza con gli approcci precedenti. Credito:American Chemical Society
Dalle batterie alla biologia, i liquidi contenenti sale sono vitali per la continuità delle prestazioni. La comprensione accurata del comportamento di questi liquidi si basa sulla corretta rappresentazione delle strutture molecolari che formano. Dott. Marcel Baer, Dottor Timothy Duignan, e il Dr. Christopher Mundy del Pacific Northwest National Laboratory hanno determinato che la struttura precisa di una coppia di ioni isolati in acqua riporta accuratamente come si comporterà un'intera soluzione.
"Questa accurata struttura locale è il pezzo importante nel mettere in relazione il microscopico con il macroscopico, o proprietà intrinseche degli ioni in soluzione a proprietà collettive, " ha detto Mundy, che ha condotto gli studi al PNNL.
Integrando calcoli ed esperimenti intorno a due ioni che formano una coppia ionica di sale, il team può comprendere la natura collettiva della soluzione. Vale a dire, il team può comprendere le statistiche di raggruppamento in relazione al comportamento specifico degli ioni a diverse concentrazioni, che viene misurato dal coefficiente osmotico. Nello specifico, l'elettrolita si forma in cluster o rimane come ioni isolati a diverse concentrazioni?
Il comportamento e la speciazione degli elettroliti influenzano tutto, dal loro uso come elettroliti di batterie al loro comportamento nelle scorie nucleari complesse. Comprendendo come le proprietà individuali degli ioni informano il loro comportamento collettivo, gli scienziati possono determinare come adattare la concentrazione e il tipo di elettrolita per applicazioni specifiche.
Il team ha esaminato come la corretta struttura molecolare influenzi la termodinamica della soluzione. Hanno determinato la struttura attraverso misurazioni estese della struttura fine dell'assorbimento di raggi X e simulazioni molecolari basate sulla meccanica quantistica. Il lavoro del team dimostra che è possibile prevedere il grado in cui gli ioni sono accoppiati in soluzione (chiamata attività) utilizzando descrizioni accurate dello ione-acqua locale, e interazioni ione-ione.
In un contestuale articolo di revisione su invito con il Dr. Tim Duignan, il team ha dimostrato come ottenere l'abbinamento giusto con calcoli di alto livello. I risultati forniscono i dettagli molecolari necessari per migliorare le teorie macroscopiche della solvatazione ionica.