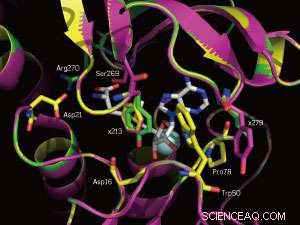
Un primo piano dei siti di legame SAM dell'enzima nativo (giallo) e di due mutanti (magenta e verde). Le posizioni mutate 213 e 279 sono etichettate. Credito:WILEY-VCH Verlag GmbH &Co. KGaA, Weinheim
Le molecole organiche contenenti un atomo di fluoro sono ampiamente utilizzate nei materiali, industrie agrochimiche e farmaceutiche. Però, la sintesi del legame carbonio-fluoro utilizza tipicamente catalizzatori metallici tossici e richiede condizioni anidre e temperature elevate. Ora un team internazionale ha sviluppato un più mite, approccio più efficiente basato su enzimi per creare questo legame.
Questo metodo enzimatico funziona in condizioni acquose ea temperature miti ed è stato sviluppato da un consorzio che includeva ricercatori di A*STAR e altre istituzioni. "Queste condizioni sono davvero molto allettanti, " spiega il membro del team Yee Hwee Lim dell'A*STAR Institute of Chemical and Engineering Sciences.
Il team ha utilizzato uno degli enzimi fluorinasi altamente specifici che si trovano in natura:FlA1. Questi enzimi catalizzano la formazione di un legame carbonio-fluoro nella S-adenosilmetionina (SAM) utilizzando fluoruro inorganico tramite un meccanismo di sostituzione.
L'enzima, pur essendo eccellente nel catalizzare le reazioni di fluorurazione con questa molecola naturale, non ha funzionato bene su molecole non naturali. Inoltre, sforzi per modificare le strutture degli enzimi e, così, la funzione era stata una lotta, fino ad ora.
"Abbiamo dimostrato per la prima volta che l'enzima fluorinasi può essere ingegnerizzato, e che l'ingegneria può migliorare la sua attività enzimatica anche su molecole non naturali, "dice Lime.
Il team ha utilizzato la tecnica consolidata nota come "evoluzione diretta" che imita la selezione naturale per far evolvere gli enzimi in modo che possano reagire bene con molecole non naturali.
"L'evoluzione diretta non è mai stata applicata con successo a questo enzima, fino ad ora, " dice Lim. "Questo è un enzima difficile con cui lavorare e abbiamo affrontato molte sfide, inclusi problemi con il degrado del prodotto".
Il team ha utilizzato la marcatura radioattiva della 5'-cloro-5'-deossiadenosina (5'-CIDA) per mostrare le proprie capacità. In questa reazione in due fasi, 5'-CIDA radiomarcato viene convertito in SAM, e poi fluorurato per formare 5'-fluoro-5'-deossiadenosina (5'-FDA). Questo prodotto etichettato 5'-FDA potrebbe essere potenzialmente utilizzato per una procedura di diagnosi medica nota come tomografia a emissione di positroni (PET).
"Mostriamo che il triplice miglioramento dell'attività di un enzima può aprire più applicazioni, " dice Lim. "Gli enzimi nativi sono stati usati in precedenza per cercare di etichettare gli agenti PET ma i tempi di reazione erano lunghi, a volte ore. Usando il nostro enzima potremmo fare la reazione in 30 minuti, una tempistica più ragionevole dato che l'emivita di Fluorine-18 è inferiore a due ore."
Il team di Lim sta ora esplorando come la mutazione della struttura dell'enzima modifica la sua interazione con 5'-CIDA e SAM. "Vorrei coinvolgere i biologi computazionali per capire meglio le mutazioni che abbiamo fatto e come queste sono correlate alle nostre reazioni".