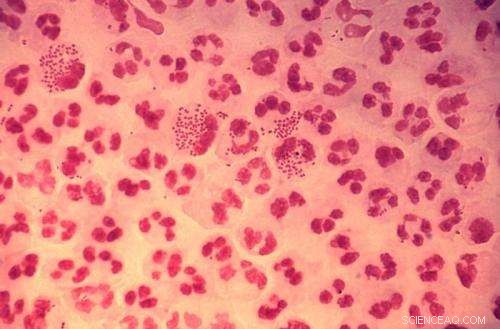
Credito:CDC
I ricercatori stanno aprendo la strada a un nuovo approccio terapeutico per la gonorrea facendo luce sul meccanismo alla base di importanti proteine sulla membrana esterna del batterio Neisseria gonorrhoeae.
Le terapie future potrebbero presentarsi sotto forma di nuovi antibiotici o, anche meglio, un vaccino.
I risultati sono particolarmente importanti in quanto la Neisseria gonorrhoeae è considerata un "superbatterio" a causa della sua resistenza a tutte le classi di antibiotici disponibili per il trattamento delle infezioni.
Gonorrea, una malattia a trasmissione sessuale il cui numero cresce di 78 milioni di nuovi casi in tutto il mondo ogni anno, è altamente dannoso per la salute riproduttiva e neonatale se non trattata o trattata in modo improprio.
Può portare a endometrite, Malattia infiammatoria pelvica, gravidanza extrauterina, epididimite e infertilità. I bambini nati da madri infette sono a maggior rischio di cecità.
La ricerca condotta dagli autori corrispondenti Aleksandra Sikora della Oregon State University e Nicholas Noinaj della Purdue University fornisce informazioni strutturali e funzionali chiave su un complesso proteico multicomponente noto come BAM, abbreviazione di macchine di assemblaggio beta-barile.
Nei batteri Gram-negativi, BAM è responsabile della biogenesi delle proteine beta-barile sulle membrane esterne delle cellule.
Le proteine della membrana esterna hanno funzioni fisiologiche e strutturali cruciali, tra cui l'acquisizione di nutrienti, secrezione, trasduzione del segnale, biogenesi della membrana esterna, e motilità. Nei batteri patogeni, quelle proteine portano anche alla colonizzazione dell'ospite e possono sfruttare le risposte immunitarie, facilitando la virulenza.
BamA è il componente principale del macchinario di assemblaggio beta-barile, e questo studio ha preso in considerazione altri due componenti, BamD e BamE.
I ricercatori hanno scoperto che in N. gonorrhoeae, BamE è esposto sulla superficie cellulare ma non è essenziale per la vitalità cellulare. Al contrario, BamD aveva i tratti opposti:non superficie visualizzata, ma essenziale per la fattibilità.
Però, quando BamE è stato eliminato negli esperimenti, BamD si è spostato in superficie.
"La perdita di BamE ha alterato la composizione dell'involucro cellulare e ha portato a una crescita cellulare più lenta, " disse Sikora, professore associato presso l'OSU College of Pharmacy. "Ha anche portato ad un aumento sia della suscettibilità agli antibiotici sia alla formazione di vescicole di membrana contenenti maggiori quantità di antigeni del vaccino".
Sikora ha notato che sia BamD che BamE sono espressi in diversi isolati gonococcici e durante diverse fasi di crescita.
"Le strutture risolte di Neisseria BamD e BamE condividono le pieghe complessive con le proteine di E. coli, ma ci sono anche differenze che possono essere importanti per la funzione, " ha detto. "Quindi, anche se il BAM è conservato tra i batteri Gram-negativi, ci sono differenze strutturali e funzionali da specie a specie che possono essere probabilmente sfruttate nello sviluppo di terapie specifiche per specie per combattere la resistenza multifarmaco».
Per esempio, nell'E. coli, BamE non è esposto in superficie; anche, l'assenza di BamE in E. coli non porta BamD a essere visualizzato sulla membrana esterna.
"Questa è un'ulteriore prova che BamE potrebbe essere un nuovo bersaglio del vaccino contro N. gonorrhoeae, " Ha detto Sikora. "Abbiamo fatto un sacco di biologia così come la risoluzione di strutture che ci danno gli strumenti per abilitare nuove terapie. Nella battaglia contro la multiresistenza, il modo ideale per prevenire le malattie è un vaccino, e avere una struttura di BamE apre le porte a un approccio strutturale alla vaccinologia".
I risultati sono stati pubblicati nel Journal of Biological Chemistry .