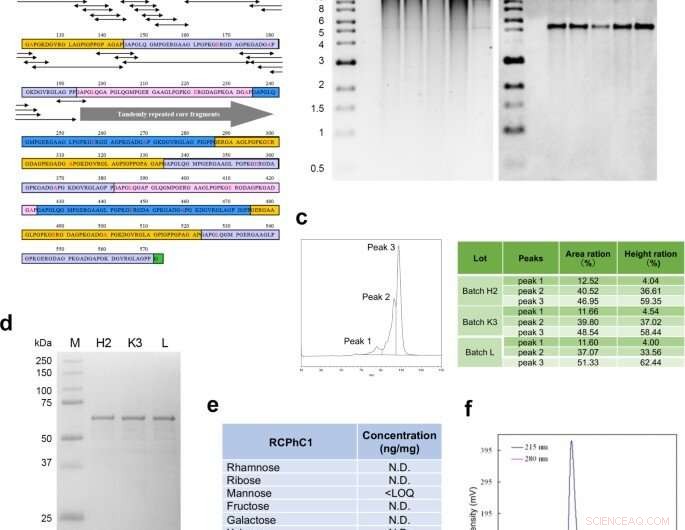
Progettazione molecolare e sintesi del polipeptide ricombinante RCPhC1. (a) La sequenza peptidica di RCPhC1 mostra ripetizioni Gly-Xaa-Yaa con sostituzioni di amminoacidi (rosso). Tutti i frammenti peptidici (sequenze penta minime) contenenti le sostituzioni di amminoacidi (frecce a doppia testa) sono stati abbinati a sequenze di collagene umano. (b) Stabilità del DNA genomico nella banca di cellule di lavoro. Dopo ciascuna delle quattro frammentazioni consecutive, il DNA genomico è stato isolato (corsie 1-4) e confrontato con il DNA genomico originale (corsia 5). Il pannello di destra, Southern blot ibridato con la sonda del promotore AOX1. (c) La riproducibilità è stata analizzata mediante cromatografia liquida. Il profilo a fase inversa ha mostrato tre picchi, che sono stati costantemente identificati in tre diversi lotti (H2, K3, e io). (d) La riproducibilità è stata valutata anche da SDA-PAGE. La singola banda di tre diversi lotti ha suggerito anche l'assenza di modifiche post-traduzionali. (e) L'assenza di glicosilazione post-traduzionale. (f) La cromatografia a permeazione di gel ha confermato l'elevata purezza di RCPhC1. Credito:Materiali di comunicazione sulla natura, doi:10.1038/s43246-020-00089-9
L'attuale gold standard per la chirurgia degli innesti ossei include autoinnesti e alloinnesti, sebbene esista una crescente domanda di sviluppo di biomateriali sintetici per una migliore biointegrazione nell'ingegneria del tessuto osseo. In un nuovo rapporto ora pubblicato su Materiali di comunicazione sulla natura , Hideo Fushimi e un team di ricerca in bioscienze e ingegneria, e biotecnologia ricostruttiva in Giappone e negli Stati Uniti, ha sviluppato un materiale per impalcatura biodegradabile utilizzando proteine ricombinanti o polipeptidi come fonte di materiali di innesto a base di idrogel. Il team ha utilizzato la catena alfa 1 del collagene di tipo I umano (abbreviato RCPhC1) come fonte per sviluppare il polipeptide ricombinante e ha dimostrato la flessibilità del materiale per progettare le caratteristiche ideali per gli innesti ossei. Il team ha anche sviluppato innesti ossei RCPhC1 utilizzando un sistema altamente scalabile, protocollo di produzione semplificato per la generazione robusta di tessuto osseo maturo in laboratorio. L'innesto osseo è stato completamente riassorbito dopo la rigenerazione dei tessuti in un modello animale preclinico per un'efficace integrazione biologica.
Ingegneria del tessuto osseo con biomimetica, innesti ossei sintetici
In questo lavoro, Fushimi et al. ha sviluppato un materiale da innesto osseo sintetico utilizzando una proteina ricombinante abbreviata RCPhC1. Lo sviluppo fornisce un materiale di partenza versatile per la produzione di innesti ossei sintetici tramite ingegneria flessibile. Utilizzando studi preclinici su modelli di difetti ossei di cani e roditori, il team ha mostrato una migliore efficienza degli innesti ossei per rigenerare il tessuto osseo con maturità strutturale. In clinica ortopedica, la perdita di volume e funzione dei tessuti è un segno distintivo di lesione, infiammazione cronica, e malattie metaboliche e genetiche. Mentre il tessuto osseo può rigenerarsi attivamente attraverso la proliferazione e la differenziazione osteogenica delle cellule mesenchimali stromali o staminali, grandi difetti ossei richiedono interventi chirurgici per riparare e ricostruire le ossa con materiali da innesto osseo.
Globalmente, I chirurghi ortopedici eseguono annualmente circa 2,2 milioni di procedure di innesto osseo in un mercato globale estremamente costoso. Il tessuto osseo umano è composto da matrice extracellulare organica, minerali di calcio e fosforo cristallizzati che formano idrossiapatite. I materiali per innesto osseo possono imitare la struttura e la composizione biochimica del tessuto osseo. Chirurghi e ricercatori ortopedici hanno utilizzato innesti ossei autologhi (cellule e tessuto ottenuti dallo stesso individuo) per riparare difetti ossei dovuti a problemi minerali e immunologici, anche se le complicazioni nei siti dell'intervento possono portare a metodi di innesto alternativi come gli allotrapianti (cellule e tessuti ottenuti da un individuo diverso). Il nuovo sviluppo della biomimetica, i biomateriali sintetici per l'ingegneria del tessuto osseo rispondono a un'urgente necessità nel settore sanitario di sviluppare nuovi materiali da innesto senza utilizzare tessuti umani o animali.
Fattori di controllo ingegneristici per lo sviluppo di strutture di ghiaccio isotropico mediante colata di congelamento a strato sottile (TLFC). (a) Schema dell'apparato di colata a freddo. (b) Misurazione tipica della temperatura del fondo della coppa di raffreddamento (blu) e della superficie del soluto (rosso) durante il processo di colata a freddo. C'era una discrepanza significativa tra la tazza di raffreddamento e la superficie del soluto durante il periodo di congelamento. (c) Schema della struttura anisotropica del modello di ghiaccio e dell'effettiva microstruttura RCPhC1 contenente la zona dei piccoli pori. La barra della scala è uguale a 500 μm. d TLFC ha ridotto la discrepanza di temperatura tra la tazza di raffreddamento (blu) e la superficie del soluto (rossa) durante il periodo di congelamento. (e) L'effetto della temperatura minima e della durata del raffreddamento sulla struttura isotropa dei pori interni. La struttura dei pori uniforme (blu) si è sviluppata quando la temperatura minima era inferiore a -10 °C ma non è stata influenzata dalla durata del raffreddamento. La struttura irregolare dei pori interni (rosso) si è sviluppata più frequentemente quando la temperatura minima era superiore a -10 °C. La barra della scala è uguale a 500 μm. L'area verde mostra i conteggi delle torte liofilizzate uniformemente. L'area rossa mostra i conteggi delle torte liofilizzate in modo irregolare. (f) L'effetto della temperatura del blocco sulla dimensione dei pori interni. I diamanti mostrano valori medi. Le temperature del blocco più basse hanno aumentato il numero di piccoli pori. La barra della scala è uguale a 500 μm. (g) La struttura interna sviluppata dall'agitazione (cerchi rossi), i metodi di colata a freddo anisotropico (cerchi verdi) e isotropi (cerchi blu) sono stati valutati mediante analisi di assorbimento d'acqua e decomposizione acida. Le spugne RCPhC1 sono state provvisoriamente reticolate deidrotermiche a 130°C per 7 h. Le linee blu nei pannelli b e d indicano la registrazione della temperatura dalla termocoppia sul fondo delle soluzioni. Le linee rosse indicano che sulla superficie della soluzione. Credito:Materiali di comunicazione sulla natura, doi:10.1038/s43246-020-00089-9 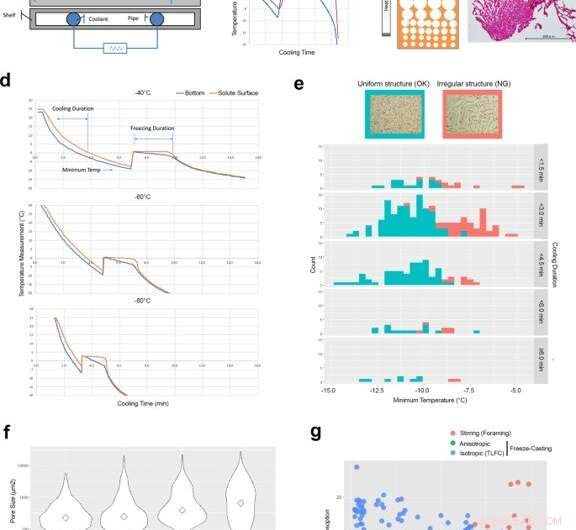
Il team ha utilizzato collagene di tipo I, abbondantemente espresso nei tessuti connettivi e nelle membrane interstiziali come principale componente organico del tessuto osseo. La sequenza proteica del collagene di tipo I svolge un ruolo importante nello stabilire la resistenza meccanica dell'osso. Il team ha prima clonato il DNA complementare (cDNA), una copia di DNA di una molecola di RNA messaggero (mRNA) che codifica per il polipeptide (sequenza proteica) RCPhC1, in un vettore di espressione. Per realizzare questo, hanno usato una specie di lievito metilotrofico nota come Pichia pastoris per trasferire la sequenza e generare banche di cellule master e di lavoro. Il team ha confermato la composizione in amminoacidi del polipeptide sintetico e ha caratterizzato ampiamente il prodotto.
Hanno quindi progettato la struttura interna del materiale di innesto per soddisfare i requisiti specifici del tessuto bersaglio. Per generare una struttura porosa uniforme, perciò, Fushimi et al. progettato un protocollo TLFC (thin-layer freeze casting). L'approccio versatile del congelamento ha generato un gran numero di pori con pareti sottili per formare un'impalcatura RCPhC1 isotropa con varie strutture interne.
Fattori ingegneristici che influenzano la reticolazione deidrotermica di RCPhC1 per controllare il tasso di biodegradazione e la resistenza meccanica. (a) L'effetto della temperatura di reticolazione e della durata della reticolazione sulla velocità di biodegradazione valutata mediante analisi di decomposizione acida in vitro. (b) La temperatura di reticolazione non ha influenzato linearmente il tasso di sopravvivenza alla decomposizione acida. Considerando la sterilizzazione a valle, la temperatura di reticolazione è stata fissata a 130°C. (c) La durata della reticolazione è risultata essere il fattore di controllo predominante, che ha aumentato linearmente il tasso di sopravvivenza alla decomposizione acida di RCPhC1 fino a 10 h. Il materiale di gelatina suina ha risposto in modo simile alla durata della reticolazione, pur richiedendo una durata molto più lunga. (d) Proprietà fisica di RCPhC1 reticolato deidrotermico. La proprietà fisica equivalente della gelatina suina reticolata deidrotermica richiedeva una durata della reticolazione 10 volte maggiore. (e) La resistenza meccanica di RCPhC1 reticolato deidrotermico (130 °C, 7 h) era significativamente superiore a quella della gelatina suina reticolata deidrotermica (130 °C, 72 h). La barra di errore rappresenta s.d. (f) RCPhC1 reticolato deidrotermico (130 °C, 7 h) è stato trattato con tripsina e sottoposto a LC ad alte prestazioni. La co-migrazione dei frammenti peptidici indicava più siti di reticolazione. Credito:Materiali di comunicazione sulla natura, doi:10.1038/s43246-020-00089-9 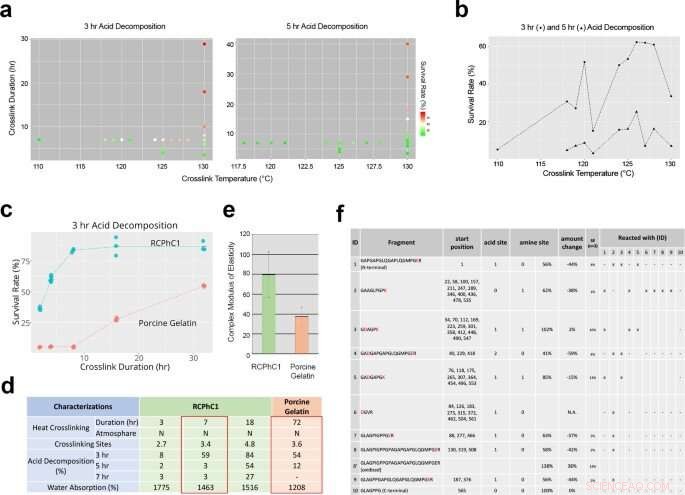
Fushimi et al. successivamente sottoposto il materiale a trattamento di reticolazione deidrotermica per testare l'effetto della temperatura e della durata di reticolazione sulla sua composizione. Dopo aver testato il prodotto a valle per la contaminazione microbica, la temperatura durante il processo di fabbricazione è stata confermata efficace per la sterilizzazione a calore secco. Ulteriori test hanno mostrato come la composizione amminoacidica unica della proteina ricombinante abbia contribuito alla sua robusta efficienza di reticolazione idrotermale. Il team ha poi ottimizzato il materiale proteico ricombinante per l'innesto osseo regolando la concentrazione del materiale polipeptidico e la sua temperatura di congelamento in base al volume dell'osso indotto dall'innesto in un modello di difetto osseo cranico (cranio) di ratto. Quattro settimane dopo l'innesto del materiale nel modello animale, il team ha utilizzato la stima del volume osseo basata sulla microtomografia computerizzata (microTC). I risultati hanno indicato una concentrazione ottimale del 7,5% RCPhC1, una temperatura di congelamento da -40 a -60 gradi Celsius, e la reticolazione deidrotermica a 130 ° C per 7 ore per essere più adatta alla produzione di materiale per innesto osseo ricombinante.
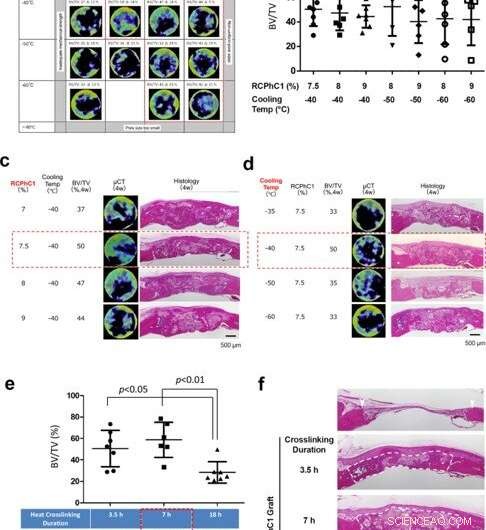
Ottimizzazione dei fattori di controllo ingegneristico. (a) Ottimizzazione dei fattori combinati della concentrazione del soluto RCPhC1 e della temperatura del blocco TLFC, con il tentativo di reticolazione deidrotermica a 130°C per 7 h. L'intervallo ottimale è stato ristretto alla concentrazione di RCPhC1 tra il 7,5 e il 9% e la temperatura del blocco TLFC tra -40 e -60 °C (blocco punteggiato di rosso). (b) misurazioni BV/TV all'interno del gruppo dell'intervallo ottimale di concentrazione di RCP1C1 e temperatura di raffreddamento. Non c'era alcuna differenza statistica tra i gruppi. (c) L'effetto della concentrazione di soluto RCPhC1 sulla rigenerazione ossea. La barra della scala è uguale a 500 μm. (d) L'effetto della temperatura del blocco TLFC sulla rigenerazione ossea. La barra della scala è uguale a 500 μm. (e) L'effetto della durata della reticolazione deidrotermica sulla formazione ossea. (n = 7; test di confronto multiplo di Tukey) (f). L'effetto della durata della reticolazione deidrotermica sul mantenimento dello spazio di guarigione della ferita nel difetto osseo cranico di ratto. Le punte di freccia bianche mostrano i bordi difettosi. Le linee tratteggiate bianche circondano il tessuto appena formato. La barra della scala è uguale a 500 μm. Linee orizzontali in b, ed e rappresenta la media ± s.d. Credito:Materiali di comunicazione sulla natura, doi:10.1038/s43246-020-00089-9
Rigenerazione robusta del tessuto osseo vitale in modelli preclinici con materiali da innesto
Sulla base delle condizioni ottimali verificate sperimentalmente, Fushimi et al. prodotto gli innesti ossei RCPhC1 con granuli porosi. Utilizzando il modello di difetto osseo cranico di ratto, hanno mostrato come l'innesto osseo inducesse in modo robusto la rigenerazione ossea all'interno della struttura dei pori interni, mentre si degrada gradualmente in vivo, per indicare biocompatibilità e biointegrazione efficace. Hanno confrontato questo risultato con uno xenotrapianto di osso spongioso decellularizzato di bovino (mucca) disponibile in commercio e non hanno osservato una rigenerazione ossea significativamente maggiore. Il team ha quindi testato il materiale dell'innesto osseo in un modello preclinico canino di estrazione del dente per comprendere la guarigione delle ferite nell'alveolo del dente, dove l'alveolo estrattivo trattato con l'innesto osseo ha mostrato una migliore formazione ossea a 12 settimane. Ormai, come previsto, l'innesto osseo è stato in gran parte sostituito da tessuto osseo.
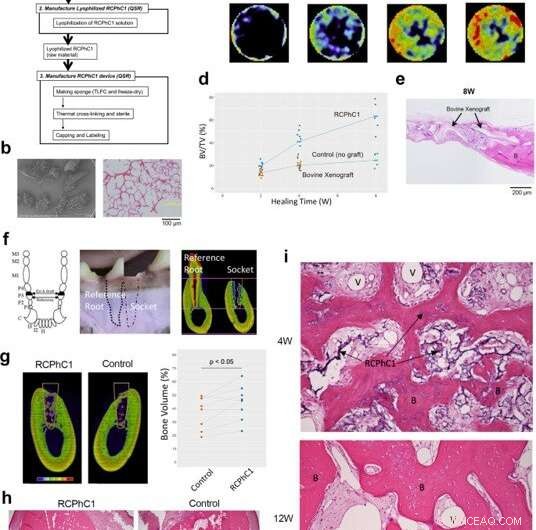
Test di efficacia preclinica del materiale RCPhC1 ottimizzato per l'innesto osseo in modelli di roditori e canini. (a) Diagramma di flusso del processo di fabbricazione dell'innesto osseo RCPhC1. La barra della scala è uguale a 100 μm. (b) L'innesto osseo RCPhC1 è stato preparato come granuli porosi di dimensioni 300-1200 µm per una migliore manipolazione. La barra della scala è uguale a 100 μm. (c) Andamento temporale della rigenerazione ossea indotta dall'innesto osseo RCPhC1 nel modello di difetto cranico di ratto. L'analisi istologica (riga superiore) ha rivelato tessuto osseo neoformato (B) all'interno del materiale da innesto RCPhC1, che si è riassorbito nel tempo. Una serie temporale di microCT in vivo (riga inferiore) ha mostrato il progressivo aumento del tessuto osseo. (d) Andamento temporale della misurazione BV/TV del difetto osseo cranico di ratto impiantato con innesto osseo RCPhC1, xenotrapianto di osso spongioso decellularizzato bovino e nessun controllo dell'innesto. (e) Valutazione istologica di xenotrapianto bovino impiantato in difetto osseo cranico di ratto. La struttura fisica dello xenotrapianto bovino era simile a quella dell'innesto osseo RCPhC1. Alla periferia del difetto, xenotrapianto bovino è stato visto fuso con l'osso neoformato (B). Al centro del difetto, granuli di xenotrapianto bovino erano circondati da tessuto fibroso. La barra della scala è uguale a 200 μm. (f) Modello di estrazione del dente canino. Il terzo premolare canino (P3) ha radici mesiali e distali quasi identiche. Il terzo premolare è stato emisezionato ed è stata estratta solo la radice distale. Un lato dell'alveolo osseo post-estrattivo è stato riempito con RCPhC1 mentre l'altro lato è stato lasciato guarire senza ulteriori trattamenti. La restante radice mediale è stata trattata endodonticamente e servita come riferimento. La barra della scala è uguale a 4 mm. (g) Sezione trasversale MicroCT raffigurante la rigenerazione ossea nell'alveolo estrattivo (linea bianca) dopo 12 settimane (12 W) di guarigione. Il volume osseo all'interno dell'alveolo era significativamente maggiore nell'alveolo impiantato con innesto osseo RCPhC1 rispetto all'alveolo di controllo non trattato (n = 8; t-test accoppiato a due lati). La barra della scala è uguale a 4 mm. (h) Sezione trasversale istologica dell'alveolo estrattivo (linea bianca) a 12 W. L'alveolo che ha ricevuto l'innesto osseo RCPhC1 ha mostrato una rigenerazione ossea più ampia. Le linee tratteggiate bianche mostrano le interfacce socket. La barra della scala è uguale a 1 mm. (i) Valutazione istologica della rigenerazione ossea associata all'innesto osseo RCPhC1 (I). È stata osservata un'abbondante formazione vascolare (II) nel tessuto del midollo osseo di rigenerazione dell'osso (III) dopo 4 settimane (4 W) di guarigione. L'innesto osseo RCPhC1 è stato ampiamente riassorbito dopo 12 W di guarigione. L'osso rigenerato conteneva osteociti vitali (IV). Credito:Materiali di comunicazione sulla natura, doi:10.1038/s43246-020-00089-9
Prospettive di scaffold sintetici nell'ingegneria del tessuto osseo
In questo modo, Hideo Fushimi e colleghi hanno ottimizzato un semplice, ma processo ingegneristico critico per regolare la concentrazione di soluto di un polipeptide ricombinante della proteina della catena alfa I del collagene umano di tipo I con sostituzioni mirate di aminoacidi, abbreviato in RCPhC1. Il team ha prima impiantato la struttura in un modello di difetto osseo cranico di ratto per comprendere i fattori ingegneristici ottimali per fabbricare l'innesto osseo. Hanno progettato il materiale dell'innesto osseo per supportare la migrazione delle cellule staminali mesenchimali (MSC) verso l'area del difetto e hanno fornito un microambiente stimolante per la differenziazione osteogenica. Il solo materiale dell'innesto osseo ha mostrato un modello di guarigione ideale in assenza di fattori di crescita e cellule staminali per rigenerare l'osso. Il materiale può essere utilizzato per generare dispositivi medici e impalcature di innesto specifici per tessuto con una notevole versatilità di produzione nell'ingegneria del tessuto osseo.
© 2020 Scienza X Rete