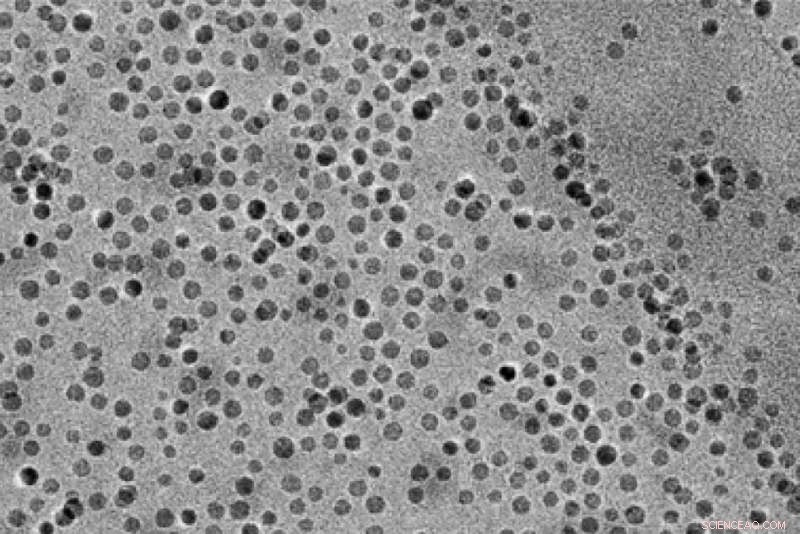
I ricercatori del MIT hanno utilizzato queste nanoparticelle di ossido di manganese per catalizzare la scomposizione dell'acqua e la successiva incorporazione di ossigeno in composti utili chiamati epossidi. Credito:ricercatori/MIT
La principale fonte di consumo energetico globale è la produzione industriale di prodotti come plastica, ferro da stiro, e acciaio. Non solo la produzione di questi materiali richiede enormi quantità di energia, ma molte delle reazioni emettono anche direttamente anidride carbonica come sottoprodotto.
Nel tentativo di contribuire a ridurre questo consumo di energia e le relative emissioni, Gli ingegneri chimici del MIT hanno ideato un approccio alternativo alla sintesi di epossidi, un tipo di sostanza chimica che viene utilizzata per fabbricare prodotti diversi, compresa la plastica, prodotti farmaceutici, e tessili. Il loro nuovo approccio, che utilizza l'elettricità per eseguire la reazione, può essere fatto a temperatura ambiente e pressione atmosferica eliminando l'anidride carbonica come sottoprodotto.
"Ciò che spesso non ci si rende conto è che l'uso di energia industriale è molto maggiore del trasporto o dell'uso residenziale. Questo è l'elefante nella stanza, e ci sono stati pochissimi progressi tecnici in termini di capacità di ridurre il consumo di energia industriale, "dice Karthish Manthiram, un assistente professore di ingegneria chimica e l'autore senior del nuovo studio.
I ricercatori hanno depositato un brevetto sulla loro tecnica, e ora stanno lavorando per migliorare l'efficienza della sintesi in modo che possa essere adattata su larga scala, uso industriale.
Il postdoc del MIT Kyoungsuk Jin è l'autore principale del documento, che appare online il 9 aprile nel Giornale della Società Chimica Americana . Altri autori includono studenti laureati Joseph Maalouf, Nikifar Lazouski, e Nathan Corbin, e postdoc Dengtao Yang.
Prodotti chimici onnipresenti
epossidi, la cui caratteristica chimica chiave è un anello a tre membri costituito da un atomo di ossigeno legato a due atomi di carbonio, sono usati per fabbricare prodotti vari come antigelo, detersivi, e poliestere.
"È impossibile andare avanti anche per un breve periodo della propria vita senza toccare o sentire o indossare qualcosa che ad un certo punto della sua storia ha coinvolto un epossido. Sono onnipresenti, " Manthiram dice. "Sono in così tanti posti diversi, ma tendiamo a non pensare all'energia incorporata e all'impronta di anidride carbonica".
Diversi epossidi sono tra le sostanze chimiche con la maggiore impronta di carbonio. La produzione di un comune epossido, ossido di etilene, genera la quinta più grande emissione di anidride carbonica di qualsiasi prodotto chimico.
La produzione di epossidi richiede molti passaggi chimici, e la maggior parte di loro sono molto energivori. Per esempio, la reazione usata per attaccare un atomo di ossigeno all'etilene, produzione di ossido di etilene, deve essere fatto a quasi 300 gradi Celsius e sotto pressioni 20 volte maggiori della pressione atmosferica. Per di più, la maggior parte dell'energia utilizzata per alimentare questo tipo di produzione proviene da combustibili fossili.
Aggiungendo all'impronta di carbonio, la reazione utilizzata per produrre ossido di etilene genera anche anidride carbonica come prodotto secondario, che viene rilasciato nell'atmosfera. Altri epossidi sono realizzati utilizzando un approccio più complicato che coinvolge perossidi pericolosi, che può essere esplosivo, e idrossido di calcio, che può causare irritazioni alla pelle.
Per trovare un approccio più sostenibile, il team del MIT si è ispirato a una reazione nota come ossidazione dell'acqua, che utilizza l'elettricità per scindere l'acqua in ossigeno, protoni, ed elettroni. Decisero di provare a eseguire l'ossidazione dell'acqua e quindi ad attaccare l'atomo di ossigeno a un composto organico chiamato olefina, che è un precursore degli epossidi.
Questo era un approccio controintuitivo, Manthiram dice, perché le olefine e l'acqua normalmente non possono reagire tra loro. Però, possono reagire tra loro quando viene applicata una tensione elettrica.
Per approfittare di questo, il team del MIT ha progettato un reattore con un anodo in cui l'acqua viene scomposta in ossigeno, ioni idrogeno (protoni), ed elettroni. Le nanoparticelle di ossido di manganese fungono da catalizzatore per aiutare questa reazione lungo, e incorporare l'ossigeno in un'olefina per fare un epossido. Protoni ed elettroni fluiscono al catodo, dove vengono convertiti in gas idrogeno.
Termodinamicamente, questa reazione richiede solo circa 1 volt di elettricità, inferiore alla tensione di una batteria AA standard. La reazione non genera anidride carbonica, e i ricercatori anticipano che potrebbero ridurre ulteriormente l'impronta di carbonio utilizzando l'elettricità da fonti rinnovabili come il solare o l'eolico per alimentare la conversione dell'epossido.
Ingrandimento
Finora, i ricercatori hanno dimostrato di poter utilizzare questo processo per creare un epossido chiamato ossido di cicloottene, e ora stanno lavorando per adattarlo ad altri epossidi. Stanno anche cercando di rendere più efficiente la conversione delle olefine in epossidi:in questo studio, circa il 30 percento della corrente elettrica è andato nella reazione di conversione, ma sperano di raddoppiare.
Stimano che il loro processo, se ingrandito, potrebbe produrre ossido di etilene al costo di 900 dollari per tonnellata, rispetto a $ 1, 500 per tonnellata utilizzando i metodi attuali. Tale costo potrebbe essere ulteriormente ridotto man mano che il processo diventa più efficiente. Un altro fattore che potrebbe contribuire alla fattibilità economica di questo approccio è che genera anche idrogeno come sottoprodotto, che è prezioso di per sé per alimentare le celle a combustibile.
I ricercatori hanno in programma di continuare a sviluppare la tecnologia nella speranza di commercializzarla infine per uso industriale, e stanno anche lavorando sull'uso dell'elettricità per sintetizzare altri tipi di sostanze chimiche.
"Ci sono molti processi che hanno enormi impronte di anidride carbonica, e la decarbonizzazione può essere guidata dall'elettrificazione, " Manthiram dice. "Si può eliminare la temperatura, eliminare la pressione, e usa invece la tensione."