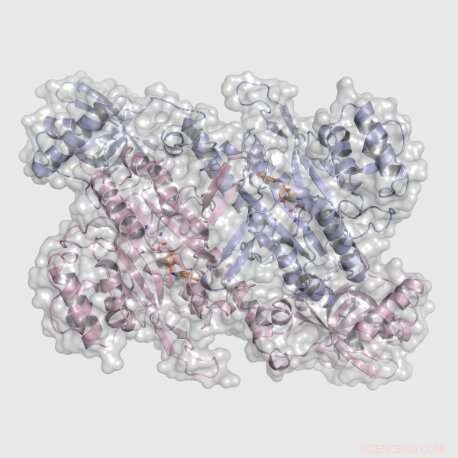
Struttura cristallina di Cryptosporidium parvum Lysyl tRNA sintetasi (CpKRS) legata a una nuova piccola molecola attiva contro i parassiti apicomplexa Plasmodium falciparum e Cryptosporidium parvum.
La ricerca di nuovi trattamenti per combattere la malaria è stata ostacolata dalla mancanza di bersagli convalidati sul parassita che causa la malattia. In un lavoro recentemente pubblicato su PNAS , un team della Drug Discovery Unit dell'Università di Dundee presenta un nuovo composto che è un inibitore selettivo dell'enzima lisil-tRNA sintetasi nei parassiti che causano la malaria e la criptosporidiosi. Il loro lavoro convalida la lisil-tRNA sintetasi come bersaglio farmacologico in questi organismi e offre un forte vantaggio per la futura scoperta di farmaci.
Controllo della malaria e della criptosporidiosi
Malaria, causata da un parassita diffuso dalle zanzare, causato più di 400, 000 morti in tutto il mondo nel 2017. Abbiamo bisogno di nuovi farmaci per combattere la malaria, dovuto sia ad un aumento della resistenza ai trattamenti esistenti, e la necessità di regimi di trattamento più semplici che possono essere completati più facilmente. Per progredire verso il controllo e l'eliminazione della malaria, avremo bisogno anche di nuovi farmaci che possano fermare la trasmissione della malattia, e prevenire le ricadute dei pazienti.
La malattia gastrointestinale criptosporidiosi è causata da un parassita correlato e si diffonde attraverso il contatto con feci umane o animali (spesso attraverso l'acqua contaminata). Negli individui sani, i sintomi generalmente regrediscono in un paio di settimane. Però, la malattia può essere fatale in pazienti con sistema immunitario compromesso, e i bambini malnutriti sono particolarmente a rischio. Non esiste un trattamento efficace per i bambini infetti, e si stima che la criptosporidiosi causi oltre 200, 000 morti ogni anno.
Gli scienziati sono alla ricerca di nuovi trattamenti, che funzionano in modi nuovi, per entrambe le malattie. Ci sono due approcci alla ricerca di nuovi farmaci contro la malaria. Il primo è lo screening fenotipico, che identifica i composti che uccidono il parassita della malaria. Per l'ultimo decennio, la Medicines for Malaria Venture (MMV) ha identificato in questo modo la maggior parte dei candidati promettenti.
Il secondo approccio, screening mirato, cerca composti che attaccano il parassita in modi specifici. È un approccio più mirato, utilizzando metodologie complementari per informare la progettazione dei farmaci. È stato un approccio di successo per molte altre malattie, ma è stato ostacolato dalla mancanza di bersagli convalidati per il parassita della malaria.
MMV ha recentemente assegnato il suo Progetto dell'anno 2018 a un team di ricercatori guidato dal Prof Ian Gilbert, Il prof. Kevin Read e la dott.ssa Beatriz Baragaña presso la Drug Discovery Unit (DDU) dell'Università di Dundee. Utilizzando la cristallografia macromolecolare (MX), e tecniche complementari, il team ha convalidato un nuovo bersaglio biologico sia per la malaria che per la criptosporidiosi e una nuova entusiasmante serie di composti che mostra attività contro questo bersaglio.
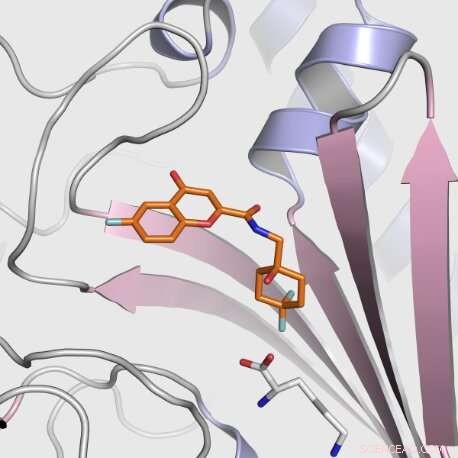
struttura di un nuovo inibitore di piccole molecole dell'apicomplexa KRS1 legato al sito attivo di Cryptosporidium parvum Lysyl tRNA sintetasi (CpKRS). Credito:sorgente luminosa a diamante
Il potere di un approccio collaborativo
Il gruppo di Dundee stava basandosi sul lavoro di un team guidato dalla microbiologa Prof Elizabeth Winzeler presso l'Università della California a San Diego. Il professor Winzeler ha identificato un composto fungino naturale (cladosporina) attivo contro la malaria, e quindi individuato il suo obiettivo.
Plasmodium falciparum è la specie parassita responsabile della forma più pericolosa di malaria, la malaria falciparum, e di circa il 50% di tutti i casi di malaria. Il parassita ha due diverse versioni di lisil-tRNA sintetasi, un enzima fondamentale per la sintesi proteica. Senza questo enzima, il parassita non può produrre proteine e quindi sopravvivere. La cladosporina attacca una versione dell'enzima, PfKRS1.
La cladosporina non è di per sé un farmaco candidato adatto, ma il team DDU è stato in grado di esplorare il potenziale di PfKRS1 come nuovo bersaglio terapeutico, lavorando attraverso la Coalizione per la scoperta dei farmaci guidata dalla struttura, finanziato dalla Fondazione Bill &Melinda Gates. Lavorando in collaborazione con il Prof Wes van Voorhis presso l'Università di Washington a Seattle, hanno selezionato librerie di composti per potenziali inibitori di PfKRS1.
Da questa proiezione, hanno trovato un punto di partenza chimico. Hanno modificato questo per creare una serie di composti simili, uno dei quali si è dimostrato efficace contro i parassiti che causano la malaria, metabolicamente stabile, e adatto per ulteriori indagini. La cristallografia macromolecolare è cruciale per questo lavoro, rivelando la forma delle molecole e intuizioni sulla loro funzione, ei cristallografi del team hanno lavorato presso le strutture di Seattle e Nuova Delhi, nonché presso la Diamond. Il team di Dundee ha accesso BAG (Block Allocation Group) a Diamond, un percorso di accesso appositamente progettato per gruppi di utenti che richiedono un accesso regolare, e chi può coordinare diversi brevi esperimenti per riempire uno spostamento temporale di 8 ore. Per questo particolare lavoro, hanno usato la linea di luce I24 Microfocus MX di Diamond.
I loro risultati offrono una forte convalida della lisil-tRNA sintetasi come bersaglio farmacologico per la malaria e la criptosporidiosi. Il team ha identificato un prezioso strumento composto, e il loro obiettivo ora è migliorare le proprietà della serie di composti. sono i primi giorni, ma l'obiettivo sarebbe quello di fornire un farmaco candidato in grado di superare tutti i traguardi di sicurezza necessari per avanzare verso lo sviluppo clinico.
Secondo il professor Gilbert, "Questo è un obiettivo molto eccitante, sicuramente da esplorare, ma c'è ancora molto lavoro da fare. È importante essere estremamente rigorosi nelle prime fasi dello sviluppo dei farmaci. Ci vorrà del tempo prima di sapere se questo lavoro porterà a un nuovo trattamento farmacologico".
Per il dottor Timothy Wells, Direttore Scientifico di MMV, "Questo lavoro rappresenta un passo avanti rispetto alla normale scoperta di farmaci. Avere una maggiore comprensione della struttura del target del farmaco è stato come gettare una luce brillante sul lavoro per ottimizzare la serie di farmaci:significa che possiamo essere davvero precisi mentre miglioriamo la selettività e la potenza dei composti."