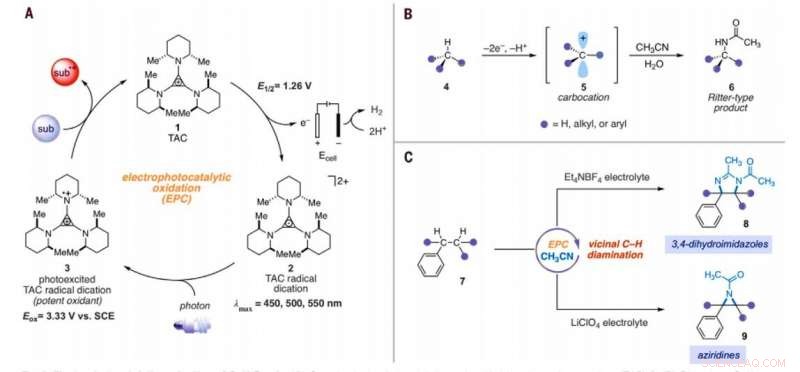
Amminazione elettrofotocatalitica dei legami C–H. (A) Ciclo elettrofotocatalitico generico con trisaminociclopropenio (TAC) 1. (B) Reazione di amminazione C–H di tipo Ritter. (C) Reazioni di diaminazione C–H vicinale elettrofotocatalitiche riportate in questo lavoro. Sub, substrato; sottoscatola, substrato ossidato; Me, metile; Et, etilico; AC, acetile; Eox, potenziale di ossidazione; lmax, lunghezza d'onda di massimo assorbimento. Credito:Scienza, 10.1126/science.abf2798
Chimica inorganica, la conversione dei legami carbonio-idrogeno (C-H) inattivati in legami carbonio-azoto (C-N) è una trasformazione molto apprezzata. Gli scienziati possono realizzare tali reazioni in un solo sito C-H poiché la prima derivatizzazione può diminuire la reattività dei legami C-H circostanti. In un nuovo rapporto ora pubblicato in Scienza , Tao Shen e Tristan H. Lambert al dipartimento di chimica e biologia chimica, Università Cornell, New York, hanno mostrato che gli areni alchilati potrebbero subire reazioni di diamminazione C-H vicinale per formare 1, Derivati 2-diammici mediante strategia elettrofotocatalitica. Durante il processo di sintesi, hanno usato acetonitrile come fonte di solvente e azoto. Hanno catalizzato la reazione utilizzando uno ione trisaminociclopropenio (TAC), che ha subito un'ossidazione anodica per fornire un dicatione radicale stabile (qualsiasi catione), mentre la reazione catodica riduceva i protoni ad idrogeno molecolare. Quando hanno irradiato la dicazione radicale TAC con una luce fluorescente compatta a luce bianca, hanno generato un intermedio fotoeccitato fortemente ossidante. In base all'elettrolita utilizzato, la squadra ha ottenuto 3, Prodotti a base di 4-diidroimidazolo o aziridina.
Un nuovo processo sintetico
Le reazioni chimiche onnipresenti che convertono i legami inerti carbonio-idrogeno (C-H) in preziosi legami carbonio-azoto (C-N) possono accelerare notevolmente la costruzione di molecole complesse rilevanti per l'impresa biomedica. I ricercatori hanno quindi derivato una serie di reazioni di amminazione C-H, ma nonostante il loro potere e la loro portata, molte campagne sintetiche devono installare numerosi collegamenti C-N. Una delle principali sfide per lo sviluppo di tali reazioni chimiche è che l'eterofunzionalità tende a disattivare i legami circostanti verso i tipici modi meccanicistici di attivazione di C–H. Finora solo poche tecnologie di reazione hanno quindi svolto funzioni multipotenti sui legami CH prossimali. Shen et al. ha descritto una strategia per una potente chimica dell'ossidazione combinando l'energia della luce e dell'elettricità all'interno di un singolo catalizzatore in un processo noto come elettrofotocatalisi (EPC). Durante questa strategia, il team ha utilizzato l'ossidazione elettrochimica dello ione trisaminociclopropenio (TAC) con un potenziale elettrochimico relativamente mite e l'irradiazione di luce visibile concomitante per eccitare l'intermedio cationico radicale risultante. La dicazione radicale fotoeccitata era un ossidante estremamente potente che ha dimostrato reazioni impegnative comprese le funzioni ossidative del benzene e di altri areni poveri di elettroni o la funzionalizzazione regioselettiva C-H degli eteri.
Ambito del substrato della diaminazione C–H vicinale elettrofotocatalitica. Tutte le rese sono di prodotti isolati. I prodotti sono stati ottenuti come miscele racemiche; le raffigurazioni di cunei e trattini indicano relazioni stereochimiche relative. (A) Diaminazione di alchilbenzeni secondari. (B) Diaminazione di alchilbenzeni primari. I dettagli sperimentali sono forniti nei materiali supplementari. Un asterisco indica l'esecuzione a 2,2 V; un simbolo di pugnale (†) indica work-up con NaHCO3 (aq) e CH3OH; e un simbolo a doppio pugnale (‡) indica nBu4NPF6 invece di Et4NBF4. SM, materiali di partenza. Il composto 36 è stato deacilato durante il workup. Credito:Scienza, 10.1126/science.abf2798 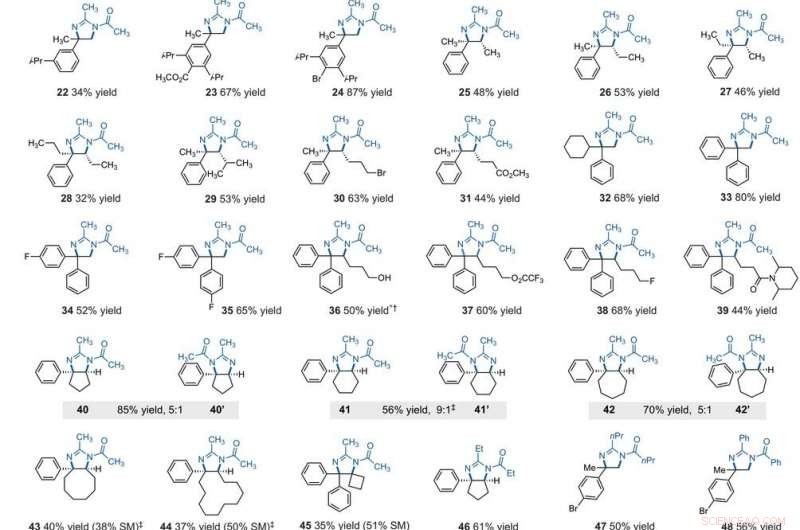
Il team ha ipotizzato che il potere ossidante della TAC consenta anche ad altri collettori di attivazione del legame CH. Nelle giuste condizioni, l'approccio elettrofotocatalitico potrebbe generare intermedi carbo-cationici per facilitare la funzionalizzazione di tipo Ritter dei legami CH senza un ossidante chimico esterno. Tipicamente, durante le reazioni di tipo Ritter generano un carbocatione con successivo intrappolamento da parte di un nitrile per formare intermedi di ioni nitrilio seguiti da prodotti ammidici dopo idrolisi. Il team ha ipotizzato che il forte ossidante, tuttavia le condizioni selettive offerte da TAC (trisaminociclopropenio) EPC (elettrofotocatalisi) potrebbero consentire una sequenza di reazioni multiple di funzionalizzazione C-H di tipo Ritter, dove il gruppo acetammide inizialmente formato ha facilitato una seconda reazione di amminazione in una posizione adiacente. Se fattibile, il metodo potrebbe facilitare l'amminazione regioselettiva di due legami CH semplicemente usando la luce visibile, un lieve potenziale elettrochimico e un comune solvente come fonte di azoto al posto dei precursori del nitrene. Shen et al. ha riportato la realizzazione della deaminazione elettrofotocatalitica dei legami C-H per fornire diidroimidazoli o aziridine, a seconda del tipo di elettrolita utilizzato durante gli esperimenti.
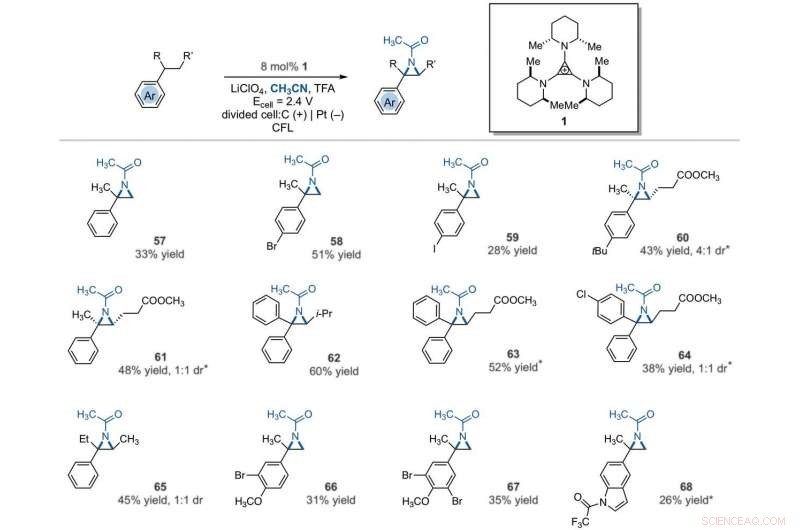
Electrophotocatalytic vicinal C–H aziridination. Detailed reaction conditions for each substrate are provided in the supplementary materials. Products were obtained as racemic mixtures; wedge and dash depictions indicate relative stereochemical relationships. An asterisk indicates run at 2.2 V. i-Pr, isopropyl. Credito:Scienza, 10.1126/science.abf2798
The synthetic products
After extensively screening, the reaction conditions including the cell potential, electrolyte, acid additive and reaction time, Shen et al. identified conditions to assist the efficient conversion of a variety of benzylic hydrocarbons of the corresponding N-acyl-4, 5-dihydroimidazole adducts. In the reaction setup, the scientists used visible light irradiation with a white compact fluorescent light of a solution of the substrate containing TAC in a divided electrolytic cell under controlled potential. The team added the TAC catalyst and substrate within the anodic chamber where the C-H deamination chemistry occurred. The resulting redox by-product was effectively traceless. Based on similar conditions, a variety of benzylic hydrocarbons underwent vicinal C-H diamination to form diverse products. In tutti i casi, the researchers noted how the function of methylene carbons occurred in preference to methyl carbons, even when in the presence of a sterically demanding group or electron-withdrawing group. Since the α-α-diaryl amines formed a valuable substructure in biomedically relevant compounds, the team also investigated the transformation on gem-diaryl substrates. They found that the 1, 1-diphenyl ethane reacted efficiently to furnish a secondary alkyl benzene compound with 80 percent yield. The compatibility of alcohol, ester, alkyl fluoride and amide substituents allowed the synthesis of more highly functionalized adducts.
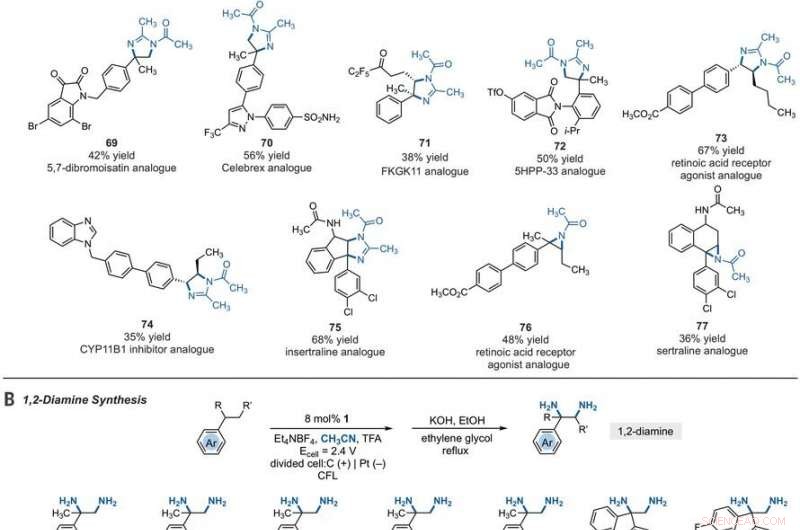
Synthetic applications of electrophotocatalytic vicinal C–H diamination. (A) Bioactive compound analogs prepared by means of electrophotocatalytic vicinal C–H diamination or aziridination. (B) 1, 2-Diamine synthesis. (C) Dihydroimidazole synthesis. (D) Bioactive compound synthesis. Detailed reaction conditions are provided in the supplementary materials. Products were obtained as racemic mixtures; wedge and dash depictions indicate relative stereochemical relationships. Products 80 and 81 were isolated as bis tosylate salts. Ph, fenile; Tf, trifluoromethanesulfonate. Credito:Scienza, 10.1126/science.abf2798
Functionalizing ring systems
The team further studied the potential of this reaction to functionalize ring systems. The reaction of phenyl cyclopentane led to the bicyclic compound in 85 percent yield. The scientists produced six- and seven-membered ring products as regioisomeric mixtures, alongside eight- and 12-membered ring products as single isomers. They improved some of the yields for cyclic substrates by using tetrabutylammonium phosphate (TBAF 6 ) as the electrolyte. In addition to acetonitrile, the researchers used other nitriles to give rise to diaminated products derived from propionitrile, butyl nitrile or benzonitrile as the nitrogen source. The scientists also tested the diamination process using unbranched benzylic substrates. Di conseguenza, imine and halogenated derivatives gave rise to aziridines in low to modest yields with nearly equal yields of diaminated products.
Mechanistic rationale for electrophotocatalytic vicinal C–H diamination. Voltages were measured in a 5:1 mixture of CH3CN and TFA to mimic the reaction conditions and are relative to SCE. Credito:Scienza, 10.1126/science.abf2798 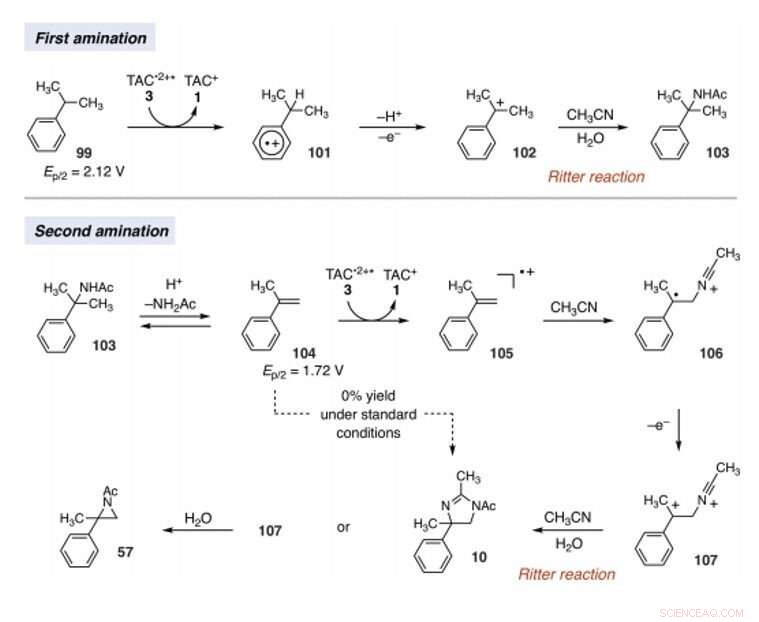
Since late-stage C-H functionalization processes offered powerful tools for the diversification of medicinal compound libraries, Shen et al. tested the difunctionalization chemistry on several molecules that are close analogs of known biologically active molecules. The team diaminated a dibromoisatin derivative to produce a bioactive molecule analogue in 42 percent yield. Per esempio, Isatin derivatives have been investigated in the past due to their medicinal properties including antitumor and antiviral activities. The scientists also found that celecoxib analogs could produce 56 percent yield under standard conditions. They then converted an analog of thalidomide with antiproliferative activity into another bioactive analog with 50 percent yield. The team further found how a small modification to the electrophotocatalytic procedure could lead to the isolation of free 1, 2-diamines in good yields. Shen et al. believe the mechanisms to have originated with Ritter-type amination of the substrates benzylic C-H bond in a process that accords with known electrochemical Ritter-type reactions. In questo modo, Tao Shen and Tristan H. Lambert noted the compatibility of deamination with a reasonable diversity of functionality for the practical applications of this reaction. The scientists used the power of combined light and electrical energy to conduct the reactions in the functionality of a single catalyst with advancing synthetic capabilities.
© 2021 Science X Network