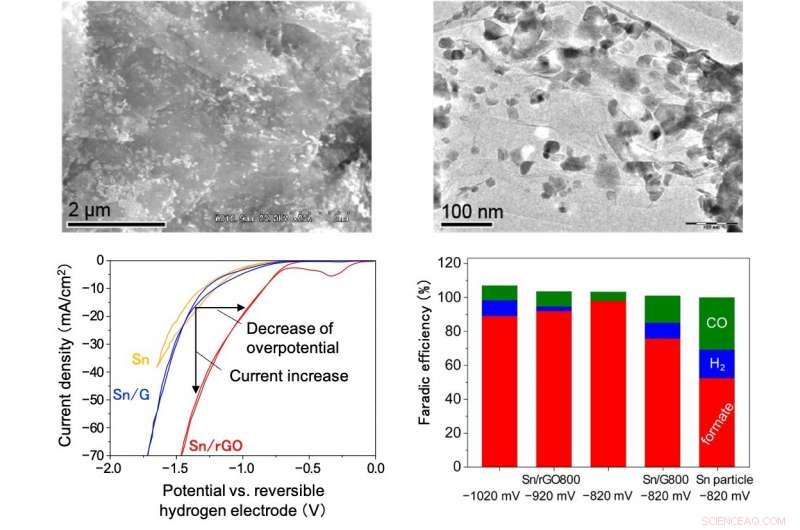
Immagine al microscopio elettronico a scansione (in alto a sinistra), immagine al microscopio elettronico a trasmissione (in alto a destra), caratteristiche di riduzione (in basso a sinistra) ed efficienza faradica (in basso a destra) del catalizzatore Sn/rGO. Si può notare che nanoparticelle di Sn di 10-50 nm sono uniformemente disperse sul foglio di ossido di grafene ridotto (in alto a sinistra e in alto a destra). Anche, il valore assoluto della densità di corrente sotto CO 2 il flusso è maggiore di quello del catalizzatore convenzionale (Sn) o dell'ossido di grafene supportato da Sn (Sn/GO), e la corrente aumenta da un potenziale elettrico iniziale di valore assoluto inferiore. Così, si può notare che l'iperpotenziale è significativamente ridotto e che la densità di corrente è aumentata. Inoltre, l'efficienza faradica del formiato è molto elevata utilizzando il catalizzatore Sn/rGO (in basso a sinistra e in basso a destra). Credito:Università di Kanazawa
Diminuzione delle emissioni e utilizzo efficiente (fissazione) dell'anidride carbonica (CO 2 ) sono questioni mondiali per prevenire il riscaldamento globale. La promozione dell'uso delle energie rinnovabili è efficace nella riduzione della CO 2 emissioni. Però, poiché ci sono grandi fluttuazioni dipendenti dal tempo e grandi differenze regionali nella produzione di energia rinnovabile, è necessario stabilire una tecnologia di fissazione per consentire il trasporto e lo stoccaggio dell'energia in modo efficiente. Così, c'è un crescente interesse per le tecnologie per la sintesi di sostanze chimiche utili dalla CO 2 utilizzando energia elettrica derivata da energie rinnovabili. In particolare, l'acido formico sta attirando molta attenzione come vettore energetico (idrogeno) perché è liquido e non tossico a temperatura ambiente. L'adozione di questa tecnologia contribuirà al trasporto e allo stoccaggio efficienti di energia rinnovabile e alla fissazione della CO 2 , e consentire lo stoccaggio di energia con un'elevata compatibilità ambientale.
Nella riduzione elettrochimica della CO 2 , è noto che l'acido formico può essere ottenuto con un'efficienza faradica di circa il 50-60% utilizzando stagno (Sn) come catalizzatore catodico. Però, al fine di sviluppare questa tecnologia per l'uso pratico, sono necessari un ulteriore miglioramento dell'efficienza faradica e una riduzione del potenziale eccessivo. C'è molto interesse attivo nella ricerca per comprendere i principi di progettazione dei catalizzatori per consentire il raggiungimento di questi obiettivi.
L'attuale gruppo di ricerca guidato dal Prof. Tsujiguchi e dai suoi colleghi dell'Università di Kanazawa in collaborazione con scienziati dell'Università di Tsukuba e dell'Università di Osaka ha preparato un catalizzatore stagno/ossido di grafene ridotto (Sn/rGO) in cui lo Sn è stato supportato su ossido di grafite ridotto mediante trattamento termico riduzione del cloruro di stagno (SnCl 2 ) e ossido di grafene (GO) ottenuto ossidando la polvere di grafite con il metodo Hummers migliorato. Nel catalizzatore così preparato, Sn è uniformemente disperso nello strato rGO, e il composito viene impilato per formare una morfologia 3-D, cioè rGO/Sn/rGO.
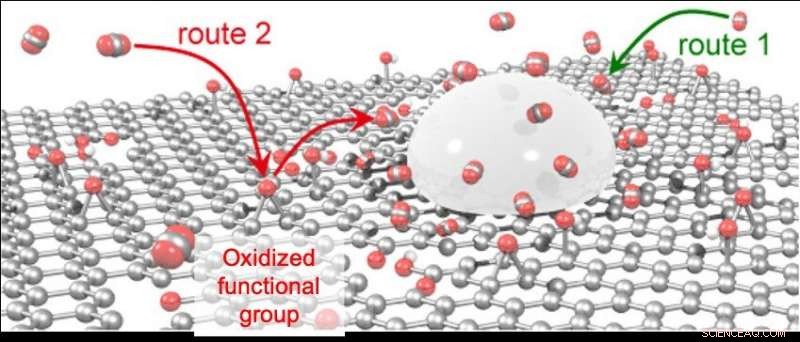
Oltre al percorso convenzionale, cioè CO 2 adsorbito direttamente su Sn (Route 1), CO 2 adsorbito sui gruppi funzionali ossidati di rGO viene fornito a Sn (Route 2). Credito:Università di Kanazawa
Questo catalizzatore è caratterizzato come un supporto con un gruppo funzionale contenente una quantità di ossigeno molto maggiore rispetto al catalizzatore stagno/grafite utilizzato per un confronto. Quando abbiamo eseguito la riduzione elettrochimica di CO 2 utilizzando questi catalizzatori con CO 2 disciolto in una soluzione di idrogenocarbonato di potassio (KHCO 3 ), si è riscontrato che il catalizzatore Sn/rGO riduceva significativamente il potenziale eccessivo e permetteva di ottenere un'elevata densità di corrente rispetto al catalizzatore Sn. Inoltre, quando la riduzione di CO 2 è stato eseguito a potenziale costante, quasi nessun prodotto diverso dall'acido formico, come H 2 e CO, sono stati rilevati e siamo riusciti ad ottenere acido formico con un'efficienza faradica del 98% (1,8 volte quella con il solo catalizzatore Sn).
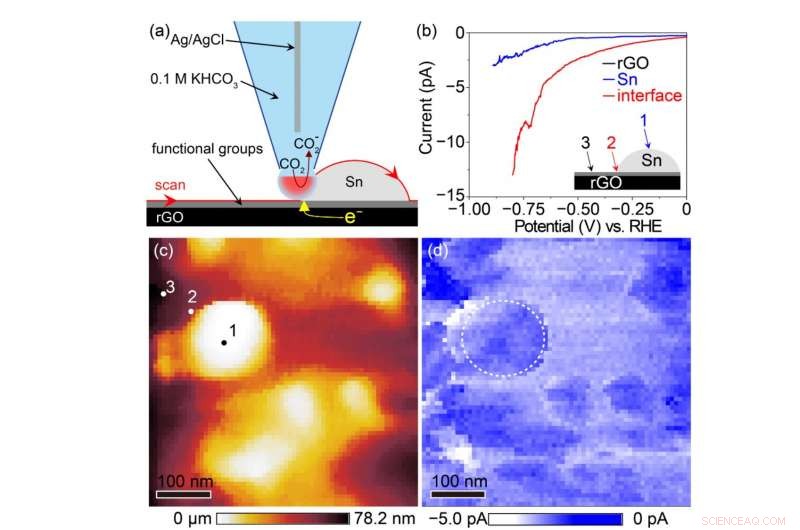
Schema concettuale dell'imaging elettrochimico Sn/rGO con un microscopio cellulare elettrochimico a scansione (in alto a sinistra), caratteristiche della CO 2 riduzione sulla superficie rGO, sulla superficie Sn, e all'interfaccia tra Sn e rGO (in alto a destra), topografia al microscopio cellulare elettrochimico (in basso a sinistra; 1, sulla superficie Sn; 2, all'interfaccia tra Sn e rGO; 3, sulla superficie rGO) e mappatura della corrente di riduzione (in basso a destra). Questa figura mostra che CO 2 è efficientemente ridotto all'interfaccia tra Sn e rGO. Credito:Università di Kanazawa
La ragione per la produzione di acido formico altamente efficiente ottenuta utilizzando il catalizzatore Sn/rGO è la sua elevata CO 2 capacità di assorbimento. Sn/rGO può assorbire quattro volte più CO 2 come catalizzatore Sn da solo. Ulteriore, il tasso di CO 2 l'adsorbimento è otto volte quello del catalizzatore Sn da solo. La chimica computazionale ha previsto che questa CO . elevata 2 la capacità di adsorbimento sarebbe dovuta ai gruppi funzionali ossidati di rGO e che la produzione di idrogeno e monossido di carbonio sarebbe soppressa poiché la CO 2 adsorbito dal gruppo funzionale ossidato di rGO viene fornito rapidamente ed efficientemente alla superficie Sn adiacente.
Per confermare sperimentalmente questo meccanismo, il nostro team ha tentato l'imaging elettrochimico dell'attività catalitica con un microscopio cellulare elettrochimico a scansione. È stato rivelato che una densità di corrente di riduzione significativamente maggiore è stata osservata all'interfaccia tra Sn e rGO rispetto alle superfici Sn o rGO (Fig. 3) suggerendo che una grande quantità di acido formico è sintetizzata su Sn adiacente a rGO, a sostegno della previsione di cui sopra mediante chimica computazionale. Questa è la prima dimostrazione sperimentale utilizzando un microscopio cellulare elettrochimico a scansione che la sintesi dell'acido formico sta avvenendo attivamente all'interfaccia tra il catalizzatore e il supporto. Così, una sintesi più efficiente dell'acido formico sarebbe possibile combinando un supporto con un'elevata CO 2 capacità di adsorbimento con catalizzatore per la riduzione elettrochimica di CO 2 . Ciò fornisce un quadro importante che potrebbe essere applicato a tutti i catalizzatori disponibili finora.
I risultati del presente studio forniscono nuove informazioni sullo sviluppo di catalizzatori per la sintesi dell'acido formico mediante la riduzione della CO 2 , e si prevedono notevoli progressi nello sviluppo della tecnologia di sintesi dell'acido formico mediante la riduzione elettrochimica di CO 2 . Inoltre, abbiamo dimostrato un miglioramento della selettività grazie all'ottima CO 2 capacità di adsorbimento del supporto oltre a chiarirne il meccanismo di reazione. Ciò dovrebbe avere un grande impatto sulla tecnologia di riduzione elettrochimica relativa alla CO 2 , compresa la sintesi di metanolo, metano e olefine. Perciò, ha il potenziale per essere un'utile tecnologia di base nella sintesi di sostanze chimiche da CO 2 . Nel futuro, prevediamo che lo sviluppo di celle di riduzione elettrochimica che utilizzino questo catalizzatore sarà incoraggiato, portando alla realizzazione di dispositivi di accumulo di energia ad elevata compatibilità ambientale che possono contribuire alla fissazione della CO 2 e promozione dell'uso efficiente delle energie rinnovabili.