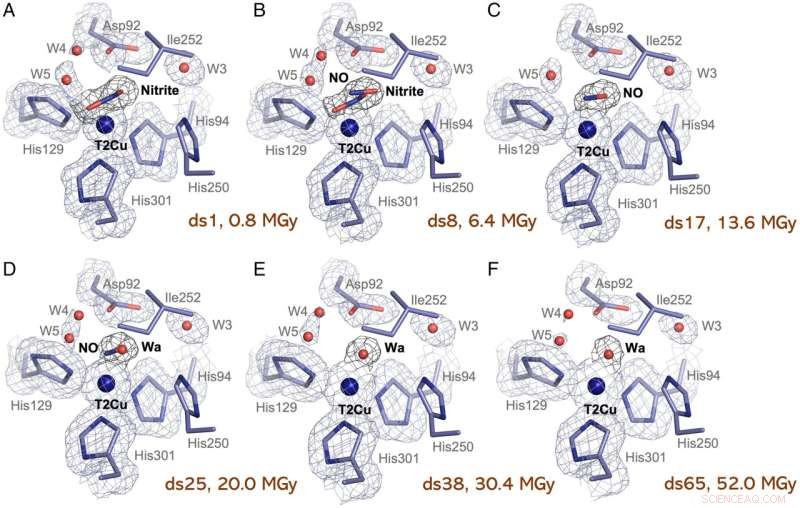
Sito T2Cu durante la serie MSOX di un Br 2D imbevuto di nitriti Cristallo NiR. (A) Il sito T2Cu dopo la prima esposizione a raggi X 0,8-MGy (DS1) che mostra la piena occupazione di un singolo nitrito laterale coordinato a T2Cu, Asp92 in posizione prossimale e due canali d'acqua (W4 e W5). Ile252 e His250 non mostrano modifiche. (B) Il sito T2Cu in DS8 (6,4 MGy) che mostra la stessa occupazione di nitrito e NO. Non si vedono altre modifiche. (C) Il sito T2Cu in DS17 (13,6 MGy) che mostra la piena occupazione di un singolo NO laterale coordinato a T2Cu. W4 ora è scomparso. (D) Il sito T2Cu in DS25 (20 MGy) che mostra la stessa occupazione di NO e acqua (Wa). W4 è ora tornato. (E) Il sito T2Cu in DS38 (30,4 MGy) che mostra la piena occupazione di una singola acqua coordinata a T2Cu, imitando il sito T2CuII ossidato in altri CuNiR prototipici. Non si vedono altre modifiche. (F) Il sito T2Cu nel set di dati finale della serie MSOX legata ai nitriti (DS65), dopo un totale di 50 MGy, che mostra la singola acqua (Wa) ancora coordinata a T2Cu. Asp92 mostra segni di bruciatura a causa del superamento del limite di dose nel cristallo con una perdita di densità osservata. Anche W4 e W5 sono quasi completamente scomparsi. Le mappe di densità elettronica dei residui 2Fo − Fc sono contornate a livello 1σ. Le mappe di densità elettronica 2Fo − Fc dei ligandi sono contornate a livello di 0,9σ. T2Cu è mostrato come una sfera blu. Credito:Atti dell'Accademia Nazionale delle Scienze (2022). DOI:10.1073/pnas.2205664119
Un team internazionale di scienziati, guidato dall'Università di Liverpool, ha prodotto filmati strutturali di un enzima chiave coinvolto in un percorso biologico di produzione di gas serra che offrono nuove informazioni sulla sua attività catalitica.
Uno dei principali fattori che contribuiscono al riscaldamento globale è il gas serra protossido di azoto, che è 300 volte più dannoso per lo strato di ozono rispetto al biossido di carbonio. Il protossido di azoto è un sottoprodotto del percorso di denitrificazione, che si verifica quando tipi speciali di microrganismi rimuovono i nitrati o i nitriti in eccesso dagli ecosistemi e li riconvertono in azoto gassoso.
La prima fase di questo processo coinvolge un enzima chiamato rame nitrito reduttasi (CuNiR), che converte il nitrito in ossido nitrico gassoso, utilizzando un elettrone e un protone. Recentemente è stato scoperto un CuNiR di una specie Rhizobia con un'attività catalitica sostanzialmente inferiore. Questa specie è abbondante in agricoltura ed è un importante contributo al percorso di denitrificazione e quindi al protossido di azoto.
CuNiR è una metalloproteina, nel senso che contiene ioni metallici per funzionare correttamente, in questo caso contiene due siti di rame, uno dove avviene la catalisi e un altro che riceve e dona un elettrone necessario per la catalisi. Le metalloproteine sono molto diffuse in biologia, costituendo almeno il 30% di tutte le proteine.
I ricercatori del Regno Unito e del Giappone hanno utilizzato la spettroscopia a cristallo singolo e un approccio di cristallografia a raggi X noto come MSOX (strutture multiple da un cristallo) per produrre un film molecolare dell'enzima al fine di capire perché l'attività è molto più bassa in questo CuNiR. La cristallografia a raggi X è una tecnica importante che consente di visualizzare i dettagli atomici delle molecole biologiche in tre dimensioni, aiutando a capire come sono assemblati, come funzionano e come interagiscono. MSOX è un progresso in questo in quanto consente di visualizzare la catalisi in tempo reale.
Primo autore, Ph.D. Lo studente Samuel Rose ha detto:"Questa ricerca è importante per due motivi. In primo luogo, ci aiuta a capire perché l'attività in questo CuNiR è inferiore rispetto ad altri, il che può aiutare con la futura bioingegneria per aiutare ad affrontare il riscaldamento globale. In secondo luogo, mostra che l'approccio MSOX insieme alla spettroscopia a cristallo singolo è un'entusiasmante combinazione che può aiutare a sezionare complesse reazioni redox in altri metalloenzimi fondamentali."
Il professor Samar Hasnain, che ha guidato la ricerca presso l'Università di Liverpool, ha dichiarato:"Solo comprendendo i processi biologici e chimici fondamentali saremo in grado di affrontare i principali problemi ambientali. L'approccio sviluppato per questo studio sarebbe applicabile a molti sistemi, tra cui quelli coinvolti nella produzione di idrogeno (idrogenasi), nell'utilizzo dell'azoto (nitrogenasi) e nella fotosintesi (fotosistema II)."
La ricerca è pubblicata in Atti dell'Accademia Nazionale delle Scienze . + Esplora ulteriormente