La picrotossinina, una tossina di origine vegetale utilizzata tradizionalmente dai pescatori asiatici per paralizzare e catturare i pesci, è stata a lungo considerata un possibile punto di partenza per nuove terapie umane e altri prodotti neuroattivi.
Tuttavia sono stati fatti pochi progressi a causa dell'instabilità chimica e della tossicità della picrotossinina e della difficoltà di creare e modificare la sua struttura complessa. Tuttavia, i chimici della Scripps Research hanno trovato un modo relativamente semplice per creare versioni della picrotossinina con proprietà migliorate.
In uno studio pubblicato su Nature Communications , i ricercatori hanno dimostrato che le varianti chimiche vicine della picrotossinina che contengono una singola piccola modifica hanno una migliore stabilità chimica, sono molto più facili da produrre e modificare e sono più sicure per gli esseri umani. Ciò apre la strada allo sviluppo di nuovi farmaci neurologici, pesticidi più sicuri e persino trattamenti antiparassitari.
"Solo una piccola alterazione del prodotto naturale conferisce proprietà sfuggenti per decenni", afferma l'autore senior dello studio Ryan Shenvi, Ph.D., professore presso il Dipartimento di Chimica della Scripps Research.
Il primo autore è stato Guanghu Tong, Ph.D., un ricercatore associato post-dottorato presso lo Shenvi Lab durante lo studio.
La picrotossinina proviene dai semi - spesso chiamati semi di "bacche di pesce" a causa del loro utilizzo da parte dei pescatori - di Anamirta cocculus, una pianta che si trova in alcune parti del sud-est asiatico e dell'India. La tossina blocca potentemente l'attività dei recettori neuronali presenti nella maggior parte degli organismi superiori.
Nei mammiferi, questi sono chiamati GABAA recettori, ed esistono in tutto il cervello, in gran parte per impedire ad altri neuroni di diventare iperattivi. Anche a piccole dosi, il blocco di questi recettori da parte della picrotossinina può causare convulsioni e interrompere fatalmente i segnali nervosi che controllano la respirazione.
Potrebbe sembrare contraddittorio che i chimici si rivolgano ai veleni per produrre nuovi medicinali, ma molte tossine vegetali, oltre a colpire obiettivi desiderabili, hanno già buone proprietà simili ai farmaci, ad esempio permettendo loro di raggiungere i loro obiettivi tramite somministrazione orale.
Nel caso della picrotossinina, i chimici vorrebbero modificarla per sviluppare farmaci per disturbi psichiatrici e neurologici, pesticidi e farmaci antiparassitari sicuri ed efficaci e strumenti di laboratorio per manipolare il GABA con precisione A recettori. Il problema è che le altre proprietà chimiche della picrotossinina, come la sua difficoltà di sintesi e la tendenza a reagire con i solventi comuni, l'hanno resa straordinariamente difficile da domare.
Il laboratorio di Shenvi utilizza tecniche di chimica organica per superare tali sfide e trovare modi per migliorare i prodotti naturali. Per anni, lui e il suo team si sono concentrati sulle molecole che prendono di mira il GABAA recettori e nel 2020 hanno riportato la sintesi organica di picrotossinina più breve di sempre.
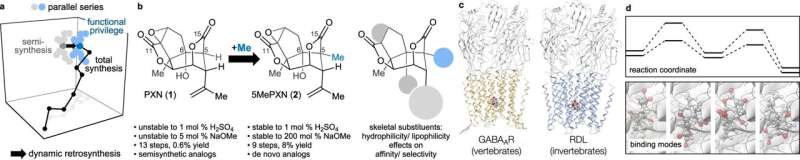
In quello studio, hanno scoperto che potevano sintetizzare molto più facilmente un composto che era quasi uguale alla picrotossinina. La 5Me-picrotossinina, come la chiamavano, potrebbe ancora legarsi al GABAA recettori e differiva dal suo cugino chimico solo per l’aggiunta di un gruppo di atomi – chiamato gruppo metilico – in una posizione chiave sulla molecola. Considerato questo cambiamento strutturale, il team di Shenvi ha studiato le nuove proprietà della 5Me-picrotossinina per il nuovo studio.
Il team ha sintetizzato due serie parallele di varianti di picrotossinina e 5Me-picrotossinina, determinando come l'assenza o la presenza del gruppo metilico modifica la stabilità della molecola e la selettività di legame del recettore.
Hanno scoperto che la versione metilata è chimicamente molto più stabile, con un'emivita nel sangue che sembra essere quasi tripla rispetto a quella della picrotossinina ordinaria. Hanno anche scoperto che la 5Me-picrotossinina è molto meno soggetta a reazioni con i comuni solventi, inclusi alcoli e acidi. I coautori Shuming Chen, Ph.D., assistente professore di chimica all'Oberlin College, e il membro del suo laboratorio Anna Crowell hanno spiegato questo utilizzando la modellazione computazionale.
Un'altra sorpresa è stata che la versione metilata ha una potenza inferiore contro il GABAA dei mammiferi recettori pur mantenendo un'elevata potenza contro le versioni del recettore degli insetti:proprio quello che si vorrebbe per un composto sicuro che uccide gli insetti.
"Il fatto che la picrotossinina prende di mira una famiglia di recettori tra cui il GABAA dei recettori è noto da diversi decenni, ma questa è la prima volta che siamo riusciti a modificare la sua selettività per tali recettori," afferma Tong.
Gli esperimenti con varianti di picrotossinina e recettori degli insetti sono stati condotti dalla collaborazione di ricercatori di Corteva Agriscience, sviluppatori di prodotti per il controllo dei parassiti. I modelli costruiti per lo studio dal chimico computazionale Corteva Avery Sader, Ph.D., suggeriscono ulteriori modi per modificare la 5Me-picrotossinina per renderla più selettiva per gli insetti nocivi e quindi più sicura per gli esseri umani.
I ricercatori intendono continuare a sintetizzare e studiare nuove varianti della 5Me-picrotossinina per il loro potenziale di sviluppo in nuovi farmaci e altri prodotti.
Ulteriori informazioni: Guanghu Tong et al, la metilazione C5 conferisce accessibilità, stabilità e selettività alla picrotossinina, Nature Communications (2023). DOI:10.1038/s41467-023-44030-3
Fornito da The Scripps Research Institute