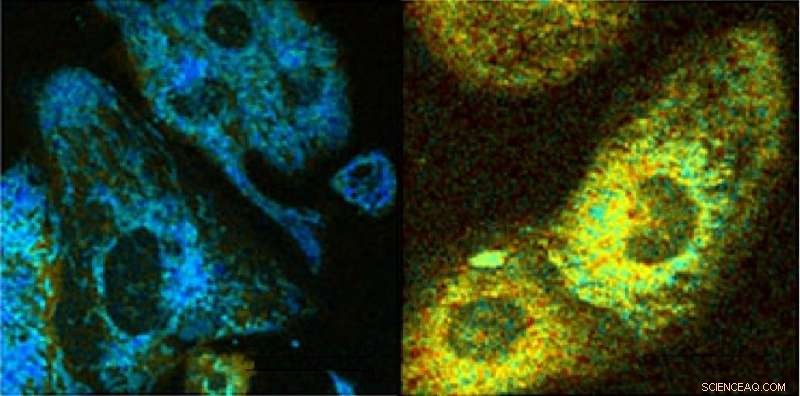
Letture ottiche di cardiomiociti HL-1 in risposta al disaccoppiamento chimico da CCCP. Mappa del rapporto di ossidoriduzione per il controllo (a sinistra), e cardiomiociti esposti CCCP (a destra). Credito:Irene Georgakoudi, Tufts University
I cambiamenti metabolici nelle cellule possono verificarsi nelle prime fasi della malattia. Nella maggior parte dei casi, la conoscenza di quei segnali è limitata, poiché di solito rileviamo la malattia solo dopo che ha causato danni significativi. Ora, un team guidato da ingegneri della Tufts University School of Engineering ha aperto una finestra sulla cellula sviluppando uno strumento ottico in grado di leggere il metabolismo a risoluzione subcellulare, senza dover perturbare le cellule con mezzi di contrasto, o distruggerli per condurre analisi. Come riportato oggi in Progressi scientifici , i ricercatori sono stati in grado di utilizzare il metodo per identificare specifiche firme metaboliche che potrebbero insorgere nel diabete, cancro, malattie cardiovascolari e neurodegenerative.
Il metodo si basa sulla fluorescenza di due importanti coenzimi (biomolecole che lavorano di concerto con gli enzimi) quando eccitati da un raggio laser. I coenzimi, nicotinammide adenina dinucleotide (NADH) e flavina adenina dinucleotide (FAD), sono coinvolti in un gran numero di vie metaboliche in ogni cellula. Per conoscere le specifiche vie metaboliche interessate da malattie o stress, gli scienziati di Tufts hanno esaminato tre parametri:il rapporto tra FAD e NADH, la fluorescenza "sbiadisce" del NADH, e l'organizzazione dei mitocondri come rivelata dalla distribuzione spaziale di NADH all'interno di una cellula (l'energia che produce "batterie" della cellula).
Il primo parametro, la quantità relativa di FAD rispetto a NADH, può rivelare quanto bene la cellula stia consumando ossigeno, metabolizzare gli zuccheri, o produrre o scomporre molecole di grasso. Il secondo parametro, la "dissolvenza" della fluorescenza del NADH, rivela dettagli sull'ambiente locale del NADH. Il terzo parametro, la distribuzione spaziale del NADH nelle cellule, mostra come i mitocondri si dividono e si fondono in risposta alla crescita cellulare e allo stress.
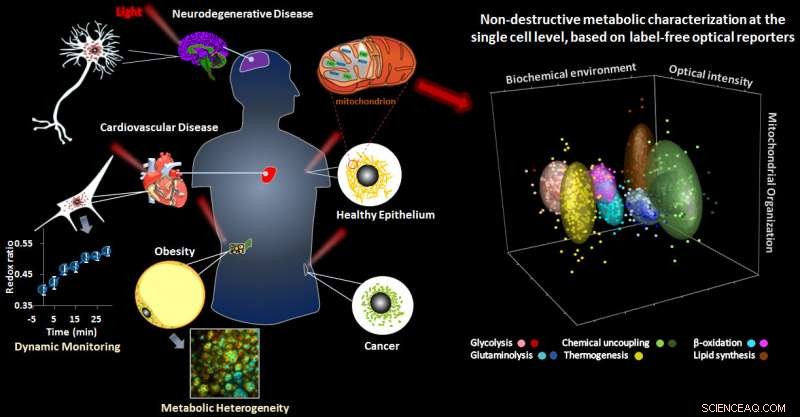
Abstract grafico di studio. Credito:I. Georgakoudi, Z. Liu, e D. Pouli
"Presi insieme, questi tre parametri iniziano a fornire informazioni più specifiche, e firme metaboliche uniche di salute o disfunzione cellulare, " ha detto Irene Georgakoudi, dottorato di ricerca, autore corrispondente dello studio e professore di ingegneria biomedica presso la School of Engineering di Tufts. "Il potere di questo metodo è la capacità di ottenere informazioni su cellule vive, senza l'uso di mezzi di contrasto o etichette allegate che potrebbero interferire con i risultati".
Esistono altri metodi per tracciare in modo non invasivo le firme metaboliche della malattia, come la scansione PET, che viene spesso utilizzato nella ricerca. Ma mentre le scansioni PET forniscono informazioni a bassa risoluzione con un'eccellente penetrazione in profondità nei tessuti viventi, il metodo ottico introdotto dai ricercatori di Tufts rileva l'attività metabolica alla risoluzione delle singole cellule, anche se per lo più vicino alla superficie.
Questo non è necessariamente un limite. Molte malattie possono essere rilevate sulla superficie dei tessuti, compreso il cancro, mentre molti studi preclinici vengono eseguiti con modelli animali e tessuti tridimensionali ingegnerizzati che possono trarre vantaggio dal monitoraggio non distruttivo. Il metodo sviluppato da Georgakoudi e colleghi potrebbe rivelarsi un potente strumento di ricerca per comprendere le loro firme metaboliche.