
Il dottorando Tyler Fulton prepara campioni di piccole molecole in un laboratorio al Caltech. Credito:Caltech
In un nuovo studio che uno scienziato ha definito sbalorditivo, un team congiunto UCLA/Caltech ha dimostrato che è possibile ottenere le strutture di piccole molecole, come alcuni ormoni e farmaci, in appena 30 minuti. Sono ore e persino giorni in meno di quanto fosse possibile prima.
Il team ha utilizzato una tecnica chiamata diffrazione di microelettroni (MicroED), che era stato utilizzato in passato per apprendere le strutture 3-D di molecole più grandi, nello specifico le proteine. In questo nuovo studio, i ricercatori mostrano che la tecnica può essere applicata a piccole molecole, e che il processo richiede molto meno tempo di preparazione del previsto. A differenza delle tecniche correlate, alcune delle quali comportano la crescita di cristalli delle dimensioni di grani di sale, questo metodo, come dimostra il nuovo studio, può lavorare con campioni di partenza comuni, a volte anche polveri raschiate dal lato di un bicchiere.
"Abbiamo preso i campioni più bassi che puoi ottenere e ottenuto le strutture di altissima qualità in pochissimo tempo, " dice il professore di chimica del Caltech Brian Stoltz, chi è coautore del nuovo studio, pubblicato sulla rivista Scienze Centrali ACS . "Quando ho visto i risultati per la prima volta, la mia mascella ha colpito il pavimento." Inizialmente pubblicato sul server di prestampa Chemrxiv a metà ottobre, l'articolo è stato visualizzato più di 35, 000 volte.
Il motivo per cui il metodo funziona così bene su campioni di piccole molecole è che mentre i campioni possono sembrare semplici polveri, in realtà contengono minuscoli cristalli, ciascuno circa un miliardo di volte più piccolo di un granello di polvere. I ricercatori erano già a conoscenza di questi microcristalli nascosti, ma non si sono resi conto che potevano rivelare prontamente le strutture molecolari dei cristalli usando MicroED. "Non credo che le persone si siano rese conto di quanto siano comuni questi microcristalli nei campioni polverosi, " dice Stoltz. "Questo è come la fantascienza. Non pensavo che sarebbe successo durante la mia vita, che si potessero vedere strutture dalle polveri".
I risultati hanno implicazioni per i chimici che desiderano determinare le strutture di piccole molecole, che sono definiti quelli di peso inferiore a circa 900 dalton. (Un dalton ha circa il peso di un atomo di idrogeno.) Questi minuscoli composti includono alcune sostanze chimiche presenti in natura, alcune sostanze biologiche come gli ormoni, e una serie di farmaci terapeutici. Le possibili applicazioni della metodologia di ricerca della struttura MicroED includono la scoperta di farmaci, analisi di laboratorio criminale, test medici, e altro ancora. Ad esempio, Stoltz dice, il metodo potrebbe essere utile per testare gli ultimi farmaci dopanti negli atleti, dove possono essere presenti solo tracce di una sostanza chimica.
"Il passo più lento nella creazione di nuove molecole è determinare la struttura del prodotto. Potrebbe non essere più così, poiché questa tecnica promette di rivoluzionare la chimica organica, "dice Robert Grubbs, Victor ed Elizabeth Atkins del Caltech Professore di Chimica e vincitore del Premio Nobel 2005 per la Chimica, che non è stato coinvolto nella ricerca. "L'ultima grande svolta nella determinazione della struttura prima di questo è stata la spettroscopia di risonanza magnetica nucleare, che è stato introdotto da Jack Roberts al Caltech alla fine degli anni '60."
Come altri chimici sintetici, Stoltz e il suo team trascorrono il loro tempo cercando di capire come assemblare sostanze chimiche in laboratorio a partire da materiali di partenza di base. Il loro laboratorio si concentra su piccole molecole naturali come la famiglia di composti beta-lattamici derivati dai funghi, che sono legati alle penicilline. Per costruire queste sostanze chimiche, hanno bisogno di determinare le strutture delle molecole nelle loro reazioni, sia le molecole intermedie che i prodotti finali, per vedere se sono sulla strada giusta.
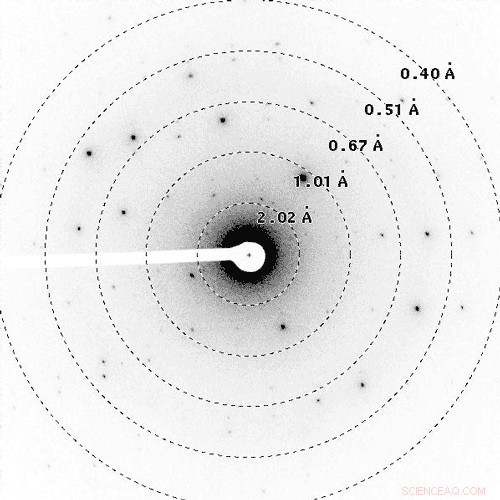
Questo film è un esempio di raccolta di dati di diffrazione elettronica (MicroED), in cui gli elettroni vengono sparati su un nanocristallo mentre vengono continuamente ruotati. I dati del film vengono infine convertiti in una struttura chimica 3-D. Credito:UCLA/Caltech
Una tecnica per farlo è la cristallografia a raggi X, in cui un campione chimico viene colpito da raggi X che diffrangono i suoi atomi; il modello di quei raggi X di diffrazione rivela la struttura 3-D della sostanza chimica mirata. Spesso, questo metodo viene utilizzato per risolvere le strutture di molecole veramente grandi, come proteine di membrana complesse, ma può essere applicato anche a piccole molecole. La sfida è che per eseguire questo metodo un chimico deve creare pezzi di cristallo di buone dimensioni da un campione, che non è sempre facile. "Una volta ho passato mesi a cercare di ottenere i cristalli giusti per uno dei miei campioni, "dice Stoltz.
Un altro metodo affidabile è NMR (risonanza magnetica nucleare), che non richiede cristalli ma richiede una quantità relativamente grande di campione, che può essere difficile da accumulare. Anche, L'NMR fornisce solo informazioni strutturali indirette.
Prima di adesso, MicroED, che è simile alla cristallografia a raggi X ma utilizza gli elettroni invece dei raggi X, è stato utilizzato principalmente su proteine cristallizzate e non su piccole molecole. Co-autore Tamir Gonen, un esperto di cristallografia elettronica all'UCLA che ha iniziato a sviluppare la tecnica MicroED per le proteine mentre era all'Howard Hughes Medical Institute in Virginia, ha detto che ha iniziato a pensare di usare il metodo su piccole molecole solo dopo essersi trasferito alla UCLA e aver collaborato con Caltech.
"Tamir aveva usato questa tecnica sulle proteine, e mi è capitato di dire che a volte possono farlo funzionare usando solo campioni polverosi di proteine, " dice Osea Nelson (Ph.D. '13), un assistente professore di chimica e biochimica all'UCLA. "La mia mente è stata colpita da questo, che non dovevi far crescere i cristalli, ed è stato all'incirca nel periodo in cui il team ha iniziato a rendersi conto che potevamo applicare questo metodo a una classe completamente nuova di molecole con implicazioni di vasta portata per tutti i tipi di chimica".
Il team ha testato diversi campioni di diverse qualità, senza mai tentare di cristallizzarli, e sono stati in grado di determinare le loro strutture grazie agli ampi microcristalli dei campioni. Sono riusciti a ottenere strutture per campioni di farmaci di marca Tylenol e Advil, e sono stati in grado di identificare strutture distinte da una miscela in polvere di quattro sostanze chimiche.
Il team UCLA/Caltech spera che questo metodo diventi di routine nei laboratori di chimica in futuro.
"Nei nostri laboratori, abbiamo studenti e dottori di ricerca che creano ogni giorno entità molecolari totalmente nuove e uniche, " dice Stoltz. "Ora abbiamo il potere di capire rapidamente cosa sono. Questo cambierà la chimica sintetica".