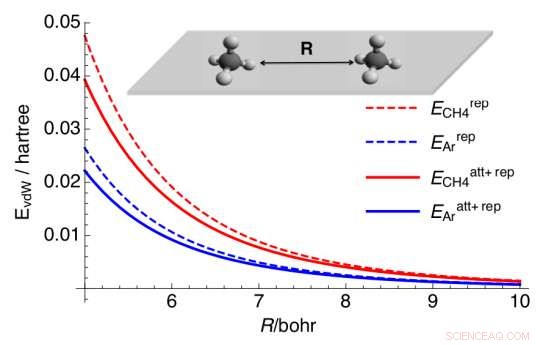
Interazione repulsiva dello stato fondamentale E rep (linee continue) e somma dell'energia di repulsione ed attrazione di Londra (E att) (linee spezzate) per dimeri di argon e metano su una superficie perfettamente riflettente. Credito:arXiv:1610.09275 [cond-mat.mes-hall]
Le interazioni di Van der Waals tra le molecole sono tra le forze più importanti in biologia, fisica, e chimica, poiché determinano le proprietà e il comportamento fisico di molti materiali. Per molto tempo, si è ritenuto che queste interazioni tra molecole siano sempre attraenti. Ora, per la prima volta, Mainak Sadhukhan e Alexandre Tkatchenko dell'Unità di ricerca in fisica e scienza dei materiali dell'Università del Lussemburgo hanno scoperto che in molte situazioni piuttosto comuni in natura la forza di van der Waals tra due molecole diventa repulsiva. Questo potrebbe portare a un cambio di paradigma nelle interazioni molecolari.
"Finora i libri di testo presumevano che le forze fossero unicamente attraenti. Per noi, la domanda interessante è se puoi anche renderli ripugnanti, " Spiega il professor Tkatchenko. "Fino a poco tempo fa, non c'erano prove nella letteratura scientifica che le forze di van der Waals potessero anche essere respinte." Ora, i ricercatori hanno mostrato nel loro articolo, pubblicato sulla rinomata rivista scientifica Lettere di revisione fisica , che le forze sono, infatti, ripugnanti quando si svolgono in reclusione.
L'onnipresente forza di van der Waals fu spiegata per la prima volta dal fisico tedesco-americano Fritz London nel 1930. Usando la meccanica quantistica, ha dimostrato la natura puramente attrattiva della forza di van der Waals per due molecole che interagiscono nello spazio libero. "Però, in natura le molecole nella maggior parte dei casi interagiscono in spazi ristretti, come le cellule, membrane, nanotubi, ecc. In questa situazione particolare, le forze di van der Waals diventano repulsive a grandi distanze tra le molecole, " dice il professor Tkatchenko.
Mainak Sadhukhan, il coautore dello studio, hanno sviluppato un nuovo metodo quantomeccanico che ha permesso loro di modellare le forze di van der Waals in confinamento. "Potremmo razionalizzare molti risultati sperimentali precedenti rimasti inspiegabili fino ad ora. La nostra nuova teoria consente, per la prima volta, per un'interpretazione di molti fenomeni interessanti osservati per le molecole sotto confinamento, " dice Mainak Sadhukhan.
La scoperta potrebbe avere molte potenziali implicazioni per la somministrazione di molecole farmaceutiche nelle cellule, desalinizzazione e trasporto dell'acqua, e autoassemblaggio di strati molecolari in dispositivi fotovoltaici.
Il gruppo di ricerca del professor Tkatchenko sta lavorando su metodi che modellano le proprietà di un'ampia gamma di interazioni intermolecolari. Solo nel 2016, hanno scoperto che la vera natura di queste forze di van der Wals differisce dalla saggezza convenzionale in chimica e biologia, in quanto devono essere trattati come accoppiamento tra onde piuttosto che come reciproca attrazione (o repulsione) tra particelle.