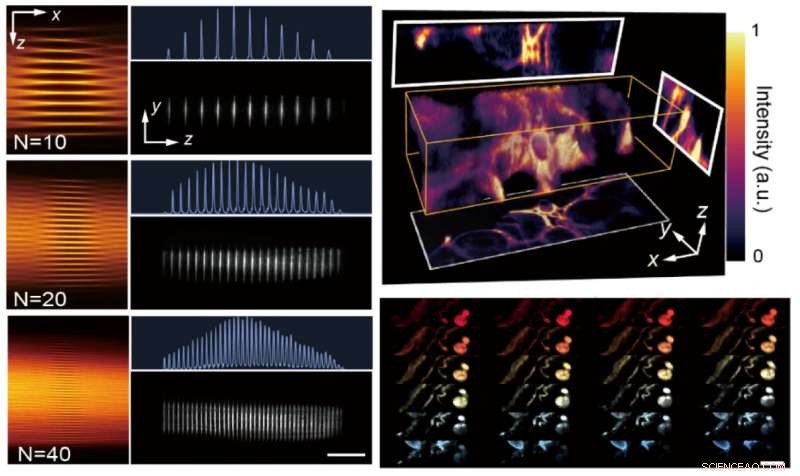
(Sinistra) Profili di illuminazione CLAM in più viste. (In alto a destra) Immagine 3D renderizzata con tre proiezioni ortogonali di intensità di deviazione standard della struttura epiteliale tubolare nel rene di topo. (In basso a destra) Immagini in sezione dei glomeruli di topo catturate dal microscopio CLAM. Credito:Y.-X. Ren, J. Wu, Q.T.K.Lai, H.M. Lai, D.M.D. Siu, W. Wu, K.K.Y.Wong, e K. K. Tsia
È ora disponibile un arsenale di strumenti di microscopia avanzati per fornire una visualizzazione di alta qualità di cellule e organismi in 3-D e ha quindi confermato la nostra comprensione dei complessi sistemi e funzioni biologici.
In un nuovo articolo pubblicato su Luce:scienza e applicazioni , un gruppo di ricerca guidato dall'Università di Hong Kong (HKU) ha sviluppato una nuova forma di modalità di imaging, microscopia a matrice di fogli di luce codificata coniata (CLAM) che consente l'imaging a fluorescenza parallela 3D completa senza alcun meccanismo di scansione, una capacità altrimenti impegnativa nelle tecniche esistenti.
Tecniche di microscopia biologica 3-D consolidate, in particolare confocale, microscopia multifotonica, e microscopia a fluorescenza a foglio luminoso (LSFM), si affidano prevalentemente alla scansione laser per l'acquisizione delle immagini. Ancora, va a scapito della velocità di imaging perché l'intero volume deve essere scansionato in sequenza punto per punto, linea per linea o piano per piano a una velocità limitata dai movimenti meccanici che coinvolgono le parti di imaging.
Persino peggio, molti approcci di scansione seriale stimolano ripetutamente la fluorescenza sfocata, e quindi accelerare il fotosbiancamento e il fotodanneggiamento. Non sono quindi favorevoli a lungo termine, imaging volumetrico su larga scala indispensabile in applicazioni diverse come la scienza anatomica, biologia dello sviluppo e neuroscienze.
La parallelizzazione 3D in CLAM richiede un'illuminazione ancora più delicata per ottenere un livello simile di sensibilità dell'immagine alla stessa frequenza di fotogrammi volumetrica. Quindi, riduce ulteriormente il tasso di fotosbiancamento e quindi il rischio di fotodanneggiamento. Questo è un attributo critico per preservare la vitalità del campione biologico negli studi di monitoraggio a lungo termine.
Il cuore di CLAM è il concetto di "specchio infinito" (cioè, una coppia di specchi paralleli), che è comune nell'arte visiva e nella decorazione, ed è stato precedentemente adottato dallo stesso team per consentire l'imaging a cellula singola optofluidico ultraveloce. Qui il team ha utilizzato lo "specchio infinito" insieme alla semplice modellazione del raggio per trasformare un singolo raggio laser in una matrice ad alta densità di poche decine di fogli di luce per l'eccitazione della fluorescenza parallela 3-D.
"Una caratteristica distintiva di CLAM è la sua capacità di riconfigurare in modo flessibile la densità spaziale e la coerenza temporale della matrice di fogli leggeri, semplicemente regolando la geometria dello specchio, come la separazione degli specchi e l'angolo di inclinazione, " ha spiegato il dottor Yuxuan Ren, il ricercatore post-dottorato e il primo autore del lavoro.
"Questa capacità è stata una sfida nei metodi di modellazione del fronte d'onda coerenti esistenti, tuttavia potrebbe consentire un efficiente LSFM 3D parallelizzato nell'imaging di tessuti sparsi con artefatti di macchioline minimi, " ha aggiunto Ren.
CLAM adotta anche il multiplexing a divisione di codice (CDM) (es. multiplexing a divisione di frequenza ortogonale dimostrato in questo lavoro), una tecnica ampiamente utilizzata nelle telecomunicazioni, per imprimere il segnale di fluorescenza da ciascun piano immagine con un codice univoco. Di conseguenza, consente l'acquisizione di immagini 3D parallelizzate con sezionamento ottico utilizzando un sensore di immagini 2D.
"CLAM non ha limiti fondamentali nel ridimensionamento a una velocità di volume più elevata poiché la tecnologia della fotocamera avanza continuamente, "Dottor Kevin Tsia, Professore Associato nel Dipartimento di Ingegneria Elettrica ed Elettronica presso HKU e il principale ricercatore del team ha sottolineato.
"Anche, CLAM può essere adattato a qualsiasi sistema LSFM esistente con modifiche hardware o software minime. Perciò, è prontamente disponibile per la diffusione alla più ampia comunità di LSFM e relative tecniche di imaging 3D, "aggiunse Tsia.