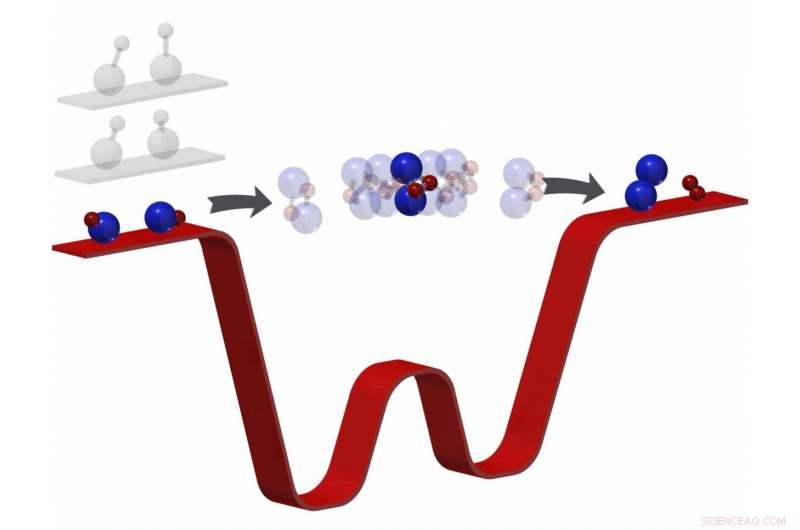
I ricercatori di Harvard scoprono che le temperature ultrafredde rallentano le reazioni chimiche a velocità lente, regalando loro un assaggio di come le molecole si trasformano e intuizioni nel mondo quantistico. Credito:Ni Lab/Università di Harvard
In una famosa parabola, tre ciechi incontrano per la prima volta un elefante. Ognuno tocca una parte:il tronco, orecchio, o di lato - e conclude che la creatura è un grosso serpente, fan, o muro. Questo elefante, disse Kang-Kuen Ni, è come il mondo quantistico. Gli scienziati possono esplorare solo una cellula di questo vasto, creatura sconosciuta alla volta. Ora, Ni ha rivelato alcuni altri da esplorare.
Tutto è iniziato lo scorso dicembre, quando lei e il suo team hanno completato un nuovo apparato in grado di ottenere le reazioni chimiche a temperatura più bassa di qualsiasi tecnologia attualmente disponibile e poi hanno rotto e formato i legami più freddi nella storia dell'accoppiamento molecolare. Ma le loro reazioni ultrafredde hanno anche inaspettatamente rallentato la reazione a una velocità lenta, regalando ai ricercatori uno sguardo in tempo reale su ciò che accade durante una trasformazione chimica. Ora, sebbene le reazioni siano considerate troppo veloci da misurare, Ni non solo ha determinato la durata di quella reazione, ha risolto un mistero ultrafreddo nel processo.
Con la chimica ultrafredda, Ni, il professore associato Morris Kahn di chimica e biologia chimica e di fisica, e il suo team ha raffreddato due molecole di potassio-rubidio appena sopra lo zero assoluto e ha trovato "l'intermedio, " lo spazio dove i reagenti si trasformano in prodotti, vissuto per circa 360 nanosecondi (ancora miliardesimi di secondo, ma abbastanza a lungo). "Non è il reagente. Non è il prodotto. È qualcosa nel mezzo, " disse Ni. Guardando quella trasformazione, come toccare il fianco di un elefante, può dirle qualcosa di nuovo su come le molecole, il fondamento di tutto, opera.
Ma non si limitavano a guardare.
"Questa cosa vive così a lungo che ora possiamo davvero giocarci un po'... con la luce, "ha detto Yu Liu, uno studente laureato presso la Graduate School of Arts and Sciences e primo autore del loro studio pubblicato in Fisica della natura . "Complessi tipici, come quelli in una reazione a temperatura ambiente, non saresti in grado di fare molto perché si dissociano in prodotti così rapidamente."
Come i raggi del trattore di Star Trek, i laser possono intrappolare e manipolare le molecole. Nella fisica ultrafredda, questo è il metodo ideale per catturare e controllare gli atomi, osservarli nel loro stato fondamentale quantistico o costringerli a reagire. Ma quando gli scienziati sono passati dalla manipolazione degli atomi al pasticcio con le molecole, accadde qualcosa di strano:le molecole iniziarono a scomparire dalla vista.
"Hanno preparato queste molecole, sperando di realizzare molte delle applicazioni che promettono:costruire computer quantistici, per esempio, ma invece quello che vedono è la perdita, " ha detto Liù.
atomi alcalini, come il potassio e il rubidio Ni e il suo studio di squadra, sono facili da raffreddare nel regno ultrafreddo. Nel 1997, gli scienziati hanno vinto un premio Nobel per la fisica per il raffreddamento e l'intrappolamento di atomi alcalini nella luce laser. Ma le molecole sono più stravaganti degli atomi:non sono solo una cosa sferica seduta lì, disse Liu, possono ruotare e vibrare. Quando intrappolati insieme nella luce laser, le molecole di gas si sono scontrate l'una contro l'altra come previsto, ma alcuni sono semplicemente scomparsi.

Professor Kang-Kuen Ni (a destra, giacca arancione) e Ming-Guang (al centro) e Yu Liu (a sinistra) hanno misurato la durata della reazione più fredda nell'universo conosciuto e, nel processo, risolto il mistero di come scompaiono alcune molecole ultrafredde. Credito:Kris Snibbe/fotografo personale di Harvard
Gli scienziati hanno ipotizzato che la perdita molecolare fosse il risultato di reazioni:due molecole si scontravano e, invece di andare in direzioni diverse, si trasformarono in nuove specie. Ma come?
"Ciò che abbiamo trovato in questo documento risponde a questa domanda, " ha detto Liu. "La stessa cosa che usi per confinare la molecola è uccidere la molecola." In altre parole, è colpa della luce
Quando Liu e Ni hanno usato i laser per manipolare quel complesso intermedio, il centro della loro reazione chimica, hanno scoperto che la luce ha forzato le molecole fuori dal loro tipico percorso di reazione e in uno nuovo. Una coppia di molecole, uniti come un complesso intermedio, possono diventare "foto-eccitati" invece di seguire il loro percorso tradizionale, ha detto Liu. Le molecole alcaline sono particolarmente sensibili a causa di quanto tempo vivono nel loro complesso intermedio.
"Fondamentalmente, se vuoi eliminare la perdita, "Liu ha detto, "Devi spegnere la luce. Devi trovare un altro modo per intrappolare queste cose." Magneti, Per esempio, o campi elettrici possono intrappolare molecole, pure. "Ma questi sono tutti tecnicamente impegnativi, " ha detto Liu. La luce è semplicemente più semplice.
Prossimo, Ni vuole vedere dove vanno a finire questi complessi quando scompaiono. Alcune lunghezze d'onda della luce (come l'infrarosso usato dal team per eccitare le loro molecole di potassio-rubidio) possono creare percorsi di reazione diversi, ma nessuno sa quali lunghezze d'onda inviano molecole in cui nuove formazioni.
Hanno anche in programma di esplorare l'aspetto del complesso nelle varie fasi di trasformazione. "Per sondare la sua struttura, "Liu ha detto, "possiamo variare la frequenza della luce e vedere come varia il grado di eccitazione. Da lì, possiamo capire dove sono i livelli di energia di questa cosa, che informa sul suo costrutto di meccanica quantistica."
"Speriamo che questo serva da sistema modello, "Ni ha detto, un esempio di come i ricercatori possono esplorare altre reazioni a bassa temperatura che non coinvolgono potassio e rubidio.
"Questa reazione è, come molte altre reazioni chimiche, una specie di universo a sé stante, " disse Liu. Ad ogni nuova osservazione, il team rivela un minuscolo pezzo del gigantesco elefante quantistico. Poiché ci sono un numero infinito di reazioni chimiche nell'universo conosciuto, c'è ancora molto tempo, lunga strada da percorrere.