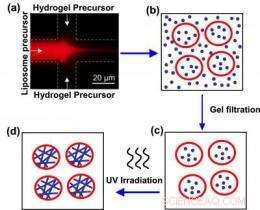
Schema raffigurante la creazione di ibridi liposomi-idrogel. Una soluzione contenente fosfolipide ("precursore liposomiale") si mescola con una soluzione contenente precursore idrogel (a). Unendo insieme all'interfaccia dei due canali, il fosfolipide forma liposomi (b) che intrappolano all'interno il precursore dell'idrogel. Il materiale esterno alle vescicole viene rimosso (c) e i liposomi vengono irradiati con raggi UV. Questo polimerizza le catene proteiche nell'idrogel e produce un ibrido liposoma-idrogel (d). Credito:NIST
Le persone hanno combinato i materiali per ottenere le migliori proprietà di entrambi da quando rame e stagno sono stati uniti per iniziare l'età del bronzo. Nell'ultima fusione di successo, ricercatori del National Institute of Standards and Technology, l'Università del Maryland e la Food and Drug Administration (FDA) statunitense hanno sviluppato un metodo per combinare due sostanze che singolarmente hanno suscitato interesse per le loro potenziali applicazioni biomediche:una "bolla" di membrana fosfolipidica chiamata liposoma e particelle di idrogel, una rete piena d'acqua di catene polimeriche. La combinazione forma una particella ibrida su nanoscala (miliardesimo di metro) che un giorno potrebbe viaggiare direttamente verso cellule specifiche come tumori, passare facilmente attraverso la membrana cellulare del bersaglio, e poi rilasciare lentamente un carico utile di droga.
In un recente articolo sulla rivista Langmuir , il team di ricerca ha esaminato il modo in cui i liposomi e le nanoparticelle di idrogel presentano vantaggi e svantaggi individuali per la somministrazione dei farmaci. Mentre i liposomi hanno proprietà superficiali utili che consentono loro di colpire cellule specifiche e passare attraverso le membrane, possono rompersi se l'ambiente circostante cambia. Le nanoparticelle di idrogel sono più stabili e possiedono capacità di rilascio controllato per regolare il dosaggio di un farmaco nel tempo, ma sono inclini al degrado e all'aggregazione. L'obiettivo dei ricercatori era progettare nanoparticelle che incorporassero entrambi i componenti per utilizzare i punti di forza di ciascun materiale compensando al contempo i loro punti deboli.
Per fabbricare le loro vescicole ibride liposomi-idrogel, i ricercatori hanno adattato una tecnica NIST-UM nota come COMANDO per la miscelazione microfluidica controllata e la determinazione delle nanoparticelle che utilizza un dispositivo microscopico fluidico (microfluidico). Nel nuovo lavoro, molecole di fosfolipidi vengono disciolte in alcol isopropilico e alimentate tramite un minuscolo (21 micrometri di diametro, o tre volte la dimensione di una cellula di lievito) canale di ingresso in un canale "mixer", poi "concentrato" in un getto fluido da una soluzione a base acquosa aggiunta attraverso due canali laterali. Le molecole precursori dell'idrogel vengono mescolate con il fluido di focalizzazione.
Poiché i componenti si fondono insieme alle interfacce dei flussi di fluido, le molecole fosfolipidiche si autoassemblano in vescicole su scala nanometrica di dimensioni controllate e intrappolano i monomeri in soluzione all'interno. Le vescicole appena formate vengono quindi irradiate con luce ultravioletta per polimerizzare i precursori idrogel che trasportano in un gel solido costituito da catene reticolate. Queste catene danno forza alle vescicole consentendo loro di mantenere la forma sferica dell'involucro liposomiale (che, a sua volta, faciliterebbe il passaggio attraverso una membrana cellulare).
Per trasformare le vescicole ibride liposoma-idrogel in veicoli di consegna cellulare, un farmaco o altro carico verrebbe aggiunto al fluido di focalizzazione durante la produzione.