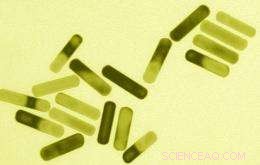
I ricercatori del MIT hanno sviluppato questi nanotubi d'oro che assorbono energia dalla luce del vicino infrarosso e la emettono sotto forma di calore, distruggere le cellule tumorali. Immagine:Laboratorio Sangeeta Bhatia; MIT
Negli ultimi 40 anni, gli scienziati hanno imparato molto su come le cellule diventano cancerose. Parte di quella conoscenza si è tradotta in nuovi trattamenti, ma la maggior parte delle volte i medici sono costretti a fare affidamento sulla chemioterapia standard e sulle radiazioni, che possono causare danni ai pazienti quasi quanto i tumori. Questa serie guarda ai trattamenti mirati che sono all'orizzonte, e cosa deve essere fatto per renderli realtà.
doxorubicina, un farmaco comunemente usato per trattare la leucemia e altri tumori, uccide le cellule tumorali danneggiando il loro DNA. Sebbene il farmaco sia efficace, può anche essere tossico per le cellule del cuore. Nel 2005, la FDA ha approvato un nuovo tipo di doxorubicina, noto come Doxil. In questa nuova formulazione, il farmaco è avvolto in un rivestimento grasso chiamato liposoma, che ostacola la sua capacità di entrare nelle cellule del cuore (e in altre cellule sane).
Doxil, di solito prescritto per il cancro ovarico in fase avanzata, rappresenta la prima generazione di trattamenti contro il cancro forniti da minuscole particelle. Le particelle di Doxil sono sulla scala dei milionesimi di metro, ma gli scienziati ora stanno lavorando su particelle di dimensioni nanometriche, che si misurano in miliardesimi di metri. Tali particelle potrebbero consentire ai medici di somministrare dosi maggiori di chemioterapia risparmiando ai tessuti sani effetti collaterali pericolosi.
Diversi farmaci a nanoparticelle sono ora in fase di sperimentazione clinica, e molti altri sono in fase di sviluppo nei laboratori di ricerca. Queste particelle hanno un grande potenziale per migliorare le prestazioni dei farmaci antitumorali esistenti, dice il medico e ingegnere Sangeeta Bhatia, il Wilson Professor di Scienze e Tecnologie della Salute e Ingegneria Elettrica e Informatica al MIT. “La chemioterapia, le radiazioni e la chirurgia sono ciò che abbiamo ora, ma la nanotecnologia sta emergendo come un approccio che integra l'armamentario esistente di strumenti clinici per avere un impatto significativo, "dice lei.
I liposomi furono scoperti per la prima volta circa 50 anni fa, ma più recentemente, gli scienziati si sono resi conto che le grandi molecole sintetiche (polimeri) come il glicole polietilenico (PEG) possono essere non tossiche e non indurre una risposta immunitaria. PEG, che consiste in una lunga catena di unità ripetitive chiamate eteri, possono essere attaccati a polimeri degradabili per formare minuscoli, particelle che rilasciano farmaci. Queste particelle sono notevolmente stabili e possono proteggere i farmaci dal sistema immunitario del corpo, che altrimenti potrebbero distruggerli prima che raggiungano la loro destinazione. Circa 15 anni fa, scienziati guidati dal professor Robert Langer dell'Istituto del MIT hanno scoperto che il PEG si presta anche alla manipolazione chimica, consentendo agli scienziati di creare particelle di somministrazione di farmaci personalizzate.
“Quando la nanoscienza ha iniziato a evolversi e siamo diventati esperti nel creare le nostre nanoparticelle, abbiamo trovato modi per progettare specificamente le nanoparticelle in modo che avessero le proprietà che volevamo, "dice Paula Hammond, il Bayer Professor of Chemical Engineering e membro del David H. Koch Institute for Integrative Cancer Research al MIT. Per esempio, gli scienziati possono progettare particelle per scaricare il carico utile del farmaco quando incontrano sacche acide all'interno di una cellula tumorale.
Gli scienziati possono anche prendere di mira le nanoparticelle specificamente per attaccare le cellule tumorali. Ci sono due modi per farlo:uno passivo e uno attivo. Negli anni '80, gli scienziati si sono resi conto che i vasi sanguigni che circondano i tumori hanno piccoli fori, fino a 500 nanometri di diametro, che consentono a piccole particelle di fluire dal flusso sanguigno nel fluido che circonda il tumore.
Mentre quel targeting passivo porta le nanoparticelle nel posto giusto, le particelle vengono lavate via dopo circa 12-24 ore, dice Hammond. “Se vuoi che la chemioterapia si avvicini al suo obiettivo, allora devi fare qualcosa per indurre la cellula cancerosa a prenderlo, "dice lei.
A quello scopo, lei e Bhatia stanno lavorando a nuovi modi per colpire attivamente le nanoparticelle decorandole con molecole che si legano alle proteine presenti in grandi quantità sulle cellule tumorali. Per esempio, possono attaccare proteine che si legano ai recettori dei folati, che si trovano ad alta densità sulle cellule tumorali perché le cellule hanno bisogno di grandi quantità di folato per produrre nuovo DNA mentre si dividono. Però, i recettori dei folati si trovano anche sulle cellule sane, in numero minore, quindi c'è ancora la possibilità di effetti collaterali indesiderati.
Per aiutare a superare questo ostacolo, un collaboratore di Bhatia, Erkki Ruoslahti dell'Università della California a Santa Barbara, ha aperto la strada a un nuovo modo per esaminare le librerie di proteine per identificare quelle che si legheranno esclusivamente alle cellule tumorali. Questo approccio ha prodotto centinaia di nuovi candidati, dice Bhatia, che è anche membro del Koch Institute e dell'Howard Hughes Medical Institute.
Molti usi per le nanoparticelle
Altri approcci nanotecnologici al cancro sfruttano le proprietà fisiche uniche di alcune nanoparticelle. Per esempio, le nanoparticelle d'oro assorbono diverse frequenze di luce a seconda della loro forma. Le particelle a forma di bastoncino assorbono la luce nel vicino infrarosso, che può passare attraverso la pelle. L'anno scorso, Bhatia e uno dei suoi studenti, Geoffrey von Maltzahn, hanno dimostrato di poter iniettare nanotubi d'oro nei topi, e che tali nanotubi si accumulerebbero nei siti tumorali. Una volta che i nanorod erano nei tumori, i ricercatori li hanno riscaldati con luce nel vicino infrarosso, alzando la temperatura a 70 gradi C, abbastanza caldo da uccidere le cellule tumorali senza danneggiare i tessuti sani vicini. La tecnica può essere utilizzata anche per l'immagine delle cellule tumorali.
Un'altra promettente applicazione per le nanoparticelle è l'interferenza dell'RNA, piccoli filamenti di RNA che possono impedire alle cellule di produrre le proteine codificate dai geni cancerosi. Basandosi su quell'idea, Hammond sta ora lavorando su nanoparticelle che fornirebbero un pugno uno-due, strati alternati di RNA e farmaci chemioterapici.
Finora, Doxil è uno dei soli due farmaci contro il cancro liposomiale ora approvato negli Stati Uniti, ma altri farmaci con nanoparticelle sono ora in fase di sperimentazione clinica. Si prevede che presto inizieranno gli studi clinici per le nanoparticelle progettate da Langer, un membro dell'Istituto Koch, Professore associato della Harvard Medical School Omid Farokhzad e altri. Queste nanoparticelle forniranno il farmaco chemioterapico docetaxel ai pazienti affetti da cancro alla prostata. Negli studi sugli animali, le particelle hanno mostrato un aumento di 20 volte della concentrazione nel sito del tumore con effetti collaterali minimi.
Come con qualsiasi nuovo tipo di trattamento medico, i ricercatori stanno anche valutando i rischi per la sicurezza. Negli ultimi anni, un nuovo campo della nanotossicologia è sorto per indagare sui rischi che le nanoparticelle potrebbero rappresentare per l'uomo. Alla nanoscala, i materiali spesso assumono nuovi tratti, ad esempio le nanoparticelle hanno un rapporto superficie-volume molto più elevato rispetto alle particelle più grandi, il che è importante perché la maggior parte della loro attività si svolge in superficie, dice Vladimir Torchilin, direttore del Center for Pharmaceutical Biotechnology and Nanomedicine presso la Northeastern University.
Però, lui dice, gli studi clinici dovrebbero rivelare se una determinata nanoparticella è sicura o pericolosa, proprio come fanno per i farmaci tradizionali. “Finora, è piuttosto difficile da dire, in anticipo, potrebbe essere pericoloso per questo, quello o quello, "dice Torchilin, chi sta sviluppando nanoparticelle per il trattamento del cancro.
Nel 2007, una task force della FDA sulla nanotecnologia ha raccomandato all'agenzia di elaborare nuove linee guida per determinare come regolamentare i prodotti nanotecnologici. Intanto, le sperimentazioni cliniche che coinvolgono le nanoparticelle stanno procedendo proprio come farebbe qualsiasi sperimentazione clinica sui farmaci. PEG, che è il componente principale di molte nanoparticelle che rilasciano farmaci, appartiene alla categoria FDA delle sostanze “generalmente riconosciute come sicure”.
Hammond è ottimista sul fatto che la nanotecnologia finirà per aiutare i malati di cancro, possibilmente entro i prossimi tre-cinque anni. "Penso che fornisca troppi vantaggi per noi per liberarcene, "dice lei.