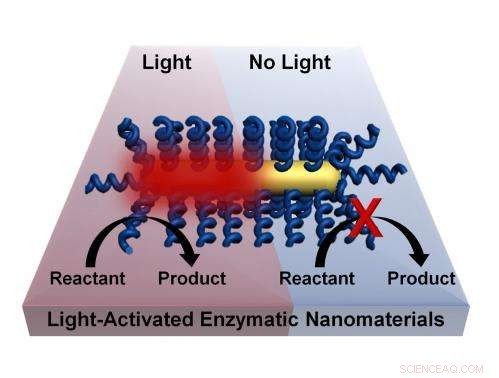
I processi chimici possono essere attivati dalla luce senza la necessità di riscaldare in massa un materiale attraverso un processo sviluppato dai ricercatori della Rice University. La tecnica prevede il rivestimento di nanotubi con enzimi termofili che vengono attivati ad alte temperature. L'accensione del nanorod d'oro plasmonico provoca un riscaldamento altamente localizzato e attiva l'enzima. Credito:Lori Pretzer/Rice University
(Phys.org)—Dalla prima lampadina di Edison, il calore è stato un sottoprodotto per lo più indesiderabile della luce. Ora i ricercatori della Rice University stanno trasformando la luce in calore nel momento del bisogno, su scala nanometrica, per innescare reazioni biochimiche a distanza su richiesta.
Il metodo creato dai laboratori Rice di Michael Wong, Ramon Gonzalez e Naomi Halas e riportato oggi sulla rivista dell'American Chemical Society ACS Nano utilizza materiali derivati da microbi unici – i termofili – che prosperano ad alte temperature ma si spengono a temperatura ambiente.
Il progetto Rice, guidato dal borsista post-dottorato Matthew Blankschien e dallo studente laureato Lori Pretzer, combina gli enzimi di queste creature con nanoparticelle d'oro plasmoniche che si riscaldano se esposte alla luce del vicino infrarosso. Che attiva gli enzimi, che sono poi in grado di svolgere le loro funzioni.
Ciò consente effettivamente che i processi chimici avvengano a temperature più basse. Poiché il riscaldamento avviene solo dove necessario:sulla superficie della nanoparticella, dove attiva l'enzima - l'ambiente rimane più fresco.
Blankschien pensa che sia affascinante.
"Fondamentalmente, stiamo ottenendo i vantaggi della produzione ad alta temperatura senza bisogno di un ambiente ad alta temperatura, "disse Blankschien, che ha vinto il Peter and Ruth Nicholas Postdoctoral Fellowship due anni fa per lavorare su queste idee. "La sfida era mantenere la temperatura più alta alla nanoparticella, dove viene attivato l'enzima, dall'influenzare l'ambiente circostante."
La tecnica ha un grande potenziale per i processi industriali che ora richiedono calore o beneficiano dell'attivazione a distanza con la luce.
"Le implicazioni sono piuttosto eccitanti, " ha detto Wong, professore di ingegneria chimica e biomolecolare e di chimica. "Nel settore chimico, c'è sempre bisogno di materiali catalitici migliori in modo che possano eseguire reazioni in modo più economico, più "verde" e più sostenibile. Non dovresti usare litri di solvente per fare un milligrammo di prodotto, anche se riesci a venderlo per un sacco di soldi."
Per l'industria, il potenziale risparmio energetico da solo può rendere il processo del riso degno di essere studiato. "Qui stiamo usando energia 'gratuita', " disse Wong. "Invece di aver bisogno di una grande caldaia per produrre vapore, accendi una lampadina a risparmio energetico, come un LED. Oppure apri una finestra".
La particella al centro del processo è una nanobarra d'oro larga circa 10 nanometri e lunga 30 che si riscalda quando viene colpita dalla luce nel vicino infrarosso di un laser. I bastoncini hanno le dimensioni e la forma giuste per reagire alla luce a circa 800 nanometri. La luce eccita i plasmoni di superficie che si increspano come l'acqua in una piscina, in questo caso emettendo energia sotto forma di calore.
Il laboratorio Rice di Halas è famoso per aver aperto la strada all'uso di nanoshell d'oro (un materiale correlato) per curare il cancro prendendo di mira i tumori con particelle che vengono riscaldate in massa per uccidere i tumori dall'interno. La terapia è ora in sperimentazione umana.
La nuova ricerca prende una virata in qualche modo diversa riscaldando nanoparticelle avvolte con un enzima termofilo modello, glucochinasi, di Aeropyrum pernix. A. pernix è un microbo scoperto nel 1996 che prospera vicino a calde bocche sottomarine al largo della costa del Giappone. A circa 176 gradi Fahrenheit, A. pernix degrada il glucosio, un processo necessario a quasi tutti gli esseri viventi. L'enzima può essere riscaldato e raffreddato ripetutamente.
Nei loro esperimenti, Blankschien e Pretzer clonarono, enzimi glucochinasi purificati e alterati in modo che si attacchino alle nanoparticelle d'oro. I complessi enzima/nanoparticelle sono stati quindi sospesi in una soluzione e testati per la degradazione del glucosio. Quando la soluzione è stata riscaldata alla rinfusa, hanno scoperto che i complessi sono diventati altamente attivi a 176 gradi, come previsto.
Quindi i complessi sono stati incapsulati in una perlina gelatinosa di alginato di calcio, che aiuta a trattenere il calore, ma è abbastanza poroso da consentire agli enzimi di reagire con i materiali circostanti. Sotto riscaldamento di massa, le prestazioni degli enzimi sono diminuite drasticamente perché le perline hanno isolato troppo bene gli enzimi.
Ma quando i complessi incapsulati erano illuminati da continui, luce laser nel vicino infrarosso, hanno funzionato sostanzialmente meglio rispetto al riscaldamento di massa lasciando la soluzione a temperatura quasi ambiente. I ricercatori hanno scoperto che i complessi sono abbastanza robusti per settimane di riutilizzo.
"Per quanto inverosimile possa sembrare, Penso che le aziende chimiche saranno interessate all'idea di utilizzare la luce per produrre sostanze chimiche, " Ha detto Wong. "Sono sempre interessati a nuove tecnologie che possono aiutare a rendere i prodotti chimici più economici".
Vede altri possibili utilizzi per il nuovo approccio nella produzione di combustibili dalla degradazione di biomasse come la lignocellulosa; per la produzione di farmaci su richiesta – forse da tatuaggi infusi con nanoparticelle sul corpo; o anche per abbassare le concentrazioni di zucchero nel sangue come un modo diverso per gestire il diabete.
"Che ora possiamo creare queste particelle è fantastico, " Ha detto Wong. "La prossima parte emozionante è pensare a come possiamo distribuirli".
Ryan Huschka, un coautore del documento, è un ex studente laureato della Rice e ora assistente professore di chimica alla Newman University. Halas è lo Stanley C. Moore Professor in Ingegneria Elettrica e Informatica, professore di ingegneria biomedica, chimica, fisica e astronomia e direttore del Laboratorio di Nanofotonica di Rice. Gonzales è professore associato di ingegneria chimica e biomolecolare e anche di bioingegneria
La ricerca è stata supportata dal Peter and Ruth Nicholas Postdoctoral Fellowship Program amministrato dal Richard E. Smalley Institute for Nanoscale Science and Technology, il Rice University Institute of Biosciences and Bioengineering Hamill Innovations Award Program, il Fondo per le iniziative dei docenti della Rice University, la Fondazione Robert A. Welch, la borsa di studio della Facoltà di scienze e ingegneria della sicurezza nazionale, l'Agenzia per la riduzione delle minacce alla difesa, l'Air Force Office of Scientific Research e la National Science Foundation.