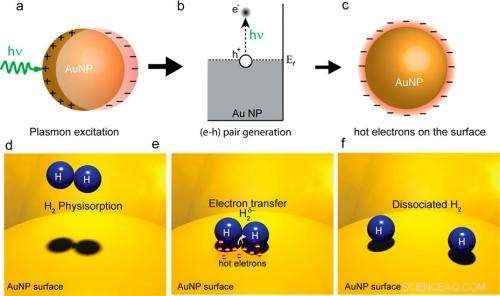
In un), (B), e C), plasmoni di superficie eccitati da un laser generano elettroni caldi su una superficie di nanoparticelle d'oro. In (d), (e), e (f), gli elettroni caldi si trasferiscono alle molecole di H2 e le fanno dissociare. Poiché la dissociazione è la fase limitante in molte reazioni chimiche, questo processo di elettroni caldi può aumentare l'efficienza della reazione. Credito immagine:Shaunak Mukherjee, et al. ©2012 American Chemical Society
(Phys.org)—Dalla raffinazione del petrolio alla lavorazione degli alimenti, la stragrande maggioranza delle applicazioni chimiche commerciali coinvolge i catalizzatori per controllare la velocità delle reazioni chimiche. Tutto ciò che può aumentare l'efficienza dei catalizzatori potrebbe avere un impatto diffuso in queste aree. In un nuovo studio, gli scienziati hanno dimostrato che un miglioramento dell'efficienza può essere possibile creando elettroni "caldi" (quelli con un'energia molto elevata) da una superficie metallica su cui avviene la reazione chimica, e usando gli elettroni per controllare la reazione chimica e renderla più efficiente.
I ricercatori, guidato dai professori Peter Nordlander e Naomi J. Halas della Rice University di Houston, Texas, e la professoressa Emily A. Carter della Princeton University, New Jersey, hanno pubblicato il loro studio sulla tecnica per migliorare la chimica catalitica in un recente numero di Nano lettere .
Nel loro metodo, i ricercatori hanno utilizzato un laser a luce visibile per illuminare una superficie di nanoparticelle d'oro (la superficie del catalizzatore) a temperatura ambiente. La luce laser in arrivo eccita otticamente i plasmoni di superficie sulla superficie metallica, e i plasmoni poi decadono in elettroni caldi. A causa delle loro alte energie, gli elettroni caldi si estendono più lontano dalle nanoparticelle rispetto agli elettroni con energie più basse. Se un altro atomo o molecola che può accettare l'elettrone è vicino, l'elettrone caldo può trasferirsi negli stati elettronici di quell'accettore.
In questi esperimenti, i ricercatori hanno adsorbito H 2 molecole sulla superficie delle nanoparticelle d'oro, una procedura che viene comunemente eseguita nella catalisi eterogenea, in cui le molecole adsorbite agiscono come reagenti. I ricercatori hanno scoperto, come risultato principale del loro studio, che alcuni degli elettroni caldi potrebbero trasferirsi nei gusci chiusi dell'H 2 molecole e far separare i due atomi di idrogeno, o dissociarsi. Questo processo, chiamata "dissociazione indotta da plasmoni di H 2 su Au, " potrebbe migliorare l'efficienza di alcune reazioni chimiche.
"In molte importanti reazioni chimiche, il fattore limitante è la dissociazione di molecole a guscio chiuso come una molecola di idrogeno, " ha detto Nordlander Phys.org . "Se questa fase di reazione può essere 'affrontata' (usando il nostro processo dimostrato di elettroni caldi), la reazione può procedere molto più velocemente e richiedere meno energia."
Per misurare la dissociazione, i ricercatori hanno esposto il substrato di nanoparticelle sia a H 2 e D 2 (due atomi di deuterio, un isotopo di idrogeno contenente un neutrone). Se gli elettroni caldi dissociassero queste molecole, comporterebbe la formazione di molecole HD. I ricercatori hanno scoperto che, non appena hanno acceso il laser, il tasso di formazione di HD sulla superficie delle nanoparticelle è aumentato di un fattore 6. Hanno anche misurato che il tasso era fortemente dipendente dalla concentrazione e dalle dimensioni delle nanoparticelle d'oro. I ricercatori hanno spiegato che, in un senso, gli elettroni "fanno l'impossibile" perché senza di loro non ci sarebbe dissociazione.
"Una molecola di idrogeno adsorbita su una superficie d'oro macroscopica non si dissocia spontaneamente, anche a temperature elevate, " ha detto Nordlander. "È una reazione chimica impossibile. L'energia per la dissociazione è semplicemente troppo grande. Abbiamo scelto il sistema idrogeno-oro proprio per questo motivo. Volevamo un sistema in cui l'interpretazione dell'effetto fosse semplice. Su altri metalli, come i metalli di transizione, una molecola di idrogeno può dissociarsi spontaneamente, in particolare in prossimità di difetti e ad elevate temperature. Ma non sull'oro".
Questi risultati dimostrano come il campo della plasmonica – che prevede interazioni tra fotoni e nanostrutture – possa avere applicazioni nel campo della chimica catalitica, in particolare fotocatalisi, I ricercatori sperano che questa dimostrazione della capacità di controllare le reazioni chimiche usando la luce possa essere estesa per usi specifici. Usando la frequenza laser per sintonizzare le risonanze plasmoniche di superficie, potrebbe essere possibile creare elettroni caldi con energie specifiche che popolano stati elettronici specifici di molecole adsorbite sulla superficie delle nanoparticelle.
"L'applicazione immediata è quella di migliorare l'efficienza dei catalizzatori metallici illuminandoli con la luce, " Ha detto Nordlander. "I nostri gruppi hanno un'"agenda verde" e il nostro intento è quello di progettare nuovi tipi di catalizzatori guidati dalla luce solare. Questo è qualcosa di cui abbiamo abbondanza qui a Houston.
"Un'altra importante applicazione è quella di indagare fino a che punto possiamo guidare e controllare le reazioni chimiche facendo trasferire elettroni caldi di particolari energie in specifici orbitali molecolari. Questo è un argomento di ricerca relativamente inesplorato. Gli elettroni normali hanno energie positive e sono molto più "caldi" che i nostri elettroni caldi. Tali elettroni ad alta energia in genere non rimangono su una molecola sufficientemente a lungo perché gli atomi inizino a muoversi".
Copyright 2012 Phys.org
Tutti i diritti riservati. Questo materiale non può essere pubblicato, trasmissione, riscritto o ridistribuito in tutto o in parte senza l'espresso permesso scritto di Phys.org.