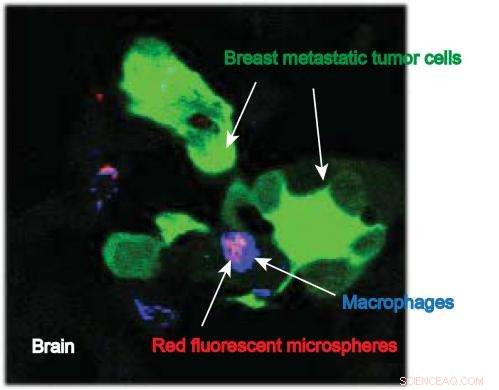
Questa immagine della ricercatrice della IU School of Medicine, Susan Clare, mostra macrofagi che trasportano nanoparticelle (con un colorante fluorescente attaccato) nel sito delle cellule metastatiche del tumore al seno nel cervello. Credito:Susan Clare, M.D., dottorato di ricerca
Un chirurgo del cancro al seno della Indiana University School of Medicine sta portando avanti una ricerca che utilizzerà il vetro, oro, nanotecnologia e mitologia greca nella speranza di sconfiggere il cancro al seno che ha metastatizzato al cervello.
Susan E. Chiara, M.D., dottorato di ricerca, professore associato di chirurgia presso la IU School of Medicine, è l'iniziatore investigatore principale per $ 573, 000 Borsa di studio del Dipartimento della Difesa che le consentirà di esplorare un nuovo approccio alla somministrazione di una terapia alle metastasi cerebrali da carcinoma mammario primario.
Come facevano gli antichi greci, La dottoressa Clare spera di consegnare segretamente "guerrieri" alla roccaforte nemica, in questo caso un tumore cerebrale metastatico. La sua ricerca esplorerà l'uso di una cellula del sistema immunitario del corpo per somministrare la chemioterapia direttamente alle metastasi cerebrali. Il farmaco o altro terapeutico è attaccato alle nanosfere, che sono trasportati all'interno della cellula immunitaria, proprio come i soldati venivano trasportati all'interno del cavallo di Troia. Le cellule immunitarie viaggiano nel flusso sanguigno e rilasciano il farmaco quando ha raggiunto il sito del tumore.
I due tipi di cancro al seno che più comunemente metastatizzano al cervello sono HER2 positivo e triplo negativo. Non esiste un trattamento specificamente mirato disponibile per il trattamento dei tumori metastatici tripli negativi, ma lapatinib è un trattamento standard per il cancro HER2 positivo che si è diffuso ad altre parti del corpo.
"Il problema per quasi tutti i farmaci, e i farmaci HER2-mirati non fanno eccezione, è che la barriera emato-encefalica è un ostacolo significativo alla somministrazione di terapie in concentrazioni che possono essere efficaci, " Ha detto la dott.ssa Clare. Quel problema biologico ha portato la dott.ssa Clare a esplorare altri metodi per somministrare farmaci ai tumori cerebrali metastatici.
Utilizzando nanoparticelle chiamate "nanoshells, " sviluppato da Naomi J. Halas, dottorato di ricerca, D.Sc., direttore del Laboratorio di Nanofotonica della Rice University, La dottoressa Clare spera di colpire i tumori cerebrali con lapatinib a una dose sufficiente per interrompere la via di segnalazione necessaria per la proliferazione delle cellule tumorali.
In un articolo di luglio sulla rivista Nanotecnologia del cancro , Dott. Clare e Halas e colleghi hanno dimostrato che le cellule immunitarie che trasportano le nanoparticelle sono state in grado di attraversare la barriera emato-encefalica e raggiungere le metastasi cerebrali in un modello sperimentale di topo.
Primo, viene raccolto un componente dei globuli bianchi chiamati macrofagi, cellule versatili che avviano una risposta immunitaria dopo l'infiltrazione di cellule anormali (cancerose). Le nanoparticelle vengono ingerite dai macrofagi, che vengono poi rilasciati nel flusso sanguigno. La dottoressa Clare ha detto che i macrofagi sono attratti dalle metastasi da agenti chemiotattici, che sono sostanze chimiche prodotte dal tumore.
Queste nanoparticelle sono in studi clinici di Fase I per il trattamento del cancro della testa e del collo, carcinoma prostatico avanzato e carcinoma polmonare attraverso Nanospectra Biosciences, con sede a Houston, Texas. Poiché si pensava che la barriera emato-encefalica fosse un ostacolo significativo al parto, la loro efficacia del trattamento per le metastasi cerebrali non è stata inclusa nei test iniziali. La sovvenzione del Dipartimento della Difesa del Dr. Clare consentirà la ricerca in tre aree chiave.
Il primo obiettivo è dimostrare che i farmaci chemioterapici possono essere legati alle nanoparticelle e rilasciati a piacimento nel punto appropriato nel cervello, ha detto la dottoressa Clare. Il rilascio "a volontà" è fondamentale nel processo.
"Il farmaco viene rilasciato dalla particella puntando un laser sulla particella, " ha detto. "Il farmaco viene trasportato tra due pezzi di DNA che sono caricati negativamente. Quando esposto alla luce laser, gli elettroni si spostano dalla nanoparticella al DNA, permettendogli di rilasciare il farmaco."
I macrofagi portano la nanoparticella direttamente alle cellule cancerose, quindi quando il farmaco viene rilasciato, è esattamente dove deve essere per diffondere al tumore e interrompere l'attività cellulare delle cellule metastatiche.
Per quanto semplice possa sembrare, non è.
La nanoparticella è una palla di silice ricoperta d'oro, che ha dimostrato di essere non tossico in un ampio, studi scientifici a lungo termine. Lo spessore del guscio d'oro determina dove sullo spettro della luce viene assorbita la luce laser. Per la massima penetrazione nei tessuti, le nanoparticelle dovrebbero assorbire la luce nel vicino infrarosso. Le nanoparticelle sviluppate dal Dr. Halas fanno proprio questo.
Però, l'osso del cranio rappresenta un'ulteriore sfida per fornire una potenza laser sufficiente alla nanoparticella. Aumentare la potenza del laser non è la risposta perché brucerà la pelle. Ci sono molte variabili per l'enigma, ma la dottoressa Clare ha assunto Keith Stantz, dottorato di ricerca, assistente professore a contratto di radiologia presso l'Indiana Institute of Biomedical Imaging Sciences, e Jacqueline A. Johnson, dottorato di ricerca, professore associato presso l'University of Tennessee Space Institute, entrambi sono esperti in laser a nanosecondi e femtosecondi. Il team crede di avere una soluzione alla sfida del potere e la testerà su modelli murini.
"Questo è un grande pezzo del puzzle, " Dr. Clare ha detto. "L'oro è usato come guscio per la particella a causa delle sue proprietà fisiche. Calcoli precisi per lo spessore dell'oro, la profondità di penetrazione ideale e la potenza del laser erano sfide che dovevano essere risolte prima di poter studiare l'efficacia del sistema di somministrazione del farmaco".