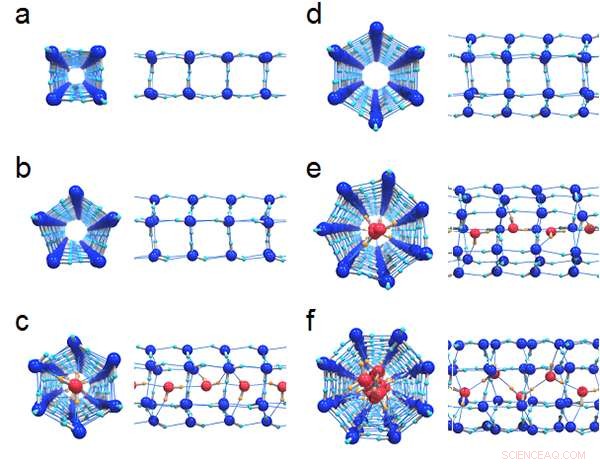
Figura 1:Strutture del legame idrogeno di sei ghiacci formati nei nanotubi:(a) (4, 0) ghiaccio, (b) (5, 0) ghiaccio e (c) pieno (6, 0) ghiaccio con un diametro di 1,11 nm, (d) (6, 0) ghiaccio, (e) pieno (7, 0) ghiaccio e (f) riempito (8, 0) ghiaccio con un diametro di 1,25 nm. Le viste dall'alto e la vista laterale corrispondente sono affiancate. Le molecole d'acqua centrali che formano una catena nei ghiacci pieni sono colorate di rosso per distinguerle dagli anelli esterni.
Molti fisici non accettano l'idea che un confine di fase solido-liquido possa terminare in un punto critico, uno stato unico in cui due fasi perdono le loro identità separate. Perché non lo fanno? L'autorevole testo di Landau e Lifshitz afferma che "si può dire solo che una particolare proprietà di simmetria esiste o esiste; ... Il punto critico quindi non può esistere per tali fasi". Ma dal 2001, la possibilità del punto critico solido-liquido è stata riportata in studi di simulazione al computer dell'acqua nei nanopori. Infatti, non vi è alcuna prova rigorosa dell'inesistenza del punto critico solido-liquido.
Kenji Mochizuki e Kenichiro Koga dell'Università di Okayama hanno fornito prove inequivocabili a sostegno del punto critico solido-liquido per una classe di acqua nei nanotubi eseguendo ampie simulazioni di dinamica molecolare:separazione macroscopica di fase solido-liquido al di sotto di una temperatura critica Tc, capacità termica divergente e compressibilità isotermica intorno a Tc, ei loci della funzione di risposta maxima (le linee Widom) sopra Tc.
La Figura 1 mostra le strutture del legame idrogeno di sei cristalli di ghiaccio formati in nanotubi di carbonio con diametri di 1,11 nm e 1,25 nm. I ricercatori hanno scoperto che tutti i confini di fase di primo ordine tra il ghiaccio e il liquido alla fine hanno cessato di esistere nei punti critici, come mostrato in Figura 2. Il diagramma di fase T-P è molto diverso da quello dell'acqua sfusa, dove le regioni di ghiaccio sono completamente circondate dai confini di fase del primo ordine (linee nere continue).
I ricercatori hanno anche fornito una spiegazione microscopica a un semplice, ancora senza risposta, domanda:come può l'acqua liquida congelarsi continuamente in ghiaccio cristallino? Hanno trovato fluttuazioni dinamiche di domini microscopici di acqua e ghiaccio vicino al punto critico, un'immagine microscopica dell'acqua nel corso di un graduale congelamento o scioglimento.
I punti critici in acque confinate sono onnipresenti e possono essere individuati in condizioni ambientali regolando il diametro dei pori, e quindi una delle potenziali applicazioni è quella di utilizzare le fluttuazioni critiche sintonizzabili per facilitare le reazioni chimiche, cambiamenti strutturali nelle molecole biologiche, e formazione di assemblaggio di biomolecole in acqua.
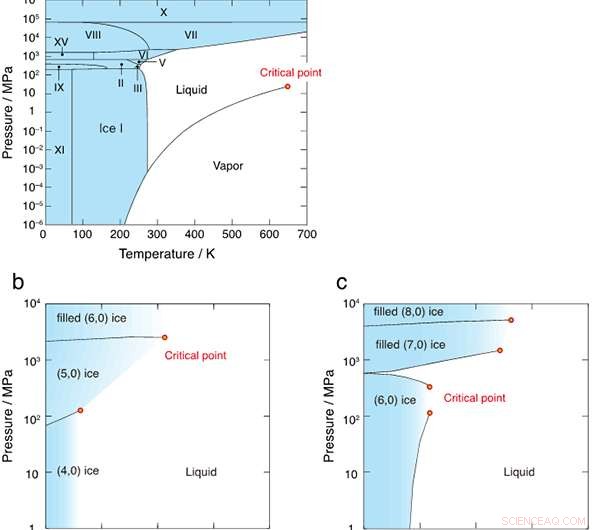
Figura 2:diagrammi di fase di (a) acqua sfusa, (b) acqua confinata nel nanotubo di un diametro di 1,11 nm, e (c) 1,25 nm. I diagrammi di fase di (b) e (c) sono inizialmente rivelati in questo studio. Le regioni solide sono colorate in blu e i punti critici sono indicati da cerchi rossi.