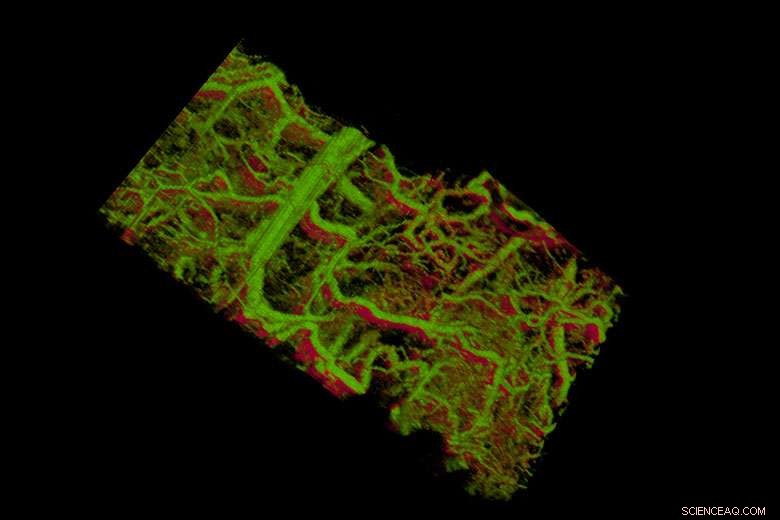
I nanotubi d'oro all'interno dei vasi sanguigni di un orecchio di topo appaiono verdi. L'angolo inferiore destro mostra i vasi all'interno di un tumore che si trova sotto la pelle. Crediti:de la Zerda lab
Gli scienziati hanno molti strumenti a loro disposizione per osservare i tessuti conservati al microscopio con dettagli incredibili, o scrutare il corpo vivente a una risoluzione inferiore. Quello che non hanno avuto è un modo per fare entrambe le cose:creare un'immagine tridimensionale in tempo reale di singole cellule o persino molecole in un animale vivente.
Ora, Gli scienziati di Stanford hanno fornito il primo sguardo sotto la pelle di un animale vivente, mostrando intricati dettagli in tempo reale in tre dimensioni della linfa e dei vasi sanguigni.
La tecnica, chiamato MOZART (per l'imaging molecolare e la caratterizzazione dei tessuti in modo non invasivo a risoluzione cellulare), potrebbe un giorno consentire agli scienziati di rilevare i tumori della pelle, colon o esofago, o anche per vedere i vasi sanguigni anormali che compaiono nelle prime fasi della degenerazione maculare, una delle principali cause di cecità.
"Abbiamo cercato di esaminare il corpo vivente e vedere le informazioni a livello della singola cellula, " disse Adam de la Zerda, un assistente professore di biologia strutturale a Stanford e autore senior della carta. "Finora non c'è stato modo di farlo."
De la Zerda, che è anche membro di Stanford Bio-X, ha affermato che la tecnica potrebbe consentire ai medici di monitorare come un tumore altrimenti invisibile sotto la pelle sta rispondendo al trattamento, o per capire come le singole cellule si liberano da un tumore e viaggiano in siti distanti.
Andando per l'oro
Esiste una tecnica per sbirciare in un tessuto vivo diversi millimetri sotto la pelle, rivelando un paesaggio di cellule, tessuti e vasi. Ma quella tecnica, chiamata tomografia a coerenza ottica, o ottobre, non è abbastanza sensibile o specifico per vedere le singole cellule o le molecole che le cellule stanno producendo, che è ciò che interessa a de la Zerda.
Un problema importante è stato trovare un modo per differenziare tra cellule o tessuti; Per esempio, individuando le cellule cancerose che iniziano a moltiplicarsi all'interno di un tessuto complessivamente sano. In altre forme di microscopia, gli scienziati hanno creato tag che si agganciano a molecole o strutture di interesse per illuminare tali strutture e fornire una visione dettagliata di dove si trovano nella cellula o nel corpo.
Non esistevano tali beacon per OCT, sebbene de la Zerda sapesse che minuscole particelle chiamate nanobarre d'oro avevano alcune delle proprietà che stava cercando. Il problema era che le nanobarre disponibili in commercio non producevano un segnale quasi sufficiente per essere rilevate in un tessuto.
Ciò di cui il team aveva bisogno erano nanotubi, ma grandi. I nanorodi sono analoghi alle canne d'organo, ha detto lo studente laureato Elliott SoRelle, perché i tubi più lunghi vibrano a frequenze più basse, creando un profondo, suono basso. Allo stesso modo, nanobarre più lunghe vibrano a frequenze più basse, o lunghezze d'onda, di luce. Quelle vibrazioni disperdono la luce, che il microscopio rileva.
Se tutti gli altri tessuti vibrano in un rumore bianco di frequenze più alte, nanobarre più lunghe risaltavano come note di organo basse in una stanza di chiacchiere.
La sfida di SoRelle era quella di produrre nanobarre più lunghe che non fossero tossiche, stabile e molto luminoso, che si è rivelato essere molto da chiedere. "Il mio background era la biochimica, e questo si è rivelato essere un problema di scienza dei materiali e chimica di superficie, " ha detto SoRelle, che è stato co-primo autore della carta. Ora può creare nanobarre non tossiche di varie dimensioni che vibrano tutte a frequenze uniche e identificabili.
Eliminazione del rumore
La sfida successiva è stata filtrare la frequenza delle nanobarre dal tessuto circostante.
Fare quello, Orly Liba, studente laureato in ingegneria elettrica e Bowes Bio-X Fellow, ha sviluppato algoritmi informatici in grado di separare le frequenze della luce diffusa da nanobarre di varie lunghezze e differenziarle dal tessuto circostante.
Con i grandi nanorod di SoRelle e gli algoritmi sensibili di Liba, de la Zerda e il suo team avevano risolto il problema iniziale di rilevare strutture specifiche in immagini tridimensionali di tessuti viventi. La risultante tridimensionale, le immagini ad alta risoluzione erano così grandi, dell'ordine dei gigapixel, che il team aveva bisogno di sviluppare algoritmi aggiuntivi per analizzare e archiviare immagini così grandi.
Il team ha testato la loro tecnologia nell'orecchio di un topo vivente, dove sono stati in grado di osservare come i nanotubi venivano assorbiti nel sistema linfatico e trasportati attraverso una rete di valvole. Sono stati in grado di distinguere tra due nanobarre di dimensioni diverse che risuonano a diverse lunghezze d'onda in vasi linfatici separati, e potevano distinguere tra quelle due nanobarre nel sistema linfatico e nei vasi sanguigni. In uno studio, potevano osservare le singole valvole all'interno dei vasi linfatici aprirsi e chiudersi per controllare il flusso del fluido in un'unica direzione.
"Nessuno ha mostrato quel livello di dettaglio prima, " ha detto Liba, che è stato co-primo autore della carta.
Obiettivo impossibile
Questo imaging dettagliato era l'obiettivo iniziale di de la Zerda quando ha avviato il suo laboratorio nel 2012, anche se spesso gli veniva detto che sarebbe stato impossibile. "Sono in un piccolo reparto, ma con facoltà molto esperte, " ha detto. "Un membro della facoltà mi ha raccontato la sua storia di vita di prendere grandi rischi e che mi ha incoraggiato. Ho pensato che sarebbe stato davvero divertente vedere se riusciamo a farlo funzionare e vedere le cellule che parlano tra loro in tempo reale".
La sua scommessa è decollata principalmente con una borsa di studio della Stanford Bio-X, che supporta la ricerca interdisciplinare in fase iniziale. "Quella sovvenzione ci ha permesso di correre un grosso rischio in una direzione che era completamente non dimostrata, " disse de la Zerda.
Avendo dimostrato che i nanotubi d'oro possono essere visti nei tessuti viventi, il prossimo passo è mostrare che quei nanorod possono legarsi a specifici tipi di cellule, come il cancro della pelle o vasi anormali nella degenerazione maculare in fase iniziale. Quindi, la tecnica potrebbe essere utilizzata per saperne di più su come queste malattie progrediscono a livello molecolare e anche per valutare i trattamenti nei singoli pazienti, qualcosa che prima non era possibile.