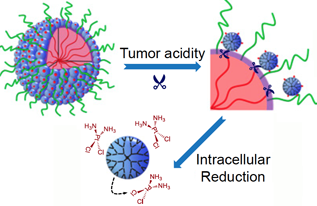
Le particelle iniziano grandi (100 nm) per consentire un trasporto regolare nel tumore attraverso i vasi sanguigni che perdono. Quindi, in condizioni acide trovate vicino ai tumori, le particelle scaricano bombe di 5 nm. All'interno delle cellule tumorali, un secondo passaggio chimico attiva il cisplatino. Credito:Jinzhi Du/Wallace H. Coulter Dipartimento di ingegneria biomedica presso Georgia Tech ed Emory
Gli scienziati hanno ideato un sistema "bomba a grappolo" a triplo stadio per la somministrazione del farmaco chemioterapico cisplatino, tramite minuscole nanoparticelle progettate per rompersi quando raggiungono un tumore.
I dettagli del design delle particelle e della loro potenza contro il cancro nei topi sono stati pubblicati il 28 marzo in PNAS . Non sono stati testati sull'uomo, sebbene modi simili di confezionamento del cisplatino siano stati in studi clinici.
Ciò che rende distintive queste particelle è che all'inizio sono relativamente grandi (100 nanometri di larghezza) per consentire un trasporto regolare nel tumore attraverso i vasi sanguigni che perdono. Quindi, in condizioni acide trovate vicino ai tumori, le particelle scaricano "bombe" di appena 5 nanometri.
All'interno delle cellule tumorali, un secondo passaggio chimico attiva il cisplatino a base di platino, che uccide reticolando e danneggiando il DNA. I medici hanno usato per decenni il cisplatino per combattere diversi tipi di cancro, ma effetti collaterali tossici - ai reni, nervi e orecchio interno, possono limitarne l'efficacia.
Il PNAS paper è il risultato di una collaborazione tra e un team guidato dal professor Jun Wang, Dottorato di ricerca presso l'Università della Scienza e della Tecnologia della Cina, e ricercatori guidati dal professor Shuming Nie, Dottorato di ricerca presso il Dipartimento di Ingegneria Biomedica di Wallace H. Coulter presso la Georgia Tech and Emory. Nie è membro del programma di ricerca Discovery and Developmental Therapeutics presso il Winship Cancer Institute della Emory University. Gli autori principali sono lo studente laureato Hong-Jun Li e i borsisti post-dottorato Jinzhi Du, PhD e Xiao-Jiao Du, dottorato di ricerca.
"Gli effetti collaterali negativi del cisplatino sono una limitazione di vecchia data per la chemioterapia convenzionale, " dice Jinzhi Du. "Nel nostro studio, il sistema di consegna è stato in grado di migliorare la penetrazione del tumore per raggiungere più cellule tumorali, oltre a rilasciare i farmaci specificamente all'interno delle cellule tumorali attraverso la loro proprietà di transizione dimensionale".
I ricercatori hanno dimostrato che le loro nanoparticelle potrebbero aumentare l'accumulo di farmaco cisplatino nei tessuti tumorali. Quando a topi portatori di tumori pancreatici umani sono state somministrate le stesse dosi di cisplatino libero o cisplatino rivestiti di nanoparticelle sensibili al pH, il livello di platino nei tessuti tumorali era sette volte superiore con le nanoparticelle. Ciò suggerisce la possibilità che la somministrazione di nanoparticelle di una dose limitata di cisplatino possa limitare gli effetti collaterali tossici durante il trattamento del cancro.
I ricercatori hanno anche dimostrato che le nanoparticelle erano efficaci contro un modello di cancro ai polmoni resistente al cisplatino e un modello di cancro al seno metastatico invasivo nei topi. Nel modello del cancro del polmone, una dose di cisplatino libero ha prodotto solo il 10% di inibizione della crescita, mentre la stessa dose rivestita di nanoparticelle ha prodotto un'inibizione della crescita del 95%, riferiscono i ricercatori.
Nel modello di carcinoma mammario metastatico, il trattamento di topi con cisplatino rivestiti di nanoparticelle ha prolungato la sopravvivenza degli animali di settimane; Il 50% dei topi sopravviveva a 54 giorni con nanoparticelle rispetto ai 37 giorni con la stessa dose di cisplatino libero. La maggiore efficacia in tre diversi modelli di tumore dimostra che questa strategia può essere applicabile a diversi tipi di cancro, Jinzhi Du dice.