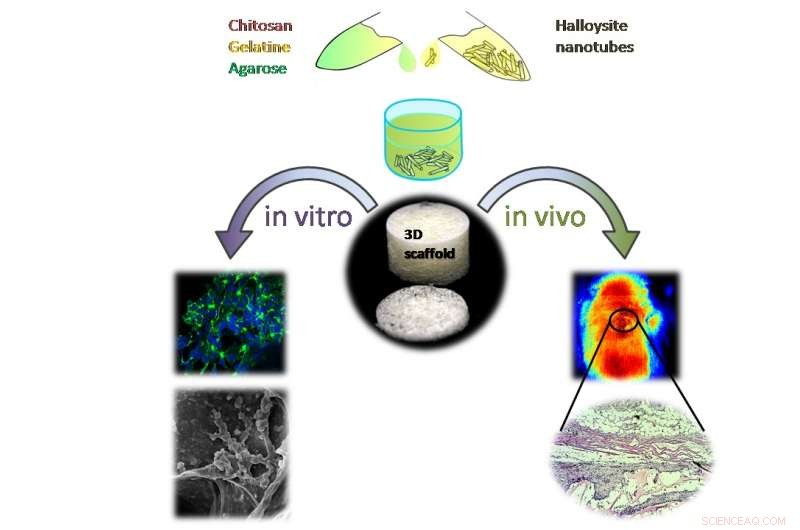
Uno schizzo che dimostra la fabbricazione e il test in vitro e in vivo di un nuovo scaffold di ingegneria tissutale biopolimerica drogato con halloysite. Credito:Laboratorio di bionanotecnologia, Istituto di Medicina Fondamentale e Biologia, Università federale di Kazan,
La fabbricazione di un tessuto prototipo con proprietà funzionali vicine ai tessuti naturali è cruciale per un trapianto efficace. Gli scaffold di ingegneria tissutale sono tipicamente utilizzati come supporti che consentono alle cellule di formare strutture simili a tessuti essenzialmente necessarie per il corretto funzionamento delle cellule nelle condizioni vicine al tessuto tridimensionale.
Gli scienziati del laboratorio di bionanotecnologia dell'Università federale di Kazan hanno combinato biopolimeri chitosano e agarosio (polisaccaridi) e proteine di gelatina per produrre scaffold di ingegneria tissutale e hanno dimostrato il miglioramento della resistenza meccanica, maggiore assorbimento di acqua e proprietà termiche negli idrogel di chitosano-gelatina-agarosio drogati con halloysite.
chitosano, un biopolimero naturale biodegradabile e chimicamente versatile, è stato efficacemente utilizzato in antibatterico, antimicotico, formulazioni antitumorali e immunostimolanti. Per superare gli svantaggi degli scaffold in chitosano puro come fragilità meccanica e bassa resistenza biologica, gli scaffold in chitosano sono tipicamente drogati con altri composti di supporto che consentono il rafforzamento meccanico, ottenendo così scaffold compositi biologicamente resistenti.
L'agarosio è un polisaccaride dello scheletro a base di galattosio isolato da alghe rosse, con notevoli proprietà meccaniche utili nella progettazione di scaffold di ingegneria tissutale.
La gelatina è formata dal collagene per idrolisi (rompendo la struttura a tripla elica in molecole a singolo filamento) e presenta numerosi vantaggi rispetto al suo precursore. È meno immunogenico rispetto al collagene e conserva sequenze segnale informative che promuovono l'adesione cellulare, migrazione, differenziazione e proliferazione.
Le irregolarità superficiali dei pori dell'impalcatura derivano da componenti nanodimensionali insolubili; questi promuovono la migliore adesione delle cellule sui materiali dell'impalcatura, mentre i riempitivi di nanoparticelle aumentano la resistenza dei compositi. Così, i ricercatori hanno drogato nanotubi di halloysite in una matrice di chitosano-agarosio-gelatina per progettare gli scaffold cellulari 3-D impiantabili.
Gli scaffold risultanti dimostrano memoria di forma alla deformazione e hanno la struttura porosa adatta per l'adesione e la proliferazione cellulare, essenziale per la fabbricazione di tessuti artificiali. Osservazioni macroscopiche hanno confermato che tutti i campioni di scaffold mostrano il comportamento spugnoso con memoria di forma e ricostituzione della forma dopo deformazione sia allo stato umido che a quello secco.
Gli esperimenti di rigonfiamento hanno indicato che l'aggiunta di halloysite può migliorare notevolmente l'idrofilia e la bagnabilità degli scaffold compositi. L'incorporazione di nanotubi di halloysite negli scaffold aumenta l'assorbimento di acqua e di conseguenza migliora la biocompatibilità. Le proprietà intrinseche dei nanotubi di halloysite possono essere utilizzate per migliorare la biocompatibilità degli scaffold mediante il caricamento e il rilascio prolungato di diversi composti bioattivi. Ciò offre la prospettiva di scaffold con proprietà definite per la differenziazione diretta di cellule su matrici a causa del rilascio graduale di fattori di differenziazione.
Esperimenti su due tipi di cellule cancerose umane (A549 e Hep3B) mostrano che l'adesione e la proliferazione cellulare in vitro sui nanocompositi si verificano senza cambiamenti nella vitalità e nella formazione del citoscheletro.
Un'ulteriore valutazione in vivo della biocompatibilità e della biodegradabilità nei ratti ha confermato che gli scaffold promuovono la formazione di nuovi vasi sanguigni intorno ai siti di impianto. Gli scaffold mostrano un eccellente riassorbimento entro sei settimane dall'impianto nei ratti. La neo-vascolarizzazione osservata nel tessuto connettivo di nuova formazione posizionato vicino all'impalcatura consente il completo ripristino del flusso sanguigno.
I risultati ottenuti indicano che gli scaffold drogati con halloysite sono biocompatibili come dimostrato sia in vitro che in vivo. Inoltre, confermano il grande potenziale degli scaffold porosi nanocompositi di chitosano-agarosi-gelatina drogati con halloysite nell'ingegneria dei tessuti con il potenziale per il rilascio prolungato di farmaci in nanotubi.