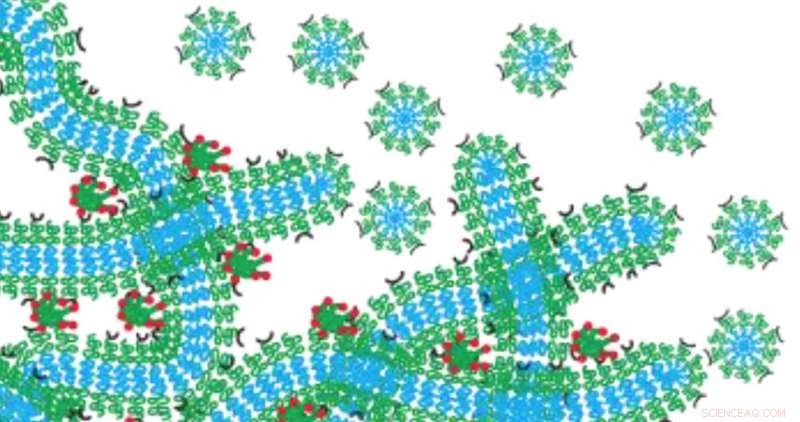
La rete di idrogel di Evan Scott funziona come un deposito di farmaci che si degrada lentamente scomponendosi in micelle. Credito:Northwestern University
Poiché possono essere programmati per viaggiare nel corpo e mirare selettivamente al cancro e ad altri siti di malattia, veicoli su scala nanometrica chiamati nanocarrier possono fornire concentrazioni più elevate di farmaci per bombardare aree specifiche del corpo riducendo al minimo gli effetti collaterali sistemici. I nanovettori possono anche fornire farmaci e agenti diagnostici che in genere non sono solubili in acqua o sangue, nonché ridurre significativamente il dosaggio efficace.
Sebbene questo metodo possa sembrare ideale per il trattamento delle malattie, i nanovettori non sono privi di sfide.
"Controllato, il parto sostenuto è vantaggioso per il trattamento di molti disturbi cronici, ma questo è difficile da ottenere con i nanomateriali senza indurre un'infiammazione locale indesiderata, ", ha affermato Evan Scott della Northwestern University. "Invece, i nanomateriali vengono generalmente somministrati come iniezioni multiple separate o come trasfusione che può richiedere più di un'ora. Sarebbe fantastico se i medici potessero fare una sola iniezione, che ha rilasciato continuamente nanomateriali per un periodo di tempo controllato."
Ora Scott, un assistente professore di ingegneria biomedica presso la McCormick School of Engineering della Northwestern, ha sviluppato un nuovo meccanismo che lo rende controllato, consegna sostenuta possibile.
Il team di Scott ha progettato una formulazione di nanocarrier che, dopo essersi rapidamente formata in un gel all'interno del corpo nel sito di iniezione, può rilasciare continuamente veicoli su nanoscala carichi di farmaci per mesi. Il gel stesso si riassembla nei nanovettori, quindi dopo che tutto il farmaco è stato consegnato, nessun materiale residuo è lasciato per indurre l'infiammazione o la formazione di tessuto fibroso. Questo sistema potrebbe, Per esempio, consentire vaccini a somministrazione singola che non richiedono richiami e un nuovo modo di somministrare la chemioterapia, terapia ormonale, o farmaci che facilitano la guarigione delle ferite.
Supportato dalla National Science Foundation e dal National Institutes of Health, la ricerca è stata pubblicata oggi online, 12 febbraio sul diario Comunicazioni sulla natura . Nicola Karabin, uno studente laureato nel laboratorio di Scott, è stato il primo autore del giornale. Kenneth Shull della Northwestern Engineering, professore di scienze e ingegneria dei materiali, anche contribuito al lavoro. Membro del Simpson Querrey Institute for BioNanotechnology and Chemistry of Life Processes Institute della Northwestern, Scott è stato l'autore corrispondente e ha guidato lo sviluppo delle nanoparticelle e la convalida in vivo.
Attualmente, i più comuni sistemi di somministrazione prolungata di nanocarrier contengono nanomateriali all'interno di matrici polimeriche. Queste reti sono impiantate nel corpo, dove rilasciano lentamente i vettori di droga intrappolati per un periodo di tempo. Il problema sta dopo che la consegna è completata:le reti rimangono all'interno del corpo, spesso suscitando una risposta da corpo estraneo. La rete residua può causare disagio e infiammazione cronica nel paziente.
Per aggirare questo problema, Scott ha sviluppato un nanocarrier utilizzando autoassemblanti, nanomateriali a forma di filamento, che sono caricati con un farmaco o un agente di imaging. Quando reticolati insieme, i filamenti formano una rete di idrogel simile al tessuto strutturale del corpo umano. Dopo che i filamenti sono stati iniettati nel corpo, la risultante rete di idrogel funziona come un deposito di farmaci che si degrada lentamente scomponendosi in nanomateriali sferici chiamati micelle, programmati per raggiungere obiettivi specifici. Poiché la rete si trasforma nel sistema di somministrazione dei farmaci, niente è meno indietro per causare infiammazione.
"Tutto il materiale trattiene il farmaco e poi lo consegna, " ha spiegato Scott. "Si degrada in modo controllato, ottenendo nanomateriali di uguale forma e dimensione. Se carichiamo un farmaco nei filamenti, le micelle prendono il farmaco e se ne vanno con esso."
Dopo aver testato il sistema sia in vitro che in vivo su un modello animale, Il team di Scott ha dimostrato di poter somministrare un'iniezione sottocutanea che ha consegnato lentamente nanomateriali alle cellule nei linfonodi per oltre un mese in modo controllato.
Scott ha affermato che il sistema può essere utilizzato per altre nanostrutture oltre alle micelle. Per esempio, il sistema potrebbe includere nanoparticelle a forma di vescicola, come liposomi o poliersomi, che hanno droghe, proteine, o anticorpi intrappolati all'interno. Vescicole diverse potrebbero trasportare farmaci diversi e rilasciarli a velocità diverse una volta all'interno del corpo.
"Stiamo quindi cercando modi per adattare il sistema alle esigenze di malattie e terapie specifiche, "Scott ha detto. "Stiamo attualmente lavorando per trovare modi per fornire chemioterapici e vaccini. La chemioterapia di solito richiede la somministrazione di più farmaci tossici ad alte concentrazioni, e potremmo fornire tutti questi farmaci in un'unica iniezione a dosaggi molto più bassi. Per l'immunizzazione, questi idrogel iniettabili potrebbero essere somministrati come vaccini standard, ma stimola più a lungo specifiche cellule del sistema immunitario, periodi di tempo controllati e potenzialmente evitare la necessità di booster."